Clear Sky Science · he
LRG1 שמקורו בהפטוציטים מכין את הכבד למטסטזות ומפחית את יעילות האימונותרפיה
למה המחקר הזה חשוב לחולי סרטן
הסרטנים לעתים חוזרים לא באיבר המקורי אלא במקומות מרוחקים כמו הכבד, וברגע שזה קורה הטיפולים נעשים בעלי תועלת מופחתת. במחקר זה חושפים כיצד הכבד «מוכן» בשקט מראש לקבל תאים סרטניים נודדים, ולמה גידולים שהתפשטו לכבד לעתים קרובות עמידים בפני תרופות אימונותרפיות מודרניות. בזיהוי חלבון כבד יחיד, LRG1, כמפתח בתהליך הזה, העבודה מציעה דרכים חדשות לחזות, למנוע ולטפל טוב יותר במטסטזות לכבד.
אות אזהרה בדם
רופאים כבר יודעים שסוגי סרטן כמו קולורקטלי, לבלב וקיבה מתפשטים לעתים קרובות לכבד, אבל לא היו להם כלים טובים לחזות מי בסיכון הגבוה ביותר. החוקרים ניתחו דגימות דם מחולים עם סוגי סרטן אלה וגילו כי אלה שכבר פיתחו מטסטזות בכבד נשאו רמות גבוהות בהרבה של חלבון הנקרא LRG1 בדם. אפילו יותר בולט — בקרב אנשים עם מחלה בשלבים מוקדמים וללא התפשטות ניתנת לגילוי, אלה שמאוחר יותר פיתחו מטסטזות בכבד כבר הציגו רמות גבוהות של LRG1 באבחון ונוטו להישנות מוקדמת יותר. במספר מודלים עכבריים החקים אדם, רמות LRG1 במחזור הדם עלו שבועות לפני שהופיעו גידולים נראים בכבד, וסימנו את שלב ה"טרום‑מטסטטי" שבו האיבר מעוצב מחדש לטובת גדילת גידול עתידי. 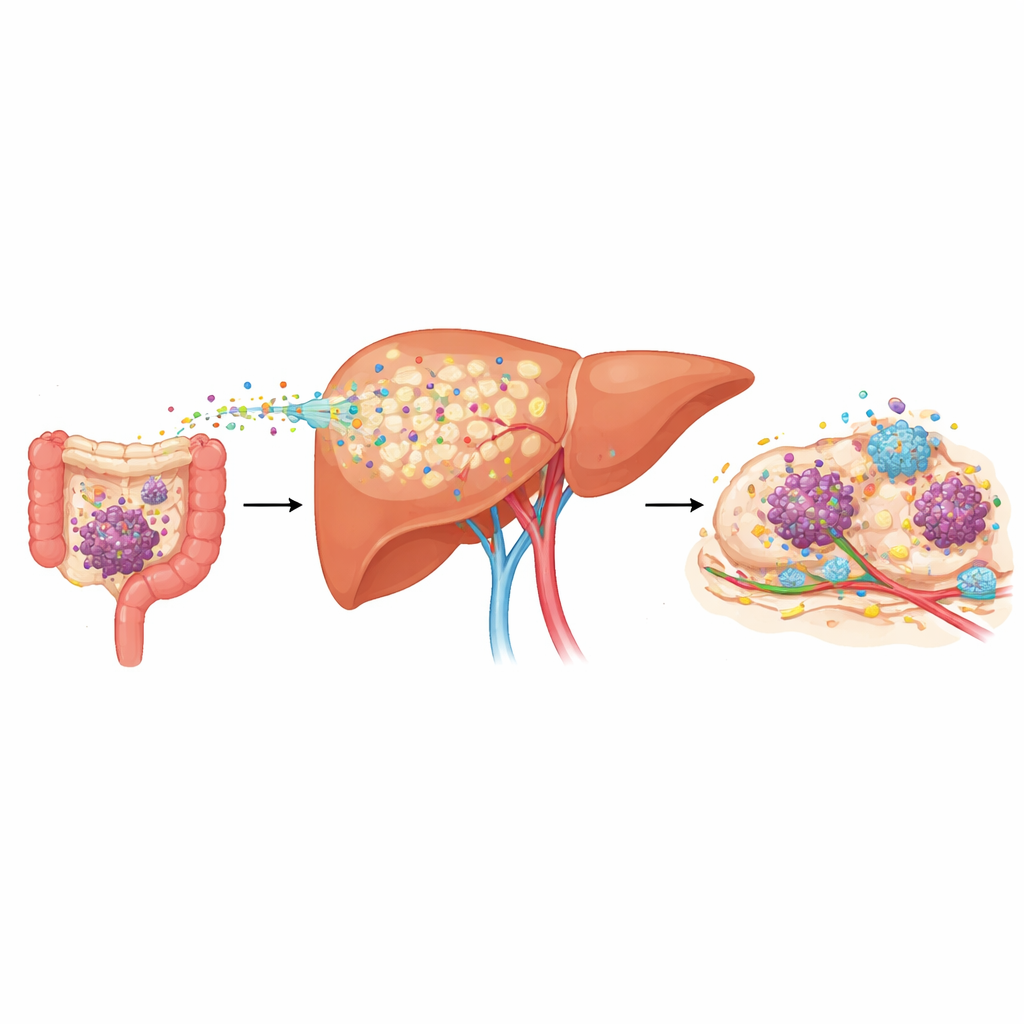
הכבד אינו רק קורבן פסיבי
כדי לעקוב מאיפה מגיעה קפיצת ה‑LRG1 הזו, הצוות בחן הרבה איברים וסוגי תאים בעכברים נושאי גידולים. הכבד בלט כמקור הדומיננטי, ובתוך הכבד, תאים פשוטים של הכבד (הפטוציטים) ייצרו הרבה יותר LRG1 מתאי מערכת החיסון או מתאי כלי הדם. כאשר המדענים השתמשו בהנדסה גנטית כדי למחוק את הגן Lrg1 רק בהפטוציטים, רמות הדם של LRG1 כמעט שלא עלו במהלך התקדמות הסרטן, והבעלי חיים פיתחו הרבה פחות מטסטזות בכבד ואלה היו קטנות יותר. למעשה, כאשר זרעו גידולים בכבד בדרך שלרוב מניבה עומס מחלה גבוה, הסרת LRG1 שמקורו בהפטוציטים קיצצה באופן דרמטי הן במספר מוקדי המטסטזות והן בגודלן, מה שמראה שחלבון זה שמיוצר בכבד מהווה מאיץ חזק של התפשטות.
שינוי מפת המערכת החיסונית של הכבד
השאלה הבאה הייתה איך LRG1 הופך כבד בריא לאדמת פורייה לסרטן. בעזרת ריצוף תא‑יחיד, החוקרים מיפו עשרות אלפי תאי כבד בודדים מעכברים בריאים ומנושאי גידול. בכבדים שנחשפו לגידול מרוחק ראו זרימה של תאי דם לבנים מסוימים שמדכאים חיסון, במיוחד נויטרופילים ותאי מיולואיד קשורים, בעוד שתאי T ו‑dendritic התומכים פחתו או נכנסו למצב תשישות. כאשר LRG1 נעדר מהפטוציטים, ההטיה הזו לעבר סביבה מדכאת חיסון הוחזרה במידה רבה. הצוות מצא כי LRG1 מפעיל ישירות נויטרופילים לשחרר מבנים דביקים בצורת רשת הידועים כרשתות חוץ‑תאיות של נויטרופילים (NETs). רשתות DNA אלו נוצרות בתוך כלי הדם של הכבד, תופסות תאי סרטן במעגל ומסייעות להם להתעגן, לשרוד ולגדול. פיצוח NETs עם אנזים, או דילול נויטרופילים, הפחית בחדות את המטסטזות בכבד וביטל במידה רבה את היתרון שניתן על ידי LRG1, וקישר מנגנון זה ישירות להתפשטות הגידול.
כיצד דלקת בגידולים מתקשרת לכבד
מה גורם להפטוציטים להגביר את ייצור LRG1 מלכתחילה? החוקרים הראו שמדובר לא במגע ישיר עם תאי הגידול, אלא באותות דלקתיים במחזור הדם. מתוך רבים מולקולות מועמדות, שליח הדלקת IL‑6 יצא ככוח המניע המרכזי: הוספת IL‑6 לתאי כבד בצלחת גרמה לאינדוקציה חזקה של LRG1, בעוד שחסימת IL‑6 או הקולטן שלו מנעה זאת. בעכברים, רמות IL‑6 עלו יחד עם LRG1 בשלב הטרום‑מטסטטי, והגברה מלאכותית של IL‑6 בכבד הגדילה את ייצור ה‑LRG1 והאיצה מטסטזות — אלא אם כן ההפטוציטים נטלו LRG1. ניתוח נוסף הצביע על מקרופאגים — תאי חיסון שמעוצבים על ידי הגידול המתפתח — כמקור מרכזי של IL‑6 בכבד, וחשף שרשרת תקשורת: דלקת הגידול מפעילה מקרופאגים, מקרופאגים משחררים IL‑6, IL‑6 מנחה את ההפטוציטים להפריש LRG1, ו‑LRG1 מעצב את הסביבה החיסונית והכלילית של הכבד לטובת תאי סרטן עתידיים. 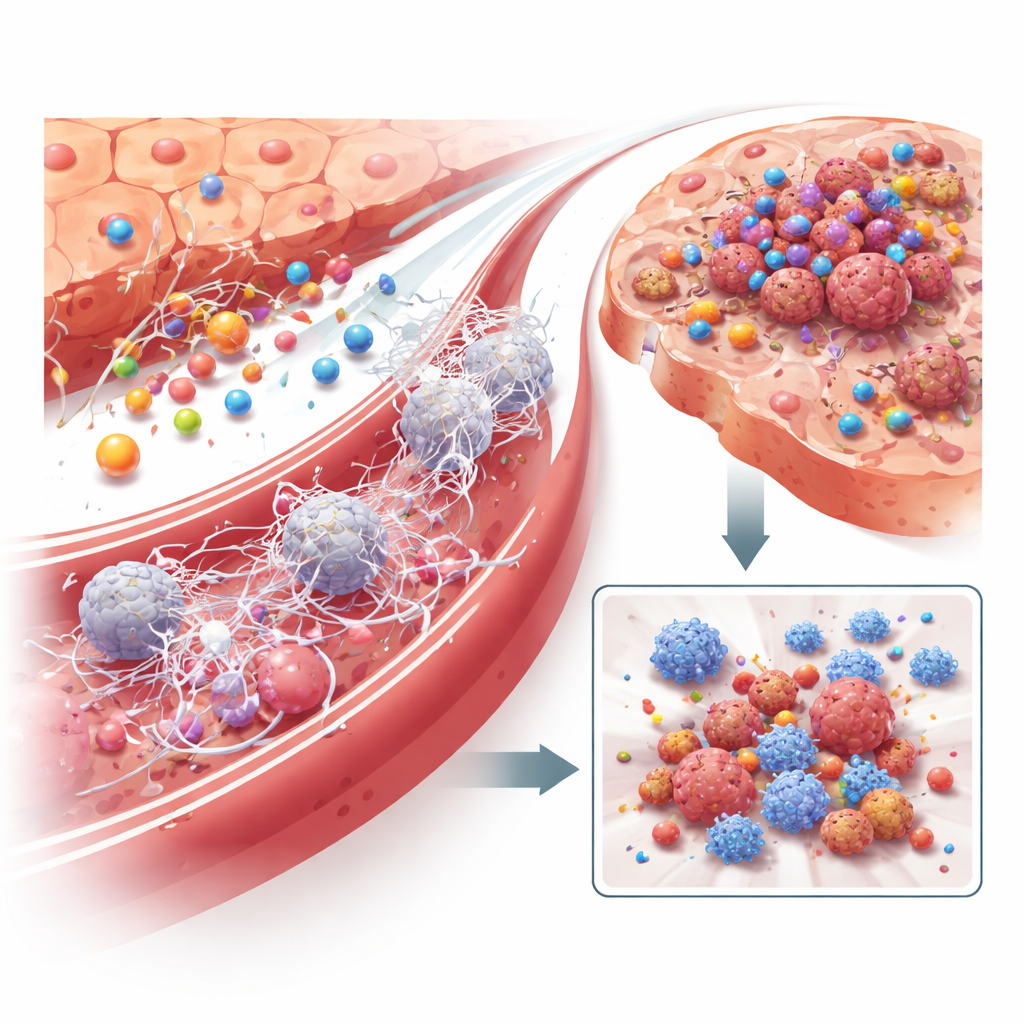
להפוך סביבת עוין לקרקע ידידותית
מכיוון ש‑LRG1 עומד בצומת קריטית זו, החוקרים בדקו האם חסימתו יכולה להיות טיפולית. בעכברים עם מטסטזות כבד שנוצרו ניסוונית, טיפול בנוגדן נגד LRG1 הפחית יצירת NETs והקטין באופן משמעותי את מספר וגודל גידולי הכבד. גישת גן שנותקה באופן סלקטיבי את Lrg1 בהפטוציטים הניבה יתרונות דומים. חשוב לציין שמטסטזות כבד ידועות כמדכאות את השפעת נוגדני נקודות בקרה אימוניות כמו אנטי‑PD‑1. כאשר המדענים שילבו חסימת LRG1 עם טיפול אנטי‑PD‑1 במודל גידול כבד, הגידולים הצטמצמו הרבה יותר מאשר בכל טיפול בנפרד, ותאי חיסון אגרסיביים (תאי CD8) הפכו לרבים יותר ופעילים יותר בהרג תאי סרטן. ממצא זה מרמז שכוונון LRG1 יכול להפוך מטסטזה "קרה" מבחינה אימונית ל"חמה" יותר, שמגיבה טוב יותר לאימונותרפיה.
מה משמעות הדבר לטיפול עתידי
בסך הכל, עבודה זו מראה שהכבד עובד באופן אקטיבי לפי תכתיבים של גידולים מרוחקים כדי להפוך למעגן בטוח לתאי סרטן, ושה‑LRG1 שמקורו בהפטוציטים הוא שליח מרכזי בתהליך זה. מדידת LRG1 בדם עשויה לעזור לזהות חולים בסיכון גבוה להתפשטות לכבד לפני הופעת מטסטזות, בעוד שתרופות החוסמות את LRG1 או את אות ה‑IL‑6 שמעליו יכולות גם למנוע מטסטזות בכבד וגם להפוך נגעים קיימים לפגיעים יותר להתקפה חיסונית. אף שהממצאים כרגע מוגבלים לעכברים ודגימות מטופלים ולא ניסויים קליניים, הם מדגישים אסטרטגיה מבטיחה חדשה: במקום לחכות לטפל במטסטזות לאחר שהן נוצרו, ייתכן שנוכל מראש לנטרל את "שטיח הקבלת הפנים" שהכבד מפיש עבור הסרטן.
ציטוט: Long, G., Cheng, B., Jiang, Y. et al. Hepatocyte-derived LRG1 primes the liver for metastasis and impairs immunotherapy. Cell Mol Immunol 23, 560–574 (2026). https://doi.org/10.1038/s41423-026-01408-9
מילות מפתח: מטסטזות בכבד, LRG1, מיקרו‑סביבה חיסונית, רשתות חוץ‑תאיות של נויטרופילים, אימונותרפיה נגד סרטן