Clear Sky Science · ar
بروتين LRG1 المشتق من الخلايا الكبدية يمهّد للكبد لحدوث النقائل ويضعف العلاج المناعي
لماذا يهم هذا البحث لمرضى السرطان
غالبًا ما يعود السرطان ليس في العضو الأصلي بل في مواقع بعيدة مثل الكبد، ومتى حدث ذلك تصبح العلاجات أقل فعالية بكثير. يكشف هذا البحث كيف يُعدّ الكبد بهدوء مسبقًا لاستقبال الخلايا السرطانية المهاجرة، ولماذا تقاوم الأورام التي تنتشر إلى الكبد غالبًا أدوية العلاج المناعي الحديثة. من خلال تحديد بروتين واحد تصنعه الكبد، LRG1، كمفتاح رئيسي في هذه العملية، يقترح العمل طرقًا جديدة للتنبؤ بنخاطر، والوقاية من، وعلاج نقائل الكبد بشكل أفضل.
إشارة تحذير في الدم
لطالما لاحظ الأطباء أن سرطانات مثل القولون والمستقيم والبنكرياس والمعدة تنتشر كثيرًا إلى الكبد، لكنهم افتقروا إلى أدوات جيدة للتنبؤ بمن هم الأكثر عرضةً. حلل الباحثون عينات دم من مرضى بهذه السرطانات ووجدوا أن من لديهم نقائل كبدية بالفعل حملوا مستويات أعلى بكثير من بروتين يسمى LRG1 في دمهم. والأكثر لفتًا للانتباه، أن الأشخاص ذوي المرض في مراحله المبكرة وبدون انتشار قابل للكشف، والذين تطورت لديهم لاحقًا نقائل كبدية، كانت لديهم مستويات مرتفعة من LRG1 عند التشخيص وكانوا يميلون للانتكاس أسرع. في عدة نماذج فأرية تحاكي السرطان البشري، ارتفع مستوى LRG1 في مجرى الدم أسابيع قبل ظهور أورام كبد مرئية، مؤكّدًا ما يُسمى بمرحلة "ما قبل النقيلة" عندما يعاد تشكيل العضو ليصبّح مواتٍ لنمو الورم المستقبلي. 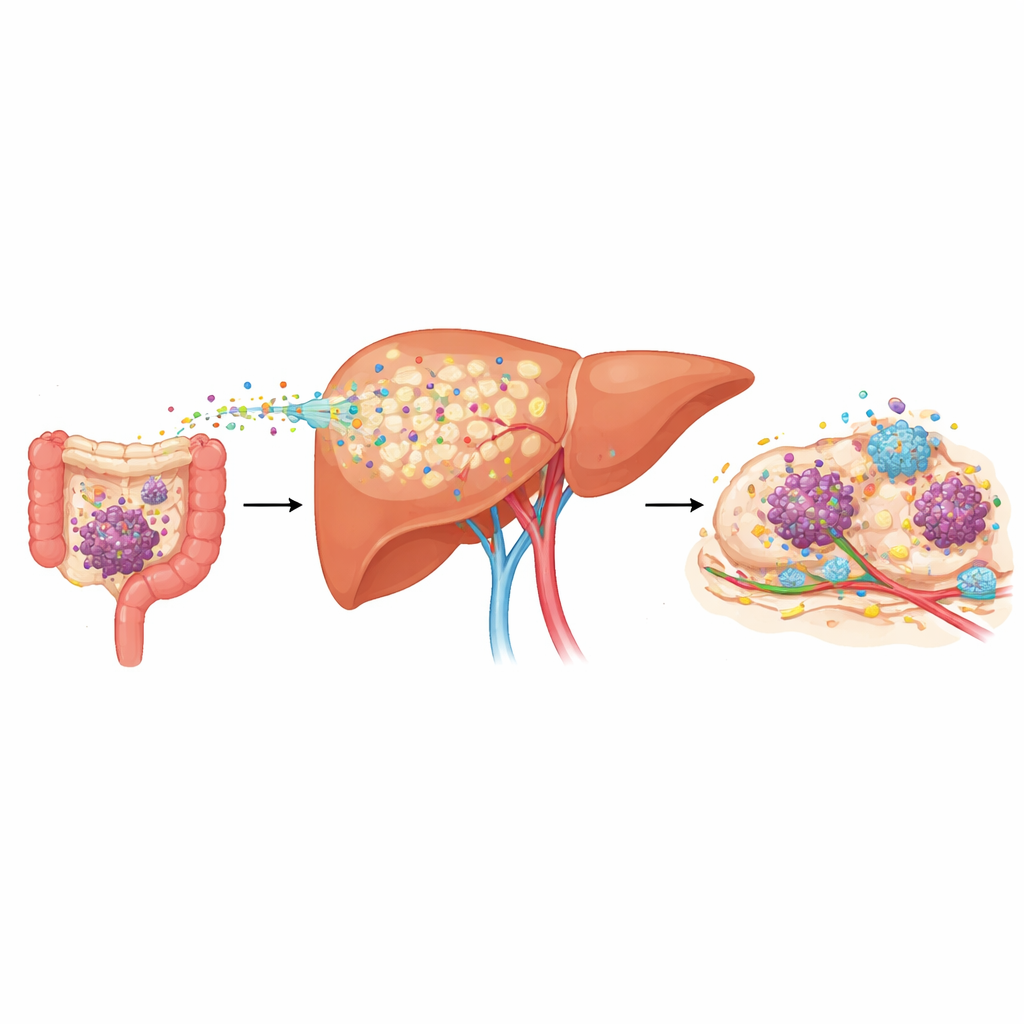
الكبد ليس ضحية سلبية فحسب
لتتبع مصدر هذا الارتفاع في LRG1، فحص الفريق العديد من الأعضاء وأنواع الخلايا في الفئران الحاملة للأورام. برز الكبد كمصدر مهيمن، وداخل الكبد كانت الخلايا الكبدية العادية (خلايا الكبد) تنتج كمية أكبر بكثير من LRG1 مقارنة بالخلايا المناعية أو خلايا الأوعية الدموية. عندما استخدم العلماء الهندسة الوراثية لحذف جين Lrg1 فقط في الخلايا الكبدية، بالكاد ارتفعت مستويات LRG1 في الدم خلال تقدم السرطان، وظهرت لدى الحيوانات نقائل كبدية أقل بكثير وأصغر حجمًا. في الواقع، عندما زرعوا أورامًا كبدية بطريقة تُنتج عادة عبئًا مرضيًا عاليًا، أدى إزالة LRG1 المشتق من الخلايا الكبدية إلى خفض حاد في كلٍّ من عدد البؤر النقيلية وحجمها، ما يبيّن أن هذا البروتين المنتج في الكبد يسهّل الانتشار بقوة.
إعادة توصيل المشهد المناعي في الكبد
كان السؤال التالي كيف يحول LRG1 كبدًا سليمًا إلى أرض خصبة للسرطان. باستخدام التسلسل الخلوي الفردي، رسم الباحثون خريطة لعشرات الآلاف من خلايا الكبد الفردية من فئران صحية وحاملة للأورام. في الكبد المعرض لورم بعيد، لاحظوا تدفقًا لأنواع معينة من خلايا الدم البيضاء التي تُخمد المناعة، خاصة النيوتروفيلات والخلايا النخاعية المرتبطة بها، بينما تقلّ أو تستنزف الخلايا التائية المفيدة وخلايا التغصن. عندما غاب LRG1 عن الخلايا الكبدية، انقلب هذا الانحراف نحو بيئة مثبطة للمناعة إلى حد كبير. وجد الفريق أن LRG1 ينشط النيوتروفيلات مباشرة لإطلاق هياكل لزجة تشبه الشبكات تُعرف بالشبكات الخارجية للنيوتروفيلات، أو NETs. تتكوّن هذه الشباك من الحمض النووي داخل أوعية الدم الكبدية، فتحتجز الخلايا السرطانية الدائرة وتساعدها على الالتصاق والنجاة والنمو. تفكيك NETs بواسطة إنزيم، أو استنفاد النيوتروفيلات، قلل بشدة من نقائل الكبد ومحو إلى حد كبير الميزة التي يمنحها LRG1، ربطًا مباشرًا لهذه الآلية بانتشار الورم.
كيف تتواصل الالتهابات الورمية مع الكبد
ما الذي يجعل الخلايا الكبدية ترفع إنتاج LRG1 في المقام الأول؟ بيّن الباحثون أنه ليس التواصل المباشر مع خلايا الورم، بل الإشارات الالتهابية المتداولة في الدم. من بين العديد من الجزيئات المرشحة، برز الرسول الالتهابي IL‑6 كسائق رئيسي: إضافة IL‑6 إلى خلايا الكبد في طبق الثقافة حثّت بشدة على إنتاج LRG1، بينما منع حجب IL‑6 أو مستقبلها هذا التأثير. في الفئران، ارتفعت مستويات IL‑6 إلى جانب LRG1 خلال مرحلة ما قبل النقيلة، وزيادة IL‑6 اصطناعيًا في الكبد عززت إنتاج LRG1 وسرعت النقائل—إلا إذا كانت الخلايا الكبدية تفتقر إلى LRG1. أشارت تحليلات إضافية إلى أن البلعمات الكبيرة (الماكروفاجات)—خلايا مناعية تتأثر بالورم المتنامي—هي مصدر رئيسي للـ IL‑6 في الكبد، مكشوفة سلسلة من التواصل: التهاب الورم ينشط الماكروفاجات، والماكروفاجات تفرز IL‑6، وIL‑6 توجّه الخلايا الكبدية لإفراز LRG1، ثم يعيد LRG1 تشكيل بيئة الكبد المناعية والوعائية لصالح الخلايا السرطانية المستقبلية. 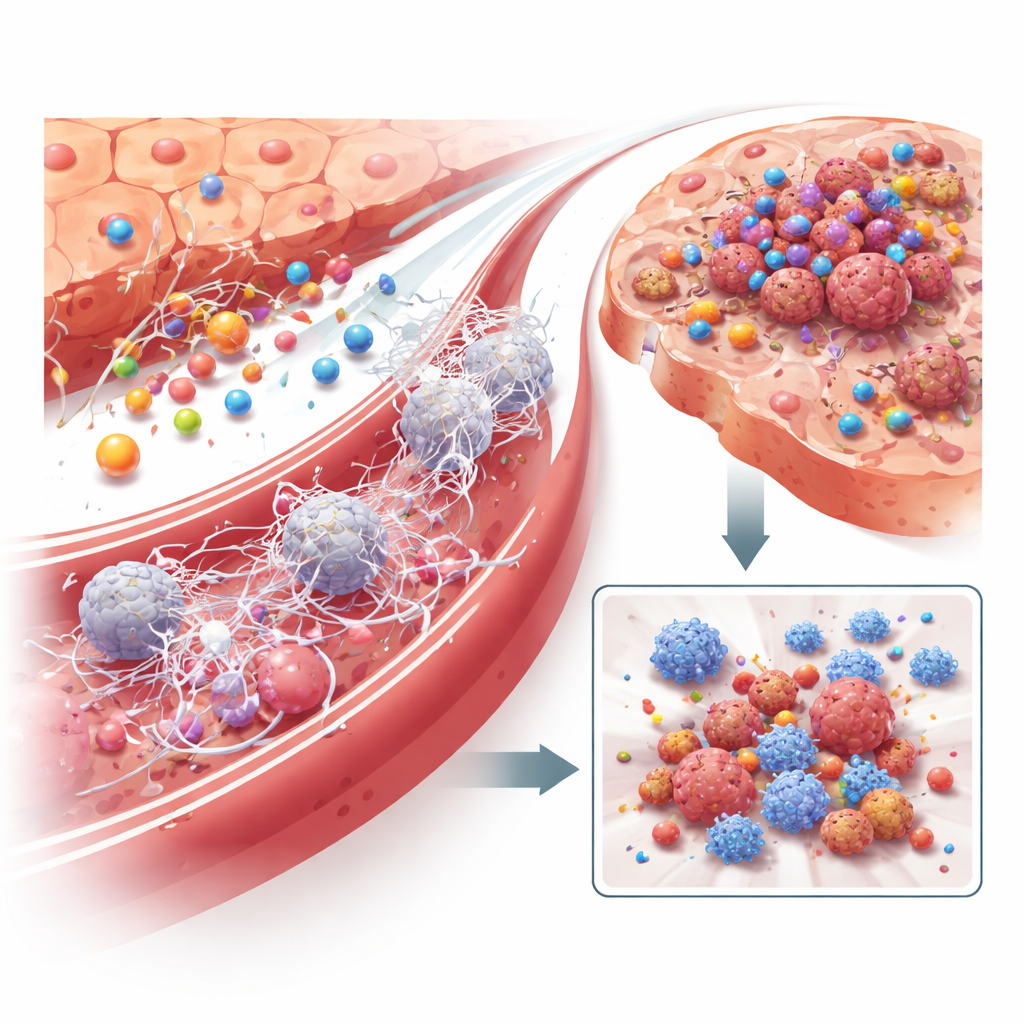
إعادة تحويل الموطن المعادي إلى أرض صديقة
لأن LRG1 يقع عند هذا المفترق الحاسم، اختبر الباحثون ما إذا كان حظره يمكن أن يكون علاجًا. في فئران لها نقائل كبدية مستحثة تجريبيًا، قلّ علاج بالأجسام المضادة ضد LRG1 من تكوّن NETs وخفّض بشكل كبير عدد وحجم أورام الكبد. كما حقق نهج علاج جيني صمتًا انتقائيًا للجين Lrg1 في الخلايا الكبدية فوائد مماثلة. من المهم أن نقائل الكبد معروفة بتقليل فعالية أدوية نقاط التفتيش المناعية مثل الأجسام المضادة المضادة لـ PD‑1. عندما جمع العلماء حجب LRG1 مع علاج مضاد‑PD‑1 في نموذج ورم كبد، تقلّصت الأورام بشكل أكبر مما كان عليه مع أي من العلاجين بمفرده، وأصبحت الخلايا المناعية العدوانية (خلايا T CD8) أكثر عددًا وأكثر فاعلية سامة للسرطان. هذا يوحي أن استهداف LRG1 يمكن أن يحول نقيلة كبدية من حالة مناعية "باردة" إلى حالة "أدفأ" تستجيب بشكل أفضل للعلاج المناعي.
ماذا يعني هذا للرعاية المستقبلية
بشكل عام، تكشف هذه الدراسة أن الكبد يتلقى إشارات نشطة من أورام بعيدة ليصبح ملاذًا آمنًا للخلايا السرطانية، وأن LRG1 المشتق من الخلايا الكبدية هو رسول رئيسي في هذه العملية. قد يساعد قياس LRG1 في الدم على تحديد المرضى المعرضين لخطر عالٍ لانتشار الكبد قبل ظهور النقائل، في حين أن أدوية تحجب LRG1 أو إشارة IL‑6 التي تسبقه قد تمنع نقائل الكبد وتجعل الآفات الموجودة أكثر عرضة للهجوم المناعي. وعلى الرغم من أن هذه النتائج محصورة حتى الآن في نماذج فأرية وعينات مرضى وليس في تجارب سريرية، فإنها تبرز استراتيجية واعدة جديدة: بدل الانتظار لعلاج النقائل بعد تكونها، قد نعمل على نزع فتيل "سجادة الترحيب" التي يفردها الكبد للسرطان مسبقًا.
الاستشهاد: Long, G., Cheng, B., Jiang, Y. et al. Hepatocyte-derived LRG1 primes the liver for metastasis and impairs immunotherapy. Cell Mol Immunol 23, 560–574 (2026). https://doi.org/10.1038/s41423-026-01408-9
الكلمات المفتاحية: نقائل الكبد, LRG1, البيئة المناعية الدقيقة, الشبكات الخارجية للنيوتروفيلات, العلاج المناعي للسرطان