Clear Sky Science · fr
La LRG1 d’origine hépatocytaire prépare le foie aux métastases et compromet l’immunothérapie
Pourquoi cette recherche compte pour les patients atteints de cancer
Le cancer récidive souvent non pas dans l’organe d’origine mais dans des sites distants comme le foie, et une fois cela arrivé, les traitements deviennent beaucoup moins efficaces. Cette étude révèle comment le foie est discrètement « préparé » à l’avance pour accueillir des cellules cancéreuses itinérantes, et pourquoi les tumeurs qui se propagent au foie résistent fréquemment aux médicaments d’immunothérapie modernes. En identifiant une seule protéine fabriquée par le foie, la LRG1, comme un élément clé de ce processus, ce travail suggère de nouvelles façons de prédire, prévenir et mieux traiter les métastases hépatiques.
Un signal d’alerte dans le sang
Les médecins observent depuis longtemps que des cancers tels que ceux du côlon, du pancréas et de l’estomac se propagent fréquemment au foie, mais manquaient d’outils fiables pour prévoir qui courait le plus de risque. Les chercheurs ont analysé des échantillons de sang de patients atteints de ces cancers et ont constaté que ceux qui avaient déjà des métastases hépatiques présentaient des taux nettement plus élevés d’une protéine nommée LRG1 dans le sang. Plus remarquable encore, parmi les personnes au stade précoce sans dissémination détectable, celles qui ont développé ensuite des métastases hépatiques avaient déjà une LRG1 élevée au diagnostic et rechutaient plus rapidement. Dans plusieurs modèles murins qui reproduisent le cancer humain, la LRG1 sanguine augmentait des semaines avant l’apparition visible de tumeurs hépatiques, marquant la phase dite « pré-métastatique » où l’organe est remodelé pour favoriser la croissance tumorale future. 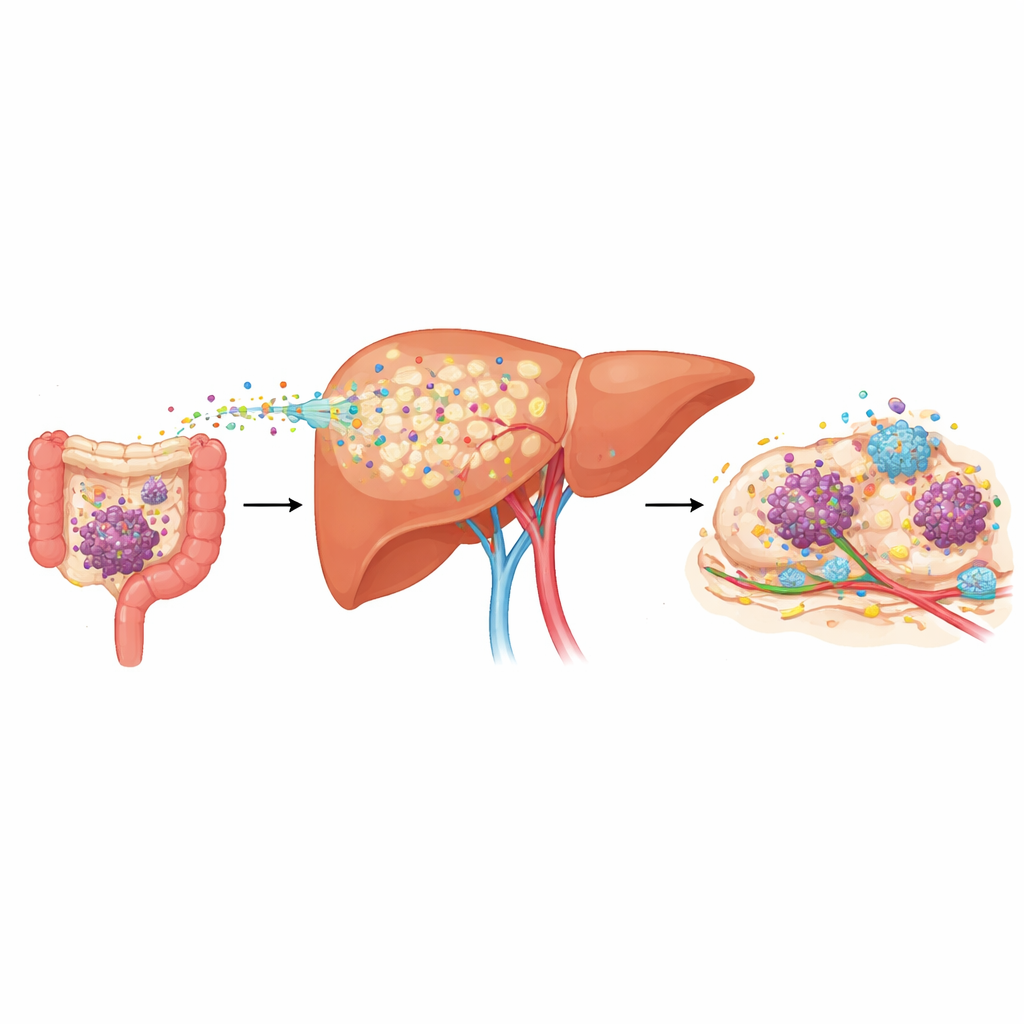
Le foie n’est pas une victime passive
Pour localiser l’origine de cette montée de LRG1, l’équipe a examiné de nombreux organes et types cellulaires chez des souris porteuses de tumeurs. Le foie est apparu comme la source dominante et, au sein du foie, les cellules hépatiques ordinaires (hépatocytes) produisaient beaucoup plus de LRG1 que les cellules immunitaires ou vasculaires. Lorsque les scientifiques ont utilisé l’ingénierie génétique pour supprimer le gène Lrg1 uniquement dans les hépatocytes, les niveaux sanguins de LRG1 n’augmentaient presque plus pendant la progression tumorale, et les animaux développaient beaucoup moins de métastases hépatiques et de plus petite taille. En fait, lorsque des tumeurs hépatiques étaient implantées de manière à produire normalement une forte charge tumorale, la suppression de la LRG1 d’origine hépatocytaire réduisait radicalement à la fois le nombre et la taille des foyers métastatiques, montrant que cette protéine produite par le foie facilite puissamment la dissémination.
Reprogrammer le paysage immunitaire du foie
La question suivante était de savoir comment la LRG1 transforme un foie sain en un terreau fertile pour le cancer. Grâce au séquençage unicellulaire, les chercheurs ont cartographié des dizaines de milliers de cellules hépatiques individuelles provenant de souris saines et porteuses de tumeur. Dans les foies exposés à une tumeur lointaine, ils ont observé un afflux de certains globules blancs qui atténuent l’immunité, en particulier des neutrophiles et des cellules myéloïdes apparentées, tandis que les lymphocytes T utiles et les cellules dendritiques diminuaient ou s’épuis[aie nt]. Lorsque la LRG1 était absente des hépatocytes, ce basculement vers un environnement immunosuppresseur était en grande partie inversé. L’équipe a découvert que la LRG1 active directement les neutrophiles pour qu’ils libèrent des structures collantes en forme de toile appelées filets extracellulaires de neutrophiles, ou NETs. Ces toiles d’ADN se forment à l’intérieur des vaisseaux sanguins hépatiques, piégeant les cellules cancéreuses circulantes et facilitant leur ancrage, leur survie et leur croissance. La dégradation des NETs par une enzyme, ou l’épuisement des neutrophiles, réduisait nettement les métastases hépatiques et effaçait en grande partie l’avantage conféré par la LRG1, liant directement ce mécanisme à la propagation tumorale.
Comment l’inflammation tumorale communique avec le foie
Qu’est-ce qui pousse les hépatocytes à augmenter la production de LRG1 au départ ? Les investigateurs ont montré qu’il ne s’agit pas d’un contact direct avec les cellules tumorales, mais de signaux inflammatoires circulant dans le sang. Parmi de nombreux candidats, le messager inflammatoire IL‑6 est apparu comme le principal moteur : l’ajout d’IL‑6 à des cellules hépatiques en culture induisait fortement la LRG1, tandis que le blocage d’IL‑6 ou de son récepteur l’empêchait. Chez la souris, les taux d’IL‑6 augmentaient parallèlement à la LRG1 lors de la phase pré-métastatique, et l’augmentation artificielle d’IL‑6 dans le foie stimulait la production de LRG1 et accélèrait les métastases—sauf si les hépatocytes étaient dépourvus de LRG1. Des analyses complémentaires ont pointé les macrophages—cellules immunitaires influencées par la tumeur en croissance—comme une source majeure d’IL‑6 dans le foie, révélant une chaîne de communication : l’inflammation tumorale active les macrophages, les macrophages libèrent de l’IL‑6, l’IL‑6 ordonne aux hépatocytes de sécréter la LRG1, et la LRG1 remodèle alors l’environnement immunitaire et vasculaire du foie en faveur des futures cellules cancéreuses. 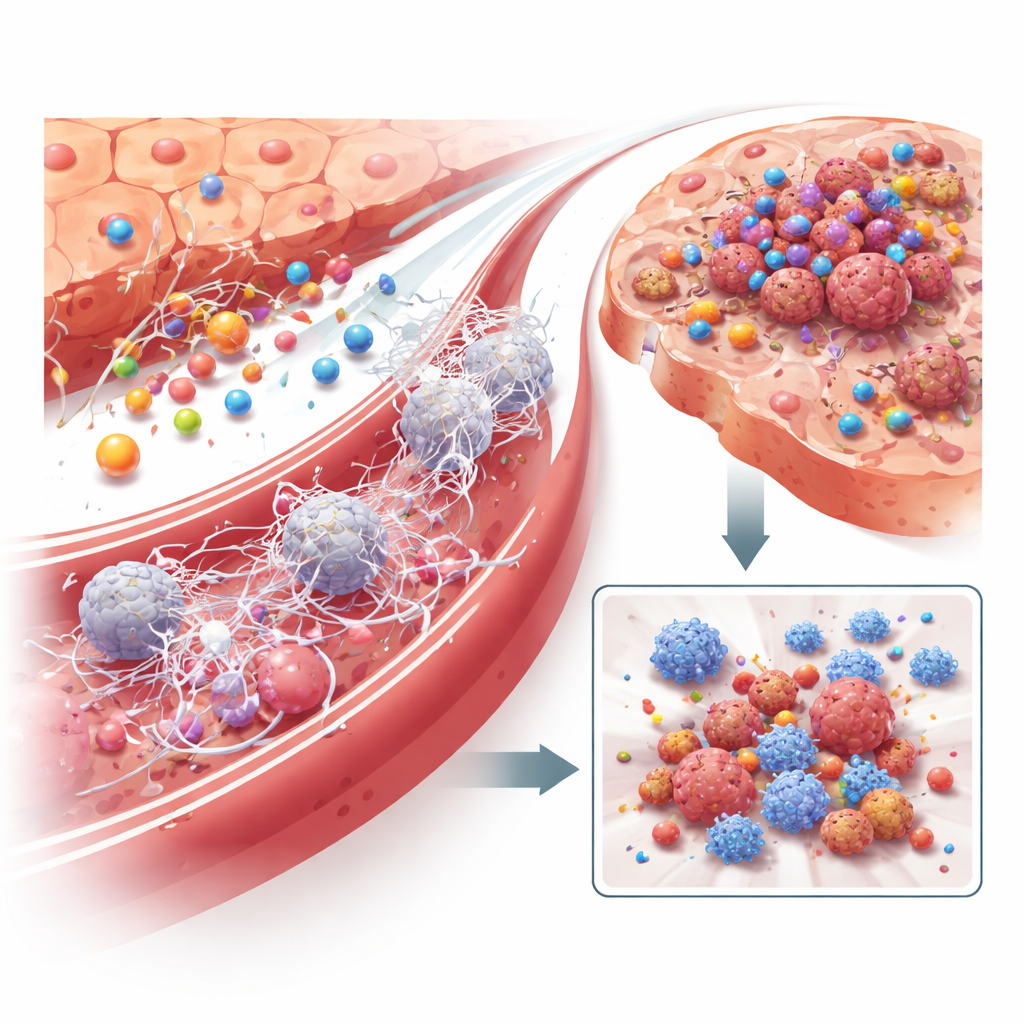
Reconvertir un niche hostile en un terrain moins propice
Parce que la LRG1 se trouve à ce carrefour critique, les chercheurs ont testé si la bloquer pouvait être thérapeutique. Chez des souris avec des métastases hépatiques expérimentales, un traitement par un anticorps anti‑LRG1 réduisait la formation de NETs et diminuait sensiblement le nombre et la taille des tumeurs hépatiques. Une approche de thérapie génique silencieuse ciblant sélectivement Lrg1 dans les hépatocytes a produit des bénéfices similaires. Il est important de noter que les métastases hépatiques sont connues pour atténuer l’effet des inhibiteurs de points de contrôle immunitaires tels que les anticorps anti‑PD‑1. Lorsque les scientifiques ont combiné le blocage de la LRG1 avec une thérapie anti‑PD‑1 dans un modèle de tumeur hépatique, les tumeurs ont régressé beaucoup plus qu’avec l’un ou l’autre traitement seul, et les cellules immunitaires agressives (lymphocytes T CD8) sont devenues plus nombreuses et plus actives contre le cancer. Cela suggère que cibler la LRG1 peut convertir une métastase hépatique immunologiquement « froide » en une métastase « plus chaude » qui répond mieux à l’immunothérapie.
Ce que cela signifie pour les soins futurs
Au total, ce travail révèle que le foie est activement « coaché » par des tumeurs distantes pour devenir un refuge sûr pour les cellules cancéreuses, et que la LRG1 d’origine hépatocytaire est un messager clé de ce coaching. Mesurer la LRG1 dans le sang pourrait aider à identifier les patients à haut risque de dissémination hépatique avant l’apparition des métastases, tandis que des médicaments bloquant la LRG1 ou son signal en amont, l’IL‑6, pourraient à la fois prévenir les métastases hépatiques et rendre les lésions existantes plus vulnérables à l’attaque immunitaire. Bien que ces résultats soient pour l’instant limités à des modèles murins et à des échantillons de patients plutôt qu’à des essais cliniques, ils mettent en lumière une stratégie prometteuse : au lieu d’attendre de traiter les métastases après leur formation, on pourrait désarmer de manière préventive le « tapis d’accueil » que le foie déploie pour le cancer.
Citation: Long, G., Cheng, B., Jiang, Y. et al. Hepatocyte-derived LRG1 primes the liver for metastasis and impairs immunotherapy. Cell Mol Immunol 23, 560–574 (2026). https://doi.org/10.1038/s41423-026-01408-9
Mots-clés: métastase hépatique, LRG1, microenvironnement immunitaire, filets extracellulaires de neutrophiles, immunothérapie contre le cancer