Clear Sky Science · nl
Vetbalans speelt een cruciale rol bij erfelijke en verworven netvliesaandoeningen
Waarom vetten in het oog ertoe doen
De lichtgevoelige cellen achter in het oog behoren tot de meest energieverslindende cellen van het lichaam; ze bouwen voortdurend hun buitenoppervlak opnieuw op zodat we scherp kunnen zien. Hiervoor hebben ze een constante, goed gereguleerde aanvoer van vetten en verwante moleculen nodig. Dit overzichtsartikel legt uit hoe die ‘‘vet-economie’’ van het netvlies normaal functioneert, wat er gebeurt wanneer ze uit balans raakt en hoe dat tekort bijdraagt aan veelvoorkomende blindheidsziekten zoals retinitis pigmentosa, diabetische retinopathie en leeftijdsgebonden maculadegeneratie. Het bespreekt ook opkomende behandelingen die erop gericht zijn het gezichtsvermogen te beschermen door het herstellen van een gezonde lipidenbalans.
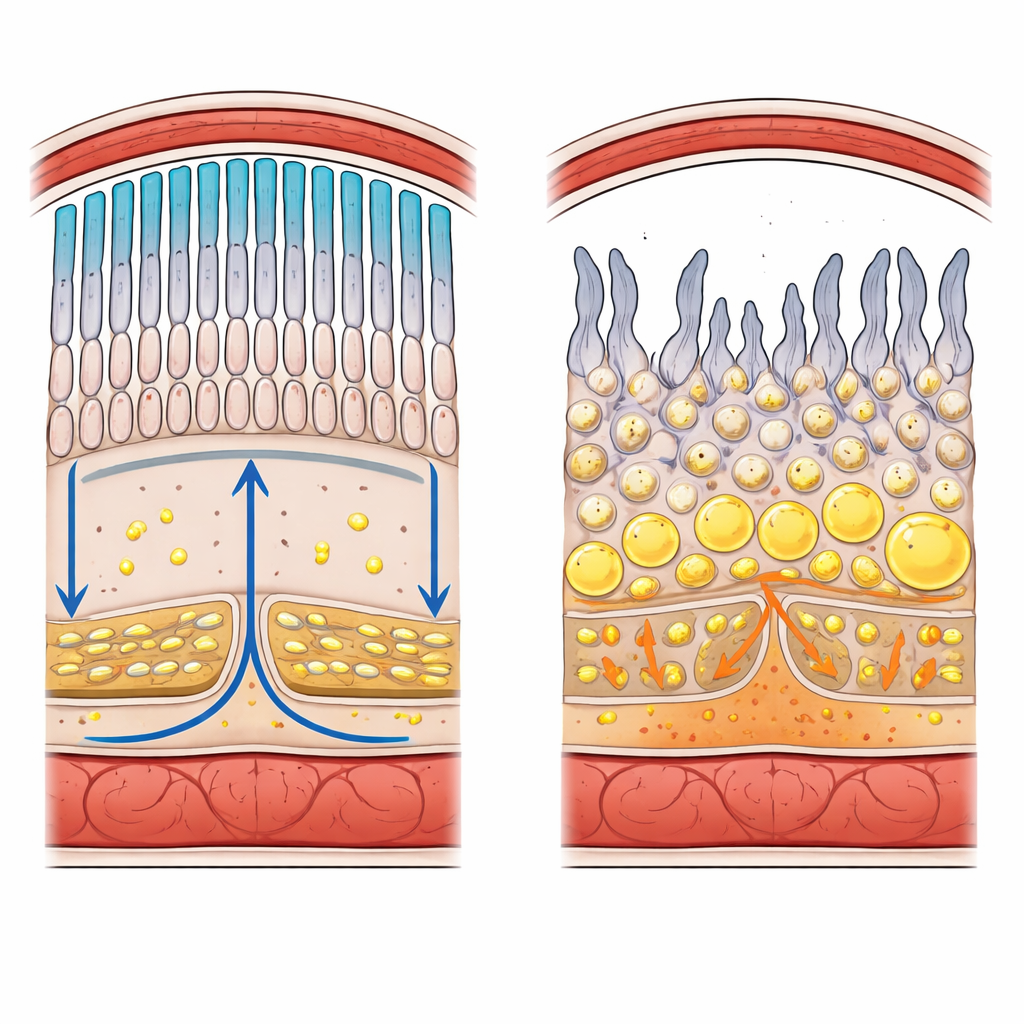
Hoe de achterkant van het oog is opgebouwd
Het netvlies is een gelaagd vel zenuwcellen dat licht omzet in elektrische signalen voor de hersenen. Aan de buitenrand bevinden zich staafjes en kegeltjes, de fotoreceptoren die schemerlicht en kleur waarnemen. Direct daaronder ligt een enkele laag ondersteunende cellen, het retinale pigmentepitheel (RPE), dat rust op een dunne barrièremembraan en een netwerk van bloedvaten. Strakke verbindingen tussen de cellen vormen een bloed–netvliesbarrière die nauwkeurig regelt welke stoffen, inclusief lipiden, uit de bloedsomloop het lichtgevoelige weefsel mogen bereiken. Fotoreceptoren stoten ongeveer 10% van hun membraan per dag af en bouwen het opnieuw op, wat een enorme vraag naar verse fosfolipiden, cholesterol en speciale omega-3 vetten creëert.
Het recyclen van licht naar zicht
Elke keer dat een foton het oog raakt, verandert een vitamine A–gebaseerd molecuul in de fotoreceptoren van vorm, wat het visuele signaal activeert. Om het zicht gaande te houden moet dit molecuul worden gerecycled in een kringloop die bekendstaat als de visuele cyclus. Na activering reist het van de fotoreceptor naar het RPE, waar enzymen het terug omzetten in de lichtgevoelige vorm. Onderweg wordt het tijdelijk opgeslagen in kleine vetgevulde druppeltjes die retinosomen worden genoemd. Deze druppeltjes fungeren als veilige opslagplaatsen voor vitamine A-esters en andere neutrale lipiden, en voorkomen de ophoping van toxische bijproducten. Gespecialiseerde eiwitten helpen deze druppeltjes op te bouwen, te laten groeien en af te breken zodat altijd de juiste hoeveelheid visueel pigment beschikbaar is.
Het balanceren van lipideverkeer tussen steuncellen en sensoren
Het RPE is een druk logistiek knooppunt voor vetten. Vanaf de bloedzijde neemt het lipoproteïnepartikels op die cholesterol en andere lipiden transporteren en leidt die naar opslagdruppels of naar de fotoreceptoren. Vanaf de retinazijde consumeert het de afgestoten topjes van de buitenste segmenten van fotoreceptoren, verteert hun membranen en recyclet de componentlipiden. Een netwerk van membraantransporters en receptoren regelt dit tweerichtingsverkeer, inclusief eiwitten die voedingsvetten importeren zoals het omega‑3 docosahexaeenzuur (DHA) en anderen die cholesterol naar buiten pompen. Wanneer deze systemen falen—door erfelijke genmutaties of verworven metabole stress—kunnen lipiden zich op de verkeerde plaatsen ophopen, ontsteking en oxidatieve schade uitlokken en geleidelijk retinale cellen doden.
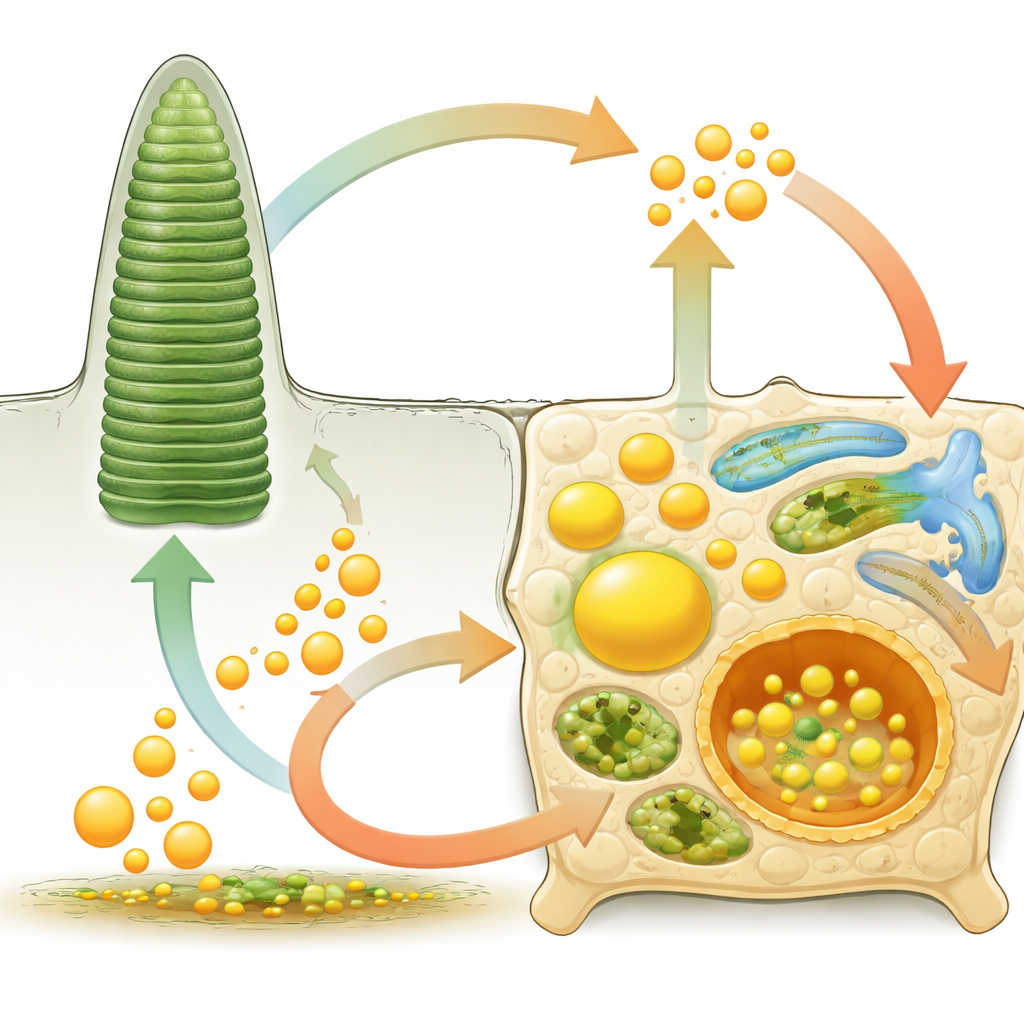
Wanneer lipidecontrole faalt: van zeldzame syndromen tot veelvoorkomende blindheid
Veel netvliesaandoeningen zijn (ten minste deels) terug te voeren op verstoord lipidebeheer. Bij de ziekte van Stargardt kan een defecte transporter in fotoreceptoren een toxisch vitamine A-bijproduct niet afvoeren, wat leidt tot ophoping van lipofuscine, een schadelijk vetpigment in RPE-cellen, en verlies van het centraal gezichtsvermogen. Mutaties in lipide-verwerkende enzymen of peroxisomen verstoren zeer lange-keten vetzuren en kunnen vroege degeneratie veroorzaken. Bij retinitis pigmentosa maken veranderingen in genen voor visuele pigmenten, lipoproteïne-assemblage of omega‑3-metabolisme fotoreceptoren structureel kwetsbaar en arm aan belangrijke vetzuren zoals DHA. Bij diabetische retinopathie en leeftijdsgebonden maculadegeneratie dragen chronisch hoge bloedsuiker, cholesterolonevenwichtigheid en inflammatoire lipiden bij aan lekkende of abnormale bloedvaten, verdikte steunmembranen en vetafzettingen onder het RPE die bekendstaan als drusen.
Nieuwe manieren om gezichtsvermogen te beschermen via lipiden
Aangezien lipidenonevenwicht een rode draad vormt in veel oogaandoeningen, is het een veelbelovende therapeutische target geworden. Geneesmiddelen die kernreceptoren zoals PPARα en liver X receptor activeren, kunnen cholesterol-efflux verhogen, ontsteking temperen en schadelijke vaatgroei beperken in modellen van diabetische en leeftijdsgebonden ziekte. Fenofibraat, een middel dat triglyceriden verlaagt, heeft in grote onderzoeken al aangetoond de voortgang van diabetische retinopathie te vertragen. Andere benaderingen proberen toxische sphingolipiden zoals ceramiden te normaliseren, beschermende omega‑3 en zeer lange-keten vetzuren aan te vullen, of statines en verwante middelen te gebruiken om cholesterolbeheer fijn af te stemmen. Parallel daaraan worden RPE-vellen en retinaweefsel afgeleid van stamcellen getest om reeds verloren cellen te vervangen. Gezamenlijk wijzen deze strategieën erop dat het behouden of herstellen van een gezonde lipidenhomeostase het gezichtsvermogen kan behouden bij een breed spectrum van erfelijke en verworven netvliesstoornissen.
Wat dit betekent voor patiënten en preventie
Vanuit afstand gezien is de boodschap van dit overzicht helder: het vermogen van het netvlies om te zien hangt af van een fragiele balans van vetten. Wanneer die balans verstoord raakt—door genen, veroudering, diabetes of slechte systemische lipidecontrole—verliest het oog langzaam het vermogen zijn lichtgevoelige cellen te vernieuwen en te beschermen. Door de sleutelroutes te begrijpen die lipiden in het netvlies verplaatsen, opslaan en ontgiften, ontdekken onderzoekers nieuwe manieren om risico’s te voorspellen, eerder in te grijpen en therapieën te ontwerpen die het natuurlijke huishoudsysteem van het oog ondersteunen. Voor patiënten wijst dit niet alleen op toekomstige gen- en celtherapieën, maar ook op praktische maatregelen vandaag—zoals het beheersen van bloedsuiker en cholesterol en het innemen van beschermende vetzuren—die kunnen helpen het netvlies langer gezonder te houden.
Bronvermelding: Bhattacharyya, A., Choudhary, V. Lipid homeostasis plays a critical role in inherited and acquired retinal diseases. Commun Biol 9, 536 (2026). https://doi.org/10.1038/s42003-026-10025-1
Trefwoorden: retinale lipiden, leeftijdsgebonden maculadegeneratie, diabetische retinopathie, retinitis pigmentosa, omega-3 vetzuren