Clear Sky Science · de
Die Lipid-Homöostase spielt eine entscheidende Rolle bei erblichen und erworbenen Netzhauterkrankungen
Warum Fette im Auge wichtig sind
Die lichtempfindlichen Zellen im hinteren Teil des Auges gehören zu den energiehungrigsten Zellen des Körpers und bauen ständig ihre äußere Oberfläche neu auf, damit wir scharf sehen können. Dafür benötigen sie eine stetige, gut kontrollierte Versorgung mit Fetten und verwandten Molekülen. Dieser Übersichtsartikel erklärt, wie diese „Fettwirtschaft" der Netzhaut normalerweise funktioniert, was passiert, wenn sie aus dem Gleichgewicht gerät, und wie dieser Zusammenbruch zu häufigen erblindenden Erkrankungen wie Retinitis pigmentosa, diabetischer Retinopathie und altersbedingter Makuladegeneration beiträgt. Er beleuchtet auch aufkommende Behandlungen, die darauf abzielen, das Sehvermögen durch Wiederherstellung eines gesunden Lipidgleichgewichts zu schützen.
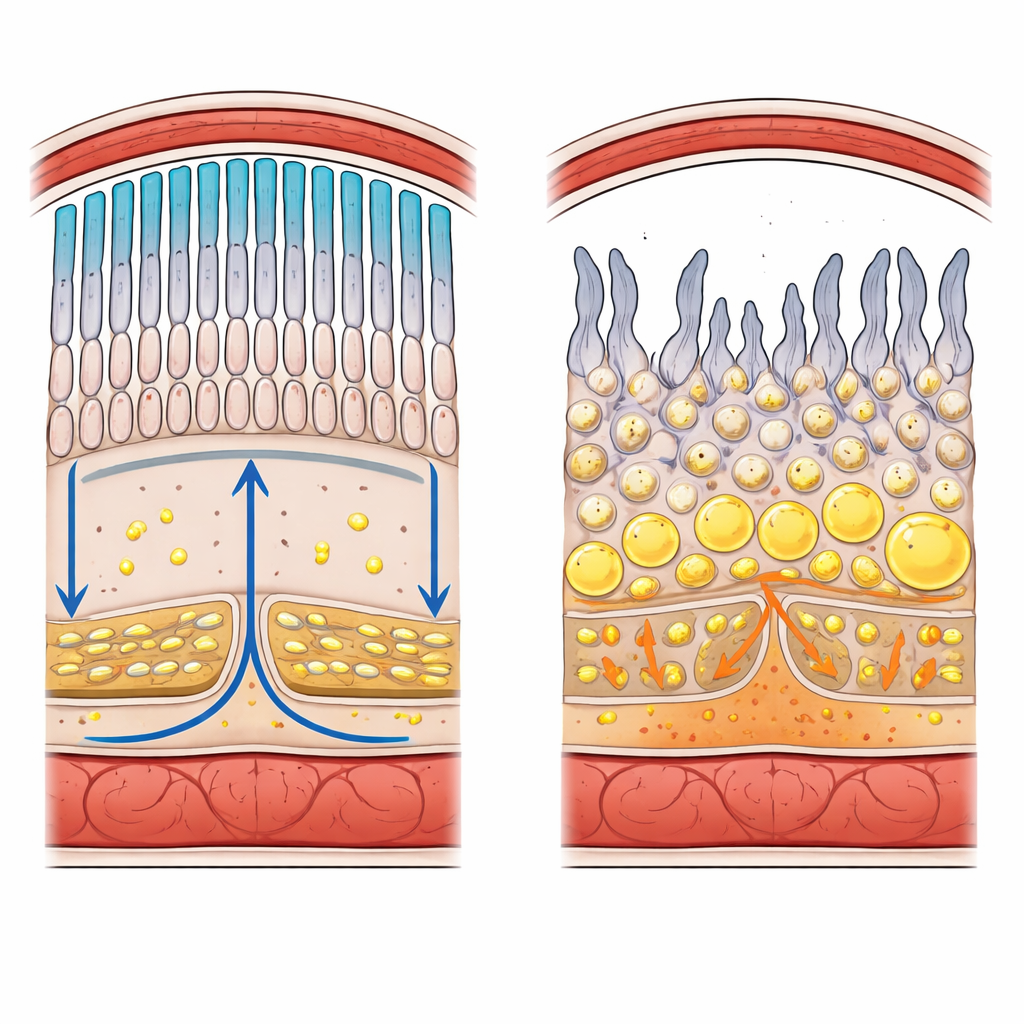
Wie der hintere Teil des Auges aufgebaut ist
Die Netzhaut ist ein geschichtetes Blatt aus Nervenzellen, das Licht in elektrische Signale für das Gehirn umwandelt. Am äußeren Rand sitzen Stäbchen und Zapfen, die Photorezeptoren, die schwaches Licht und Farbe detektieren. Direkt darunter liegt eine einzelne Lage von Stützzellen, das retinal pigment epithelium (RPE), die auf einer dünnen Barrieremembran und einem Gefäßbett ruht. Dichte Zellkontakte bilden eine Blut–Retina-Schranke, die genau steuert, welche Stoffe, einschließlich Lipiden, aus dem Kreislauf in das lichtempfindliche Gewebe gelangen können. Photorezeptoren stoßen täglich etwa 10 % ihrer Membran ab und bauen sie wieder auf, wodurch ein enormer Bedarf an frischen Phospholipiden, Cholesterin und speziellen Omega-3-Fetten entsteht.
Wie Licht in Sehen recycelt wird
Jedes Mal, wenn ein Photon auf das Auge trifft, ändert ein vitamin‑A‑basiertes Molekül in den Photorezeptoren seine Form und löst das visuelle Signal aus. Damit das Sehen erhalten bleibt, muss dieses Molekül in einer Schleife recycelt werden, die als visueller Zyklus bekannt ist. Nach der Aktivierung wandert es vom Photorezeptor zum RPE, wo Enzyme es wieder in seine lichtempfindliche Form umwandeln. Unterwegs wird es vorübergehend in winzigen, mit Fett gefüllten Tröpfchen gespeichert, den Retinosomen. Diese Tröpfchen fungieren als sichere Lagerstätten für Vitamin‑A‑Ester und andere neutrale Lipide und verhindern die Anhäufung toxischer Nebenprodukte. Spezialisierte Proteine helfen beim Aufbau, Wachstum und Abbau dieser Tröpfchen, sodass immer die richtige Menge an visuellen Pigmenten verfügbar ist.
Das Gleichgewicht des Lipidverkehrs zwischen Stützzellen und Sensoren
Das RPE ist ein geschäftiger Logistikhub für Fette. Von der Blutseite nimmt es Lipoproteinpartikel auf, die Cholesterin und andere Lipide transportieren, und leitet sie in Speicherdroplets oder weiter zu den Photorezeptoren. Von der retinalen Seite phagozytiert es die abgestoßenen Spitzen der äußeren Photorezeptorsegmente, verdaut deren Membranen und recycelt die enthaltenen Lipide. Ein Netzwerk aus Membrantransportern und Rezeptoren steuert diesen bidirektionalen Verkehr, darunter Proteine, die diätetische Fette wie die Omega‑3‑Docosahexaensäure (DHA) importieren, und andere, die Cholesterin hinauspumpen. Versagen diese Systeme – sei es durch vererbte Genmutationen oder erworbenen metabolischen Stress – können Lipide an den falschen Stellen akkumulieren, Entzündungen und oxidative Schäden auslösen und nach und nach Netzhautzellen abtöten.
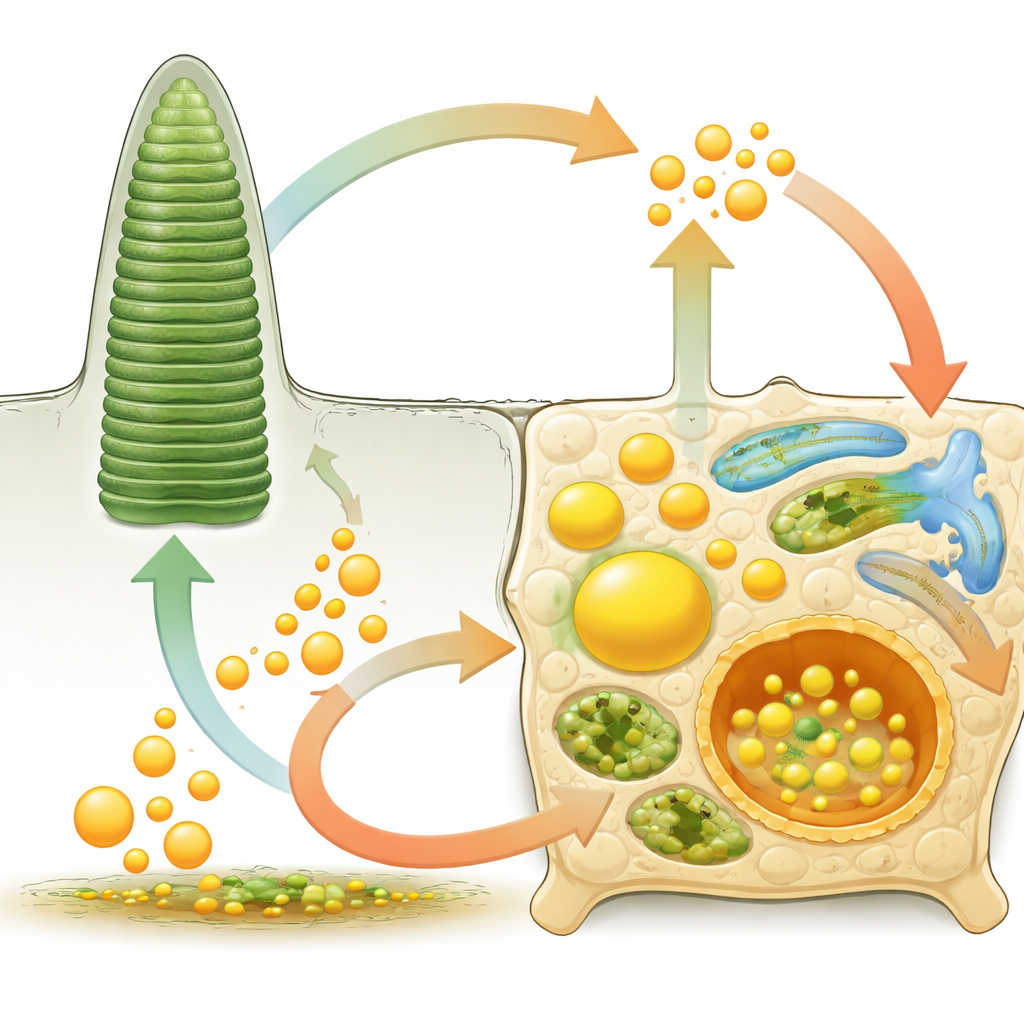
Wenn die Lipidkontrolle versagt: Von seltenen Syndromen bis zur häufigen Erblindung
Viele Netzhauterkrankungen lassen sich zumindest teilweise auf gestörtes Lipidmanagement zurückführen. Bei der Stargardt‑Krankheit kann ein fehlerhafter Transporter in den Photorezeptoren ein toxisches Vitamin‑A‑Nebenprodukt nicht ausschleusen, was zur Ansammlung von Lipofuszin führt – einem schädlichen Fettpigment in RPE‑Zellen – und zum Verlust des zentralen Sehens. Mutationen in lipidverarbeitenden Enzymen oder Peroxisomen stören sehr langkettige Fettsäuren und können früh einsetzende Degenerationen verursachen. Bei Retinitis pigmentosa machen Veränderungen in Genen für visuelle Pigmente, Lipoproteinaufbau oder Omega‑3‑Stoffwechsel die Photorezeptoren strukturell fragil und arm an wichtigen Fettsäuren wie DHA. Bei diabetischer Retinopathie und altersbedingter Makuladegeneration tragen chronisch hoher Blutzucker, Cholesterinungleichgewicht und entzündungsfördernde Lipide zu undichten oder abnormalen Blutgefäßen, verdickten Stützmembranen und fetthaltigen Ablagerungen unter dem RPE bei, den sogenannten Drusen.
Neue Wege, das Sehvermögen über Lipide zu schützen
Weil Lipidungleichgewicht bei so vielen Augenerkrankungen eine Rolle spielt, ist es zu einem vielversprechenden therapeutischen Ziel geworden. Wirkstoffe, die nukleare Rezeptoren wie PPARα und den liver X receptor aktivieren, können den Cholesterinabfluss steigern, Entzündungen dämpfen und das schädliche Gefäßwachstum in Modellen diabetischer und altersbedingter Erkrankungen begrenzen. Fenofibrat, ein triglyceridsenkendes Medikament, hat in großen Studien bereits gezeigt, dass es die diabetische Retinopathie verlangsamen kann. Weitere Ansätze zielen darauf ab, toxische Sphingolipide wie Ceramide zu normalisieren, schützende Omega‑3‑ und sehr langkettige Fettsäuren zu ergänzen oder Statine und verwandte Wirkstoffe zur Feinabstimmung des Cholesterinmanagements zu nutzen. Parallel dazu werden aus Stammzellen gewonnene RPE‑Schichten und Netzhautgewebe getestet, um bereits verlorene Zellen zu ersetzen. Zusammengenommen deuten diese Strategien darauf hin, dass die Erhaltung oder Wiederherstellung einer gesunden Lipid‑Homöostase das Sehvermögen bei einem breiten Spektrum erblich bedingter und erworbener Netzhauterkrankungen bewahren könnte.
Was das für Patienten und Prävention bedeutet
Aus der Vogelperspektive ist die Botschaft dieser Übersichtsarbeit klar: Die Fähigkeit der Netzhaut zu sehen hängt von einem empfindlichen Gleichgewicht der Fette ab. Wird dieses Gleichgewicht gestört – durch Gene, Alter, Diabetes oder eine schlechte systemische Lipidkontrolle – verliert das Auge langsam die Fähigkeit, seine lichtempfindlichen Zellen zu erneuern und zu schützen. Durch das Verständnis der Schlüsselpfade, die Lipide in der Netzhaut bewegen, speichern und entgiften, entdecken Forscher neue Wege, Risiken vorherzusagen, früher einzugreifen und Therapien zu entwickeln, die die natürlichen Haushaltsmechanismen des Auges unterstützen. Für Patienten verweist dies nicht nur auf künftige Gen‑ und Zelltherapien, sondern auch auf praktische Maßnahmen heute – wie die Kontrolle von Blutzucker und Cholesterin sowie die Aufnahme schützender Fettsäuren –, die dazu beitragen können, die Netzhaut länger gesund zu erhalten.
Zitation: Bhattacharyya, A., Choudhary, V. Lipid homeostasis plays a critical role in inherited and acquired retinal diseases. Commun Biol 9, 536 (2026). https://doi.org/10.1038/s42003-026-10025-1
Schlüsselwörter: retinale Lipide, altersbedingte Makuladegeneration, diabetische Retinopathie, Retinitis pigmentosa, Omega-3-Fettsäuren