Clear Sky Science · ar
يلعب اتزان الشحميات دورًا حاسمًا في أمراض الشبكية الوراثية والمكتسبة
لماذا تهمّ الدهون في العين
خلايا التقاط الضوء في قعر العين هي من بين أكثر الخلايا استهلاكًا للطاقة في الجسم، إذ تعيد باستمرار بناء سطوحها الخارجية لنتمكن من الرؤية الواضحة. وللقيام بذلك تحتاج إلى إمداد ثابت ومتحكم به من الدهون والجزيئات المرتبطة بها. يوضح هذا المقال الاستعراضي كيف يعمل «اقتصاد الدهون» في الشبكية عادةً، ما الذي يحدث عندما يخرج عن توازنه، وكيف يسهم هذا الانهيار في أمراض تسبب العمى مثل التهاب الشبكية الصباغي، واعتلال الشبكية السكري، والضمور البقعي المرتبط بالعمر. كما يستعرض العلاجات الناشئة التي تهدف إلى حماية البصر عن طريق استعادة توازن الشحميات الصحي.
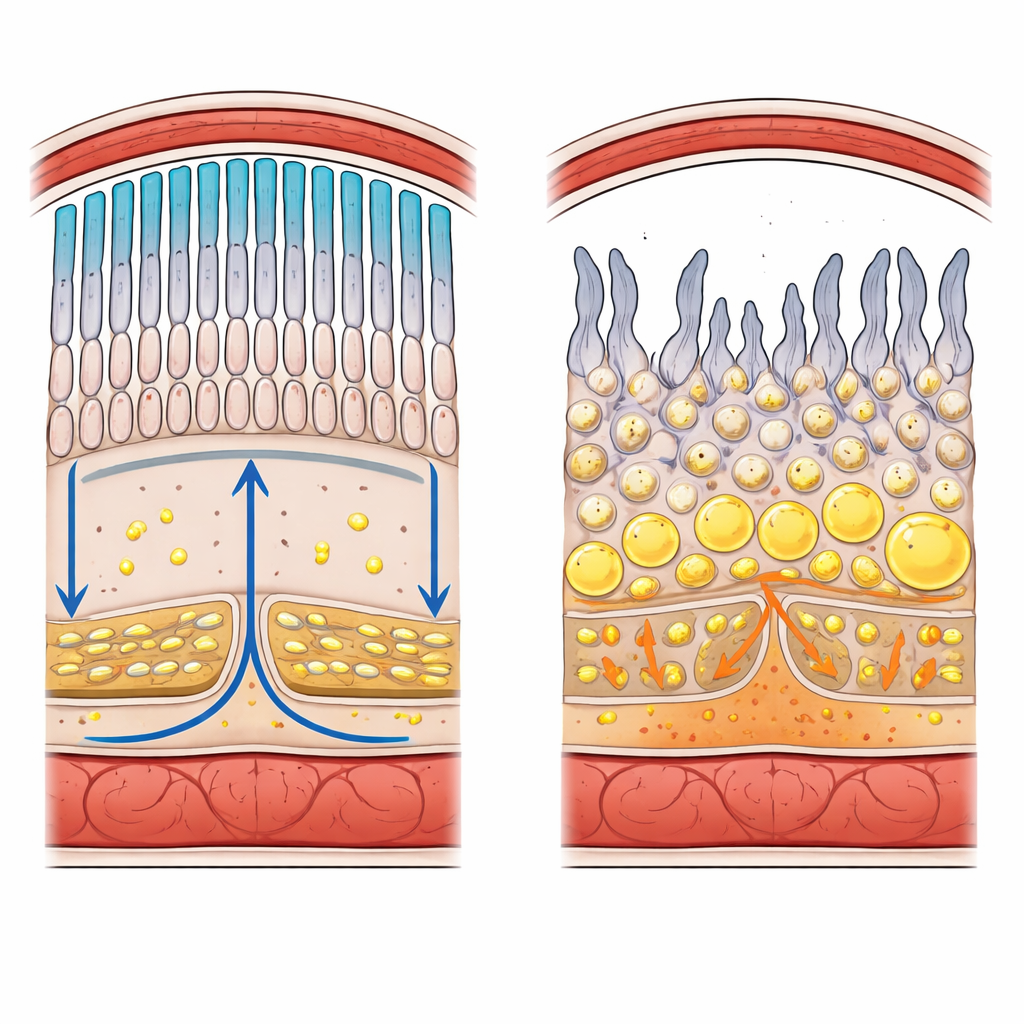
كيف تُبنى الجهة الخلفية من العين
الشبكية عبارة عن صفائح متعددة من الخلايا العصبية تحول الضوء إلى إشارات كهربائية إلى الدماغ. على حافتها الخارجية توجد العصي والمخاريط، الخلايا الضوئية التي تكشف الضوء الخافت والألوان. أسفلها مباشرة توجد طبقة واحدة من خلايا الدعم تُسمى طبقة صباغ الشبكية (RPE)، ترتكز على غشاء حاجز رقيق وطبقة من الأوعية الدموية. تشكل وصلات محكمة بين الخلايا حاجز دم–شبكية يتحكم بعناية فيما يمكن أن ينتقل من الدورة الدموية إلى النسيج الحساس للضوء، بما في ذلك الشحميات. تتخلى الخلايا الضوئية عن نحو 10% من غشائها كل يوم وتعيد بنائه، مما يخلق طلبًا هائلًا على الفسفوليبيدات والكوليسترول والدهون الخاصة من نوع أوميغا-3.
إعادة تدوير الضوء إلى رؤية
في كل مرة يصطدم فوتون بالعين، يتغير شكل جزيء معتمد على فيتامين A في الخلايا الضوئية، مما يطلق الإشارة البصرية. للمحافظة على الرؤية يجب إعادة تدوير هذا الجزيء ضمن حلقة تعرف بالدورة البصرية. بعد تنشيطه ينتقل من الخلية الضوئية إلى طبقة RPE حيث تحول الإنزيمات إياه مرة أخرى إلى شكله الحساس للضوء. على طول الطريق يُخزّن مؤقتًا في قطرات صغيرة مملوءة بالدهون تُسمى الريتينوزومات. تعمل هذه القطرات كمخازن آمنة لإسترات فيتامين A وغيرها من الشحميات المحايدة، مما يمنع تراكم نواتج سامة. تساعد بروتينات متخصصة على بناء وتكبير وتحلل هذه القطرات بحيث تتوفر دائمًا كمية مناسبة من الصبغة البصرية.
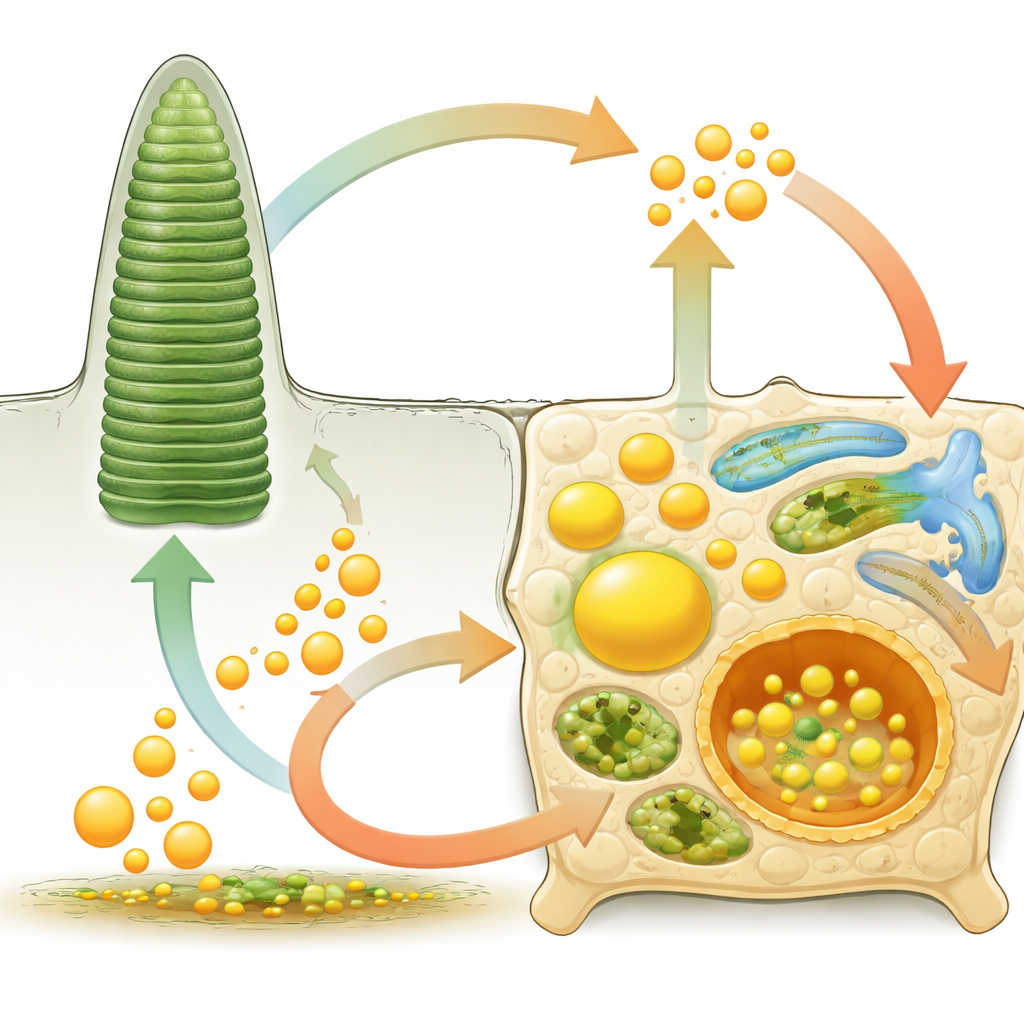
موازنة حركة الشحميات بين خلايا الدعم والمستشعرات
تعد طبقة RPE مركزًا لوجستيًا نشطًا للدهون. من جهة الدم، تمتص جزيئات الشحميات الحاملة للكوليسترول وغيرها وتوجهها إلى قطرات التخزين أو ترسلها نحو الخلايا الضوئية. من جهة الشبكية، تبتلع أطراف مقصّات الخلايا الضوئية المتخلفة، تهضم أغشيتها، وتعيد تدوير الشحميات المكونة لها. تتحكم شبكة من ناقلات وغشائية ومستقبِلات البروتين في هذه الحركة ثنائية الاتجاه، بما في ذلك بروتينات تستورد الدهون الغذائية مثل حمض الدوكوساهكسانويك (DHA) من أوميغا‑3 وأخرى تضخ الكوليسترول للخارج. عندما تفشل هذه الأنظمة—بسبب طفرات جينية موروثة أو إجهاد أيضي مكتسب—قد تتراكم الشحميات في أماكن خاطئة، فتثير التهابًا وتأكسدًا وتدمر الخلايا الشبكية تدريجيًا.
عندما يفشل ضبط الشحميات: من المتلازمات النادرة إلى العمى الشائع
ترجع العديد من أمراض الشبكية جزئيًا على الأقل إلى اضطراب في معالجة الشحميات. في مرض ستارغارت، يعجز ناقل معيب في الخلايا الضوئية عن إزالة ناتج سام من فيتامين A، مما يؤدي إلى تراكم الليبوفوسين، صبغة دهنية ضارة في خلايا RPE، وفقدان الرؤية المركزية. تؤدي طفرات في إنزيمات معالجة الشحميات أو في البيروكسيسومات إلى اضطراب الأحماض الدهنية شديدة الطول وقد تسبب ضمورًا يبدأ مبكرًا. في التهاب الشبكية الصباغي، تترك تغييرات في جينات الصبغات البصرية أو تركيب البروتينات الحاملة للشحميات أو أيض أوميغا‑3 الخلايا الضوئية هشة هيكليًا وفقيرةً في الأحماض الدهنية الحيوية مثل DHA. في اعتلال الشبكية السكري والضمور البقعي المرتبط بالعمر، يساهم ارتفاع السكر المزمن في الدم، واضطراب توازن الكوليسترول، والشحميات الالتهابية في تسرب الأوعية أو تشوهها، وتثخن الأغشية الداعمة، وترسبات دهنية تحت RPE تعرف بالدرسين.
سبل جديدة لحماية الرؤية عبر الشحميات
بما أن اختلال الشحميات يمر عبر مسارات العديد من أمراض العين، فقد أصبح هدفًا علاجيًا واعدًا. يمكن للأدوية التي تنشط مستقبلات نووية مثل PPARα ومُستقبِل الكبد X أن تعزز تدفق الكوليسترول للخارج، وتكبح الالتهاب، وتحد من نمو الأوعية الضارة في نماذج الأمراض السكرية والمرتبطة بالعمر. أظهر الفينوفيبرات، دواء خافض للدهون الثلاثية، في تجارب واسعة أنه يبطئ تقدم اعتلال الشبكية السكري. تهدف طرق أخرى إلى تطبيع سفينجوليبيدات سامة مثل السراميد، أو تكملة الأحماض الدهنية الوقائية من نوع أوميغا‑3 والأحماض الدهنية الطويلة جدًا، أو استخدام الستاتينات وعوامل مشابهة لضبط معالجة الكوليسترول. بالتوازي، تُجرى تجارب على صفائح RPE ومختلَفات شبكية مشتقة من الخلايا الجذعية لاستبدال الخلايا المفقودة بالفعل. توحي هذه الاستراتيجيات مجتمعة بأن الحفاظ على توازن شحميات صحي أو استعادته قد يحفظ البصر عبر طيف واسع من اضطرابات الشبكية الوراثية والمكتسبة.
ماذا يعني هذا للمرضى والوقاية
من زاويةٍ بعيدة، الرسالة الرئيسية لهذا الاستعراضي بسيطة: قدرة الشبكية على الرؤية تعتمد على توازن دقيق للدهون. عندما يختل هذا التوازن—بسبب الجينات أو الشيخوخة أو السكري أو ضعف التحكم في شحميات الجسم—تفقد العين تدريجيًا قدرتها على تجديد وحماية خلاياها الحساسة للضوء. من خلال فهم المسارات الرئيسية التي تنقل وتخزن وتزيل السموم الناتجة عن الشحميات في الشبكية، يكشف الباحثون عن طرق جديدة للتنبؤ بالمخاطر، والتدخل مبكرًا، وتصميم علاجات تدعم آليات التنظيف الطبيعي في العين. بالنسبة للمرضى، يشير ذلك ليس فقط إلى علاجات جينية وخلوية مستقبلية، بل أيضًا إلى إجراءات عملية اليوم—مثل ضبط سكر الدم والكوليسترول وتناول الأحماض الدهنية الوقائية—التي قد تساعد في الحفاظ على صحة الشبكية لفترة أطول.
الاستشهاد: Bhattacharyya, A., Choudhary, V. Lipid homeostasis plays a critical role in inherited and acquired retinal diseases. Commun Biol 9, 536 (2026). https://doi.org/10.1038/s42003-026-10025-1
الكلمات المفتاحية: دهون شبكية, الضمور البقعي المرتبط بالعمر, اعتلال الشبكية السكري, التهاب الشبكية الصباغي, أحماض أوميغا-3 الدهنية