Clear Sky Science · fr
L’homéostasie des lipides joue un rôle critique dans les maladies rétiniennes héritées et acquises
Pourquoi les graisses de l’œil comptent
Les cellules photoréceptrices au fond de l’œil figurent parmi les cellules les plus gourmandes en énergie de l’organisme ; elles reconstruisent en permanence leur surface externe pour que la vision reste nette. Pour ce faire, elles ont besoin d’un apport régulier et strictement régulé de graisses et de molécules apparentées. Cet article de synthèse explique comment fonctionne normalement cette « économie lipidique » de la rétine, ce qui se produit lorsqu’elle se dérègle, et comment ce déséquilibre contribue à des maladies aveuglantes courantes comme la rétinite pigmentaire, la rétinopathie diabétique et la dégénérescence maculaire liée à l’âge. Il explore également des traitements émergents visant à protéger la vision en restaurant un équilibre lipidique sain.
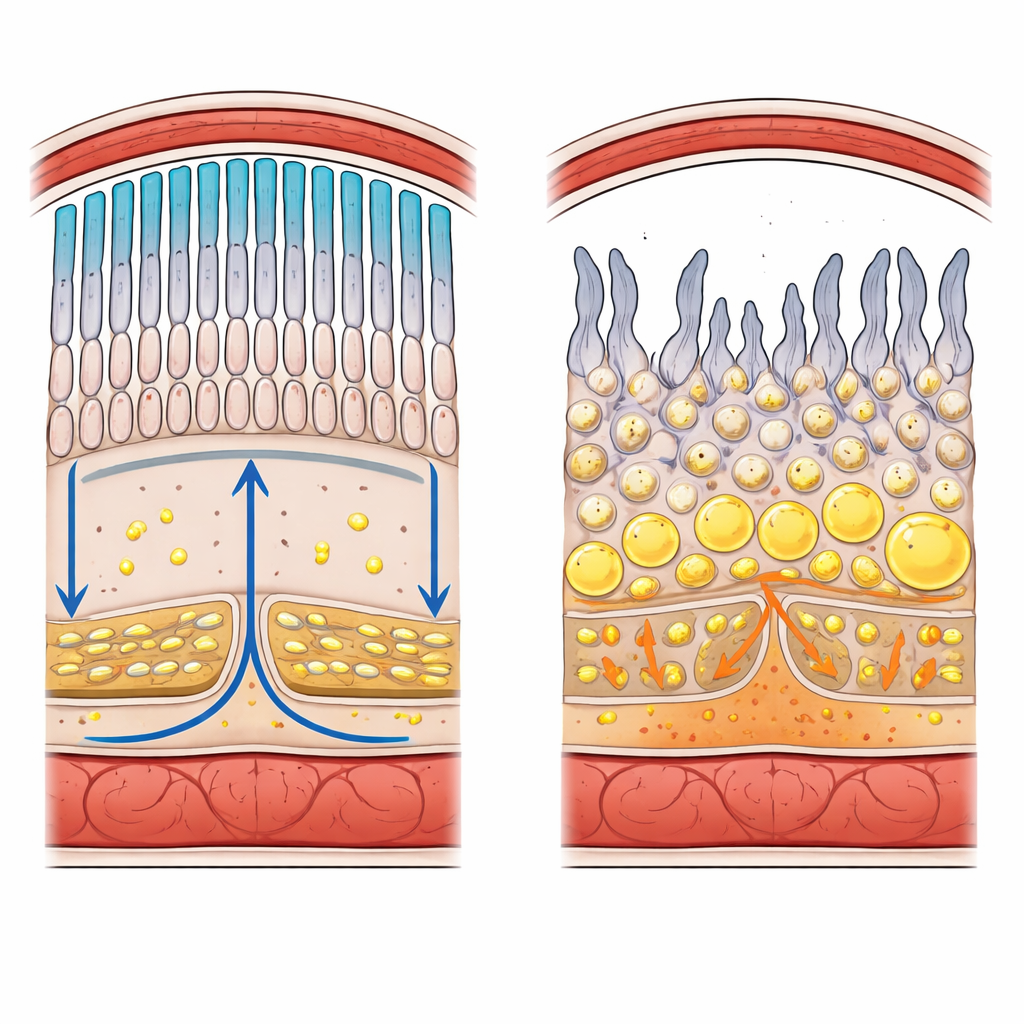
Comment est structurée la partie postérieure de l’œil
La rétine est une couche organisée de cellules nerveuses qui convertit la lumière en signaux électriques pour le cerveau. À son bord externe se trouvent les bâtonnets et les cônes, les photorécepteurs qui détectent la faible luminosité et les couleurs. Juste en dessous se trouve une seule couche de cellules de soutien appelée épithélium pigmentaire rétinien (EPR), reposant sur une membrane barrière mince et un lit de vaisseaux sanguins. Des jonctions serrées entre les cellules forment une barrière sang-rétine qui contrôle soigneusement quelles substances, y compris les lipides, peuvent passer de la circulation vers le tissu photosensible. Les photorécepteurs perdent environ 10 % de leur membrane chaque jour et la reconstruisent, créant une demande énorme en phospholipides, en cholestérol et en acides gras oméga‑3 spécialisés.
Recycler la lumière en vision
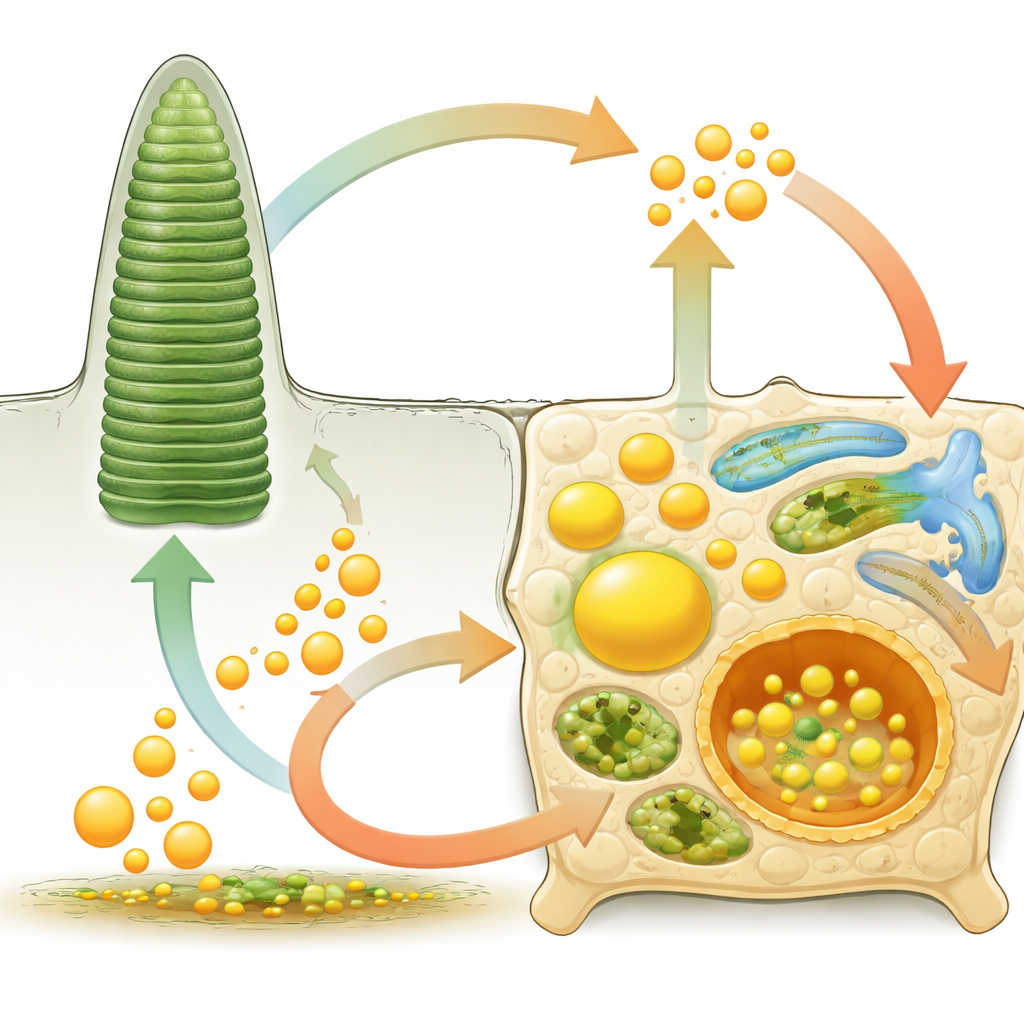
Chaque fois qu’un photon atteint l’œil, une molécule à base de vitamine A dans les photorécepteurs change de conformation, déclenchant le signal visuel. Pour que la vision continue, cette molécule doit être recyclée dans une boucle connue sous le nom de cycle visuel. Après activation, elle voyage du photorécepteur vers l’EPR, où des enzymes la reconvertissent en sa forme sensible à la lumière. En chemin, elle est stockée temporairement dans de minuscules gouttelettes remplies de lipides appelées rétinosomes. Ces gouttelettes servent d’entrepôts sûrs pour les esters de vitamine A et d’autres lipides neutres, évitant l’accumulation de sous-produits toxiques. Des protéines spécialisées participent à la formation, à la maturation et à la dégradation de ces gouttelettes afin que la quantité correcte de pigment visuel soit toujours disponible.
Équilibrer le trafic lipidique entre cellules de soutien et capteurs
L’EPR est un centre logistique actif pour les graisses. Côté sanguin, il absorbe des particules lipoprotéiques qui transportent le cholestérol et d’autres lipides et les oriente vers des gouttelettes de stockage ou vers les photorécepteurs. Côté rétinien, il phagocyte les bouts abandonnés des segments externes des photorécepteurs, digère leurs membranes et recycle les lipides composant ces membranes. Un réseau de transporteurs membranaires et de récepteurs gouverne ce trafic bilatéral, y compris des protéines qui importent des graisses alimentaires comme l’acide docosahexaénoïque (DHA) oméga‑3 et d’autres qui expulsent le cholestérol. Quand ces systèmes échouent — à cause de mutations génétiques héréditaires ou d’un stress métabolique acquis — les lipides peuvent s’accumuler au mauvais endroit, déclencher une inflammation et un dommage oxydatif, et progressivement tuer les cellules rétiniennes.
Quand le contrôle lipidique faillit : des syndromes rares à la cécité fréquente
De nombreuses maladies rétiniennes trouvent leur origine, au moins en partie, dans une altération de la gestion des lipides. Dans la maladie de Stargardt, un transporteur défectueux dans les photorécepteurs ne peut pas éliminer un sous-produit toxique de la vitamine A, entraînant l’accumulation de lipofuscine, un pigment gras nuisible dans les cellules de l’EPR, et une perte de la vision centrale. Des mutations dans des enzymes de traitement des lipides ou dans les peroxysomes perturbent les acides gras très longues chaînes et peuvent provoquer une dégénérescence d’apparition précoce. Dans la rétinite pigmentaire, des altérations des gènes codant pour les pigments visuels, l’assemblage des lipoprotéines ou le métabolisme des oméga‑3 rendent les photorécepteurs structurellement fragiles et déficients en acides gras clés comme le DHA. Dans la rétinopathie diabétique et la dégénérescence maculaire liée à l’âge, l’hyperglycémie chronique, le déséquilibre du cholestérol et les lipides inflammatoires contribuent à des vaisseaux sanguins fuyants ou anormaux, à l’épaississement des membranes de soutien et à des dépôts lipidiques sous l’EPR connus sous le nom de drusen.
Nouvelles façons de protéger la vue via les lipides
Parce que le déséquilibre lipidique est au cœur de nombreuses pathologies oculaires, il constitue une cible thérapeutique prometteuse. Des médicaments qui activent des récepteurs nucléaires tels que PPARα et le récepteur X du foie peuvent stimuler l’efflux du cholestérol, calmer l’inflammation et limiter la croissance vasculaire nocive dans des modèles de maladies diabétiques et liées à l’âge. Le fénofibrate, un médicament abaissant les triglycérides, a déjà démontré dans de grands essais qu’il ralentit la progression de la rétinopathie diabétique. D’autres approches visent à normaliser des sphingolipides toxiques comme les céramides, à supplémenter des acides gras protecteurs oméga‑3 et très longues chaînes, ou à utiliser des statines et agents apparentés pour affiner la gestion du cholestérol. Parallèlement, des feuilles d’EPR et du tissu rétinien dérivés de cellules souches sont testés pour remplacer des cellules déjà perdues. Ensemble, ces stratégies suggèrent que maintenir ou rétablir une homéostasie lipidique saine pourrait préserver la vision dans un large spectre de troubles rétiniens hérités et acquis.
Ce que cela signifie pour les patients et la prévention
Dans l’ensemble, le message de cette revue est simple : la capacité de la rétine à voir dépend d’un équilibre délicat de graisses. Lorsque cet équilibre est perturbé — par des gènes, le vieillissement, le diabète ou un mauvais contrôle systémique des lipides — l’œil perd progressivement sa capacité à renouveler et protéger ses cellules photoréceptrices. En comprenant les voies clés qui déplacent, stockent et détoxifient les lipides dans la rétine, les chercheurs mettent au jour de nouvelles façons de prédire les risques, d’intervenir plus tôt et de concevoir des thérapies qui soutiennent les systèmes naturels de maintenance de l’œil. Pour les patients, cela renvoie non seulement aux thérapies géniques et cellulaires à venir, mais aussi à des mesures pratiques aujourd’hui — telles que le contrôle de la glycémie et du cholestérol, et la consommation d’acides gras protecteurs — qui peuvent aider à maintenir leurs rétines en meilleure santé plus longtemps.
Citation: Bhattacharyya, A., Choudhary, V. Lipid homeostasis plays a critical role in inherited and acquired retinal diseases. Commun Biol 9, 536 (2026). https://doi.org/10.1038/s42003-026-10025-1
Mots-clés: lipides rétiniens, dégénérescence maculaire liée à l’âge, rétinopathie diabétique, rétinite pigmentaire, acides gras oméga-3