Clear Sky Science · it
L’omeostasi lipidica gioca un ruolo critico nelle malattie retiniche ereditarie e acquisite
Perché i grassi nell’occhio sono importanti
Le cellule sensibili alla luce nella parte posteriore dell’occhio sono tra le più affamate di energia dell’organismo, ricostruendo costantemente la loro superficie esterna per permetterci di vedere nitidamente. Per farlo hanno bisogno di un apporto stabile e ben regolato di grassi e molecole correlate. Questo articolo di revisione spiega come funziona normalmente quella “economia dei lipidi” della retina, cosa accade quando perde l’equilibrio e come questo squilibrio contribuisca a malattie dell’occhio che portano spesso alla cecità, come la retinite pigmentosa, la retinopatia diabetica e la degenerazione maculare legata all’età. Esamina inoltre terapie emergenti che mirano a proteggere la vista ripristinando un sano bilancio lipidico.
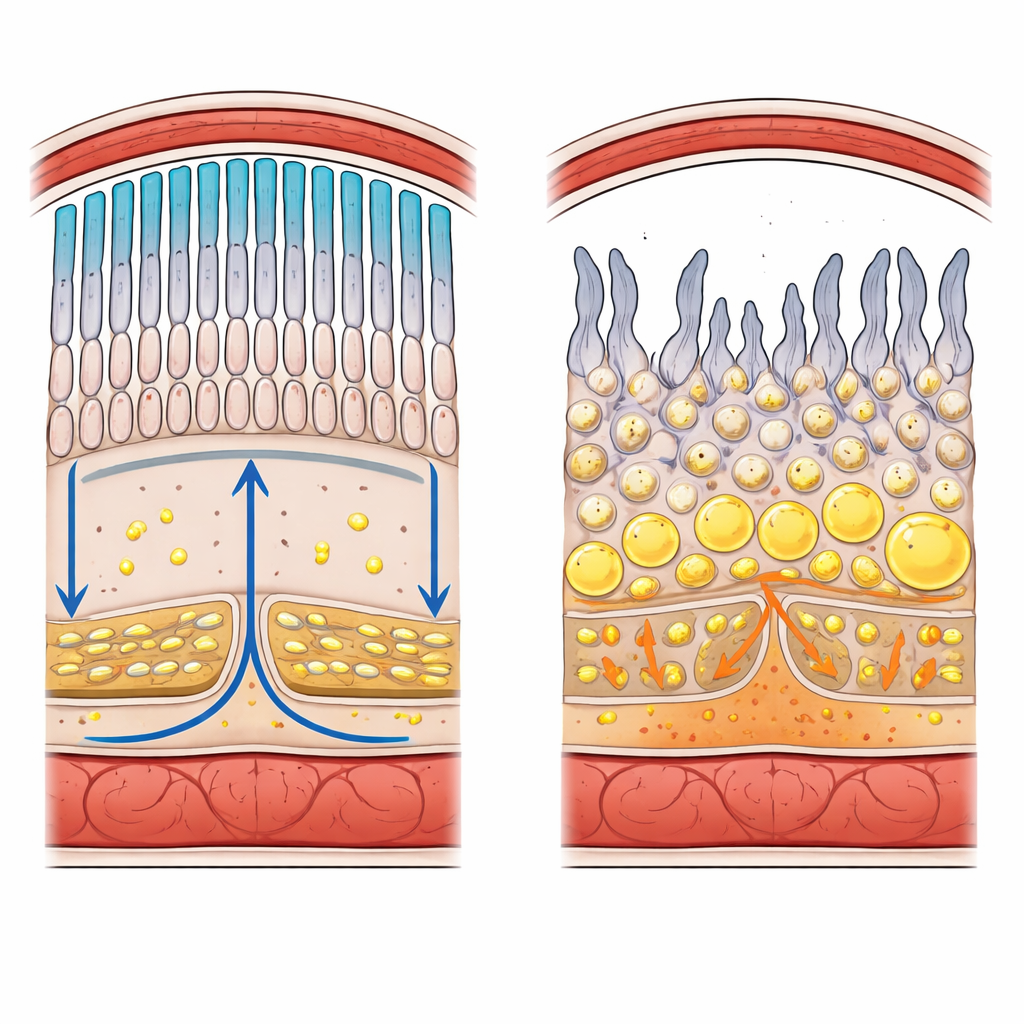
Com’è costruita la parte posteriore dell’occhio
La retina è un foglio stratificato di cellule nervose che trasforma la luce in segnali elettrici per il cervello. Al suo margine esterno si trovano bastoncelli e coni, i fotorecettori che rilevano la luce fioca e il colore. Subito sotto c’è un singolo strato di cellule di supporto chiamato epitelio pigmentato retinico (RPE), appoggiato su una membrana barriera sottile e un letto di vasi sanguigni. Giunzioni strette tra le cellule formano una barriera sangue–retina che controlla con cura quali sostanze, inclusi i lipidi, possono passare dalla circolazione al tessuto sensibile alla luce. I fotorecettori perdono circa il 10% della loro membrana ogni giorno e la ricostruiscono, creando una domanda enorme di fosfolipidi freschi, colesterolo e particolari grassi omega-3.
Riciclare la luce in visione
Ogni volta che un fotone colpisce l’occhio, una molecola a base di vitamina A nei fotorecettori cambia forma, scatenando il segnale visivo. Per mantenere la visione questa molecola deve essere riciclata in un ciclo noto come ciclo visivo. Dopo l’attivazione, viaggia dal fotorecettore all’RPE, dove enzimi la riconvertono nella sua forma sensibile alla luce. Lungo il percorso viene temporaneamente immagazzinata in minuscole goccioline piene di grasso chiamate retinosomi. Queste goccioline fungono da depositi sicuri per esteri della vitamina A e altri lipidi neutri, impedendo l’accumulo di sottoprodotti tossici. Proteine specializzate aiutano a costruire, far crescere e degradare queste goccioline in modo che la giusta quantità di pigmento visivo sia sempre disponibile.
Bilanciare il traffico lipidico tra cellule di supporto e sensori
L’RPE è un intenso centro logistico per i grassi. Dal lato sanguigno assorbe particelle lipoproteiche che trasportano colesterolo e altri lipidi, convogliandoli in goccioline di deposito o inviandoli verso i fotorecettori. Dal lato retinico fagocita le punte scartate dei segmenti esterni dei fotorecettori, digerisce le loro membrane e ricicla i lipidi componenti. Una rete di trasportatori di membrana e recettori regola questo traffico bidirezionale, compresa una serie di proteine che importano grassi dietetici come l’acido docosaesaenoico (DHA) omega‑3 e altre che pompano fuori il colesterolo. Quando questi sistemi falliscono — per mutazioni genetiche ereditarie o stress metabolico acquisito — i lipidi possono accumularsi nei posti sbagliati, scatenare infiammazione e danno ossidativo e gradualmente uccidere le cellule retiniche.
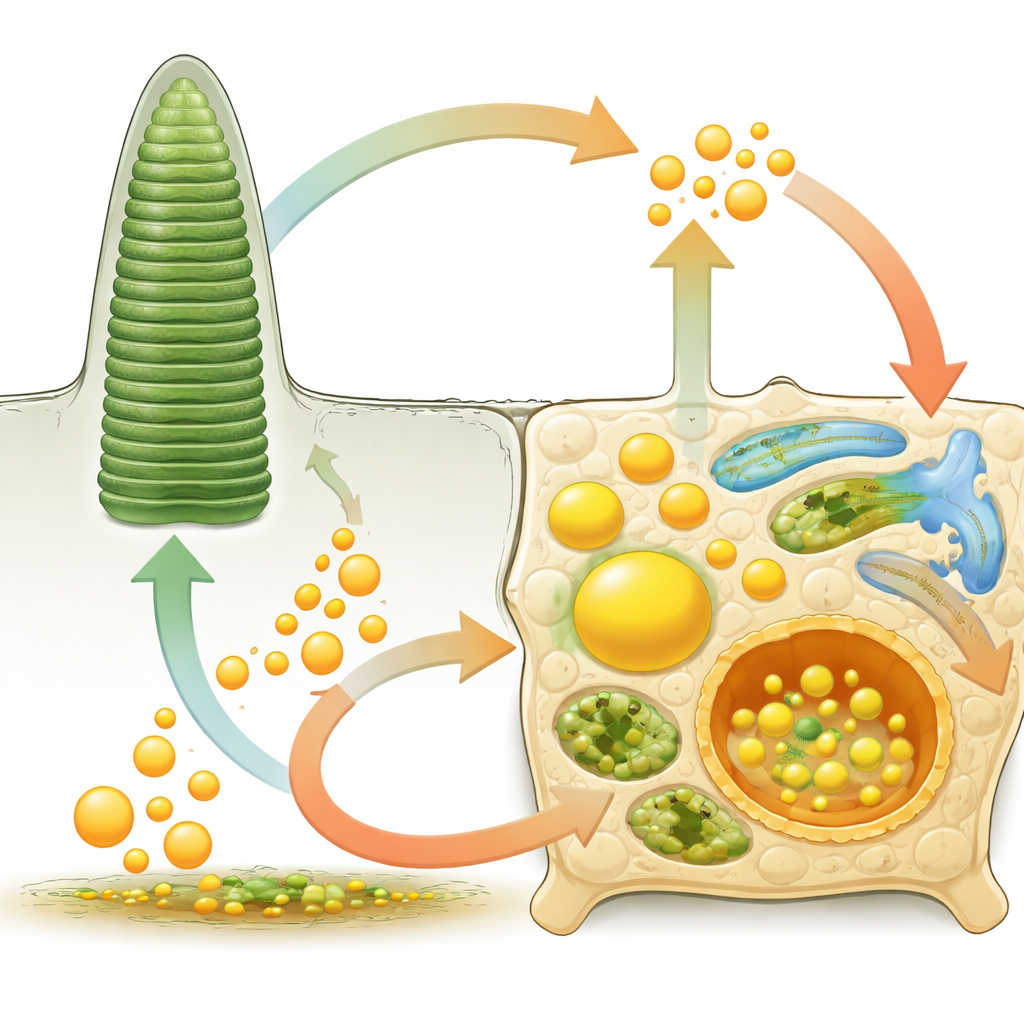
Quando il controllo lipidico fallisce: da sindromi rare a cecità comune
Molte malattie retiniche risalgono, almeno in parte, a una gestione lipidica alterata. Nella malattia di Stargardt, un trasportatore difettoso nei fotorecettori non riesce a eliminare un sottoprodotto tossico della vitamina A, causando l’accumulo di lipofuscina, un pigmento grasso dannoso nelle cellule RPE, e la perdita della visione centrale. Mutazioni in enzimi di processamento lipidico o nei perossisomi alterano gli acidi grassi a catena molto lunga e possono provocare degenerazione ad esordio precoce. Nella retinite pigmentosa, variazioni nei geni dei pigmenti visivi, nell’assemblaggio delle lipoproteine o nel metabolismo degli omega‑3 lasciano i fotorecettori strutturalmente fragili e carenti di acidi grassi chiave come il DHA. Nella retinopatia diabetica e nella degenerazione maculare legata all’età, iperglicemia cronica, squilibrio del colesterolo e lipidi infiammatori contribuiscono a vasi sanguigni che perdono o sono anomali, membrane di supporto ispessite e depositi lipidici sotto l’RPE noti come drusen.
Nuove vie per proteggere la vista tramite i lipidi
Poiché lo squilibrio lipidico attraversa molte malattie oculari, è diventato un promettente bersaglio terapeutico. Farmaci che attivano recettori nucleari come PPARα e il recettore X epatico possono aumentare l’efflusso di colesterolo, domare l’infiammazione e limitare la crescita vascolare dannosa in modelli di malattia diabetica e legata all’età. Il fenofibrato, un medicinale che abbassa i trigliceridi, ha già dimostrato in ampi studi di rallentare la retinopatia diabetica. Altri approcci mirano a normalizzare sphingolipidi tossici come i ceramidi, integrare acidi grassi protettivi omega‑3 e a catena molto lunga, o usare statine e agenti correlati per regolare il metabolismo del colesterolo. Parallelamente, fogli di RPE e tessuto retinico derivati da cellule staminali sono in sperimentazione per sostituire le cellule già perdute. Insieme, queste strategie suggeriscono che mantenere o ripristinare una sana omeostasi lipidica potrebbe preservare la vista in un ampio spettro di disturbi retinici ereditari e acquisiti.
Cosa significa questo per i pazienti e la prevenzione
Guardata nel suo insieme, la conclusione di questa revisione è chiara: la capacità della retina di vedere dipende da un delicato equilibrio di grassi. Quando tale equilibrio viene interrotto — da geni, invecchiamento, diabete o scarso controllo sistemico dei lipidi — l’occhio perde lentamente la capacità di rinnovare e proteggere le sue cellule sensibili alla luce. Comprendendo le vie chiave che muovono, immagazzinano e detossificano i lipidi nella retina, i ricercatori stanno scoprendo nuovi modi per prevedere il rischio, intervenire prima e progettare terapie che supportino i sistemi di manutenzione naturali dell’occhio. Per i pazienti ciò indica non solo future terapie geniche e cellulari, ma anche misure pratiche oggi — come controllare glicemia e colesterolo e assumere acidi grassi protettivi — che possono aiutare a mantenere la salute retinica più a lungo.
Citazione: Bhattacharyya, A., Choudhary, V. Lipid homeostasis plays a critical role in inherited and acquired retinal diseases. Commun Biol 9, 536 (2026). https://doi.org/10.1038/s42003-026-10025-1
Parole chiave: lipidi retinici, degenerazione maculare legata all’età, retinopatia diabetica, retinite pigmentosa, acidi grassi omega-3