Clear Sky Science · he
הומאוסטזת שומנים משחקת תפקיד קריטי במחלות רשתית תורשתיות ונרכשות
למה שומנים בעין חשובים
תאי החישה לאור בחלק האחורי של העין הם בין התאים הצרכניים ביותר באנרגיה בגוף, כשהם בונים מחדש באופן מתמיד את המשטח החיצוני שלהם כדי שנוכל לראות בבירור. לשם כך הם זקוקים למקור שוטף ומבוקר של שומנים ומולקולות קשורות. מאמר סקירה זה מסביר כיצד עובדת ה"כלכלת השומנים" של הרשתית במצב תקין, מה קורה כאשר היא יוצאת מאיזון, וכיצד קריסה זו תורמת למחלות עיניים עיוורוניות נפוצות כגון רטיניטיס פיגמנטוזה, רטינופתיה סוכרתית וניוון מקולרי תלוי גיל. הוא גם בוחן טיפולים מתעוררים שמטרתם להגן על הראייה על ידי שיקום איזון שומנים בריא.
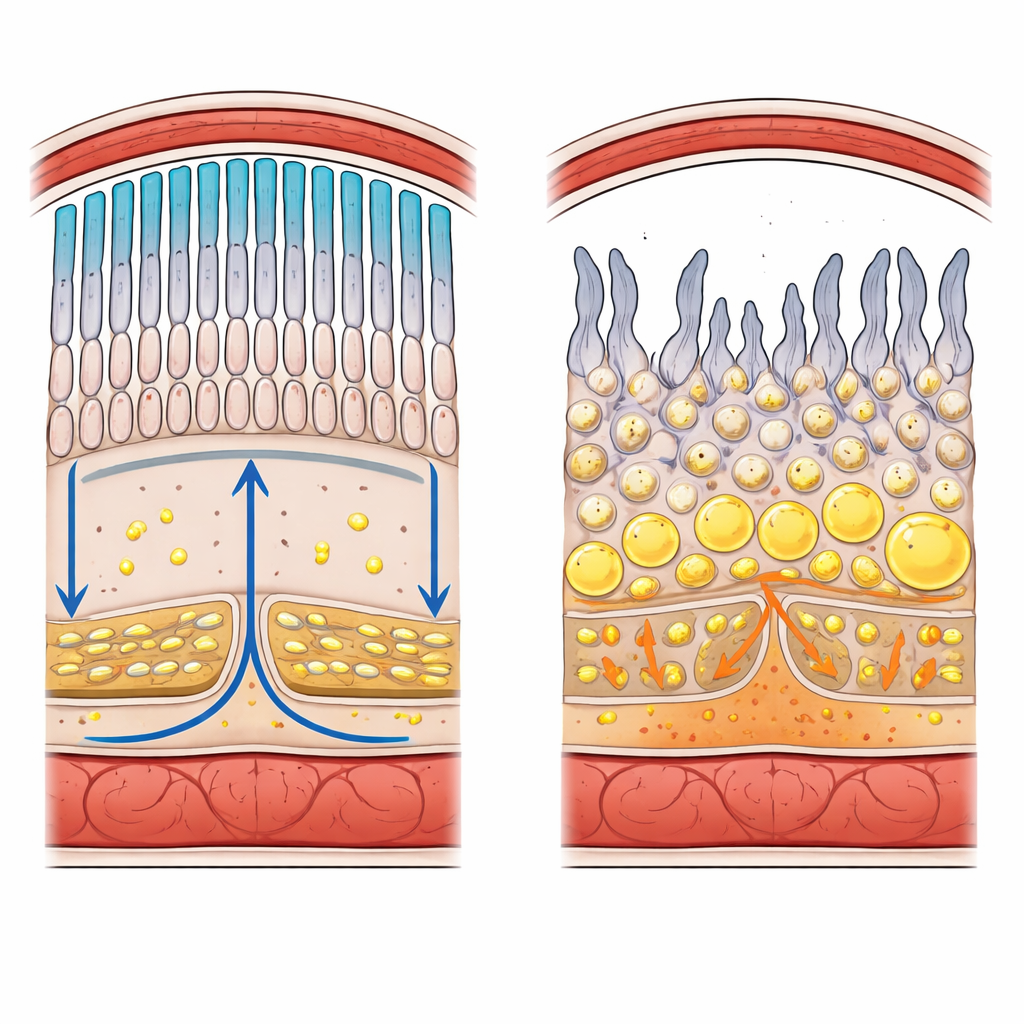
איך מבנים את החלק האחורי של העין
הרשתית היא גיליון רב־שכבתי של תאי עצב שממירים אור לאותות חשמליים המיועדים למוח. בקצוות החיצוניים שלה נמצאים מקלות וקנים, התאים הפוטורצפטורים שזיהוי אור חלש וצבעים. ממש מתחתיהם שוכב שכבה בודדת של תאי תמיכה הנקראת האפיתל הפיגמנטי של הרשתית (RPE), היושבת על ממברנה מחסום דקה ומערכת כלי דם. צמתי הדוק בין התאים יוצרים מחסום דם–רשתית השולט בקפידה אילו חומרים, כולל ליפידים, יכולים לנוע מהמחזור הדם אל הרקמה הרגישה לאור. תאי הפוטורצפטור משליכים כ־10% מממברנתם מדי יום ובונים אותה מחדש, מה שיוצר דרישה עצומה לפוספוליפידים טריים, כולסטרול ושומני אומגה‑3 מיוחדים.
ממחזרים אור לראייה
כל פעם שפוטון פוגע בעין, מולקולה מבוססת ויטמין A בתאי הפוטורצפטור משנה צורה ומפעילה את האות הוויזואלי. כדי לשמור על המשכיות הראייה, יש למחזר מולקולה זו בלולאה הנקראת מעגל הראייה. לאחר הפעלתה היא עוברת מהפוטורצפטור אל ה‑RPE, שם אנזימים ממירים אותה חזרה לצורתה הרגישה לאור. בדרך היא מאוחסנת זמנית בטיפות שמנוניות זעירות הנקראות רטינוסומים. טיפות אלה פועלות כמחסנים בטוחים לאסטרי ויטמין A ולליפידים ניטרליים אחרים, ומונעות הצטברות תוצרי לוואי רעילים. חלבונים מיוחדים מסייעים בבניית, גידול ופירוק טיפות אלה כך שתמיד תהיה כמות מתאימה של פיגמנט ויזואלי זמינה.
איזון תנועת הליפידים בין תאי תמיכה לחיישנים
ה‑RPE הוא מרכז לוגיסטי עסוק של שומנים. מצד כלי הדם הוא מושך חלקיקי ליפופרוטאין שנושאים כולסטרול וליפידים אחרים ומכוון אותם אל טיפות אחסון או שולח אותם אל תאי הפוטורצפטור. מצד הרשתית הוא בולע את קצות מקטעי החוץ שנושרים מהפוטורצפטורים, מעכל את ממברנותיהם וממוחזר את רכיבי הליפידים. רשת של נשאים וקולטנים ממברנליים מווסתת את התנועה הדו‑כיוונית הזו, כולל חלבונים המייבאים שומנים תזונתיים כגון חומצת הדוקוזהקסאאנסואיק (DHA) ואחרים שממשאבים את הוצאת הכולסטרול. כאשר מערכות אלה נכשלות—בשל מוטציות גנטיות תורשתיות או בעומס מטבולי נרכש—ליפידים עלולים להצטבר במקום הלא נכון, לעורר דלקת ונזק חמצוני, ולהמית בהדרגה תאי רשתית.
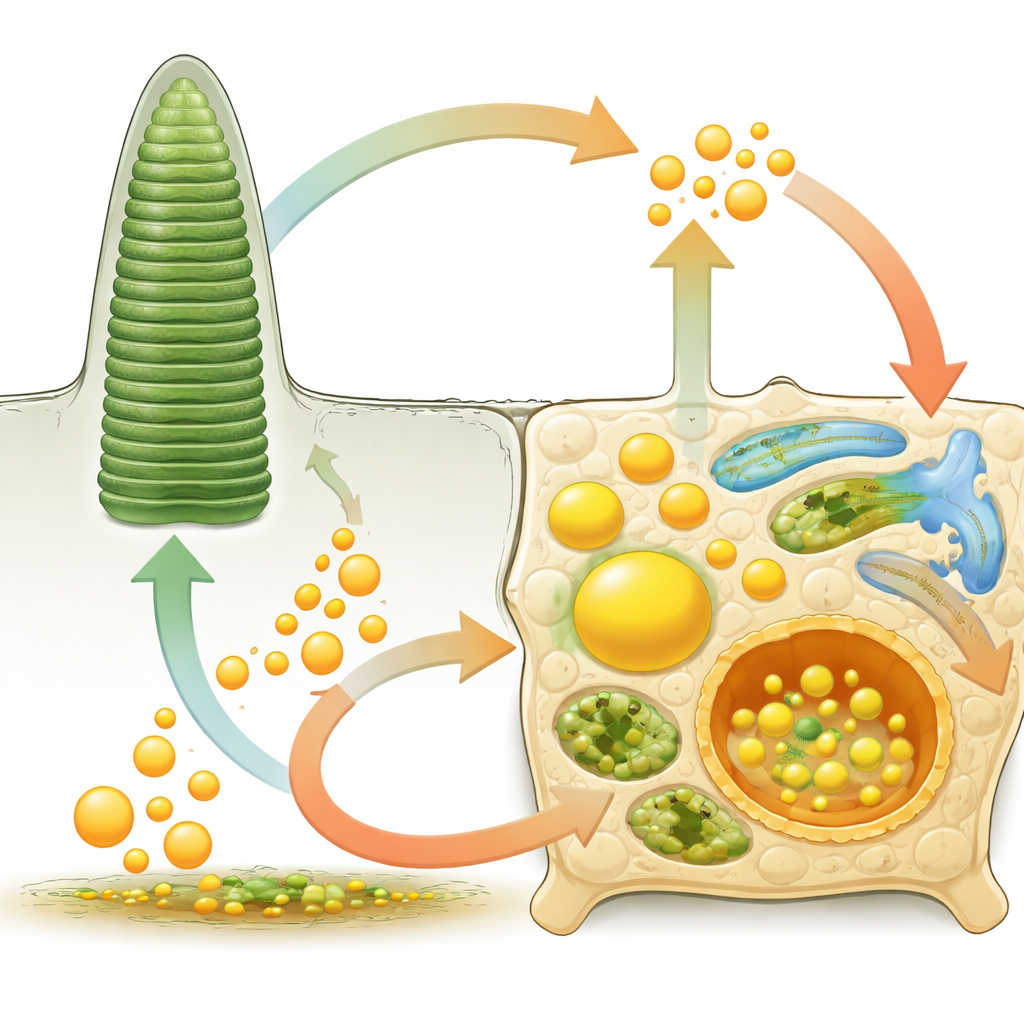
כששליטת הליפידים נכשלת: מתסמינים נדירים לעוורון שכיח
מחלות רשתית רבות נובעות, לפחות בחלקן, מהפרעות בטיפול בליפידים. במחלת סטארגטרד, נשא תקול בפוטורצפטורים אינו מסוגל לפנות תוצר לוואי רעיל של ויטמין A, מה שמוביל להצטברות של ליפופוסצין — פיגמנט שומני מזיק בתאי ה‑RPE — ואובדן הראייה המרכזית. מוטציות באנזימים המטפלים בליפידים או בפרוקיסומים מפריעות לחומצות שומן בעלות שרשרת ארוכה מאוד ועלולות לגרום לניוון מוקדם. ברטיניטיס פיגמנטוזה שינויים בגנים של פיגמנטים ויזואליים, בהרכבת ליפופרוטאינים או במטבוליזם של אומגה‑3 משאירים את הפוטורצפטורים פגיעים מבחינה מבנית ומחוסרים בחומצות שומן חשובות כמו DHA. ברטינופתיה סוכרתית ובניוון מקולרי תלוי גיל, רמות סוכר גבוהות כרוניות, חוסר איזון בכולסטרול וליפידים דלקתיים תורמים לכלי דם מדליפים או בלתי תקינים, לעיבוי ממברנות התמיכה ולהצטברויות שומניות מתחת ל‑RPE הידועות כדרוזן.
דרכים חדשות להגן על הראייה דרך שומנים
מכיוון שחוסר איזון בליפידים חוצה רבות ממחלות העין, הוא הפך למטרה טיפולית מבטיחה. תרופות המפעילות קולטנים גרעיניים כגון PPARα וקולטן X של הכבד יכולות להגביר את יצוא הכולסטרול, לרסן דלקת ולהגביל גדילה מכלילת של כלי דם במודלים של מחלה סוכרתית ותלויה גיל. פנופבראט, תרופה שמורידה טריגליצרידים, הראתה בניסויים גדולים כי היא מאיטה את התקדמות הרטינופתיה הסוכרתית. גישות נוספות מכוונות לנרמל ספינגוליפידים רעילים כמו צерамידים, להשלים חומצות שומן מגנות מסוג אומגה‑3 ושרשראות ארוכות מאוד, או להשתמש בסטטינים ובסוכנים קשורים למתן מענה למניפולציות על סילוק הכולסטרול. במקביל, גיליונות RPE ותאי רשתית שמקורם בתאי גזע נבדקים למטרת החלפת תאים שאבדו. יחד, אסטרטגיות אלה מציעות כי שמירה או שיקום הומאוסטזת שומנים בריאה עשויים לשמר ראייה בטווח רחב של הפרעות רשתית תורשתיות ונרכשות.
מה זה אומר עבור חולים ומניעה
מבט כללי על מסקנת הסקירה פשוט יחסית: יכולת הראייה של הרשתית תלויה באיזון עדין של שומנים. כאשר האיזון הזה מופר—בגלל גנים, הזדקנות, סוכרת או שליטה מערכתית לקויה ברמות שומנים—העין מאבדת בהדרגה את היכולת לחדש ולהגן על תאי החישה לאור. על ידי הבנת המסלולים המרכזיים שמזיזים, מאחסנים ומנטרלים ליפידים ברשתית, חוקרים מגלים דרכים חדשות לזהות סיכון, להתערב מוקדם יותר ולעצב טיפולים שתומכים במערכות הניקיון הטבעיות של העין. עבור החולים, הדבר מצביע לא רק על טיפולים גנטיים ותאיים עתידיים, אלא גם על צעדים מעשיים כיום—כגון ניהול רמות הסוכר והכולסטרול וצריכת חומצות שומן מגינות—שיכולים לסייע לשמור על בריאות הרשתית למשך זמן ארוך יותר.
ציטוט: Bhattacharyya, A., Choudhary, V. Lipid homeostasis plays a critical role in inherited and acquired retinal diseases. Commun Biol 9, 536 (2026). https://doi.org/10.1038/s42003-026-10025-1
מילות מפתח: שומני רשתית, ניוון מקולרי תלוי גיל, רטינופתיה סוכרתית, רטיניטיס פיגמנטוזה, חומצות שומן אומега-3