Clear Sky Science · nl
Integratieve functionele genomica-analyse identificeert pleiotrope genen voor vaatziekten
Waarom onze bloedvaten er dagelijks toe doen
Hartaanvallen, beroertes, hoge bloeddruk en verwijdingen van de hoofdslagader (aneurysma) zijn wereldwijd belangrijke oorzaken van ziekte en overlijden. Levensstijl speelt hierbij een belangrijke rol, maar ook familiegeschiedenis telt: sommige mensen zijn door hun erfelijk materiaal vatbaarder voor deze aandoeningen. Deze studie had als doel te ontdekken welke genen werkelijk verantwoordelijk zijn voor het gelijktijdig verhogen van het risico op meerdere grote vaataandoeningen, en hoe deze genen werken in de cellen die onze bloedvaten opbouwen en onderhouden.
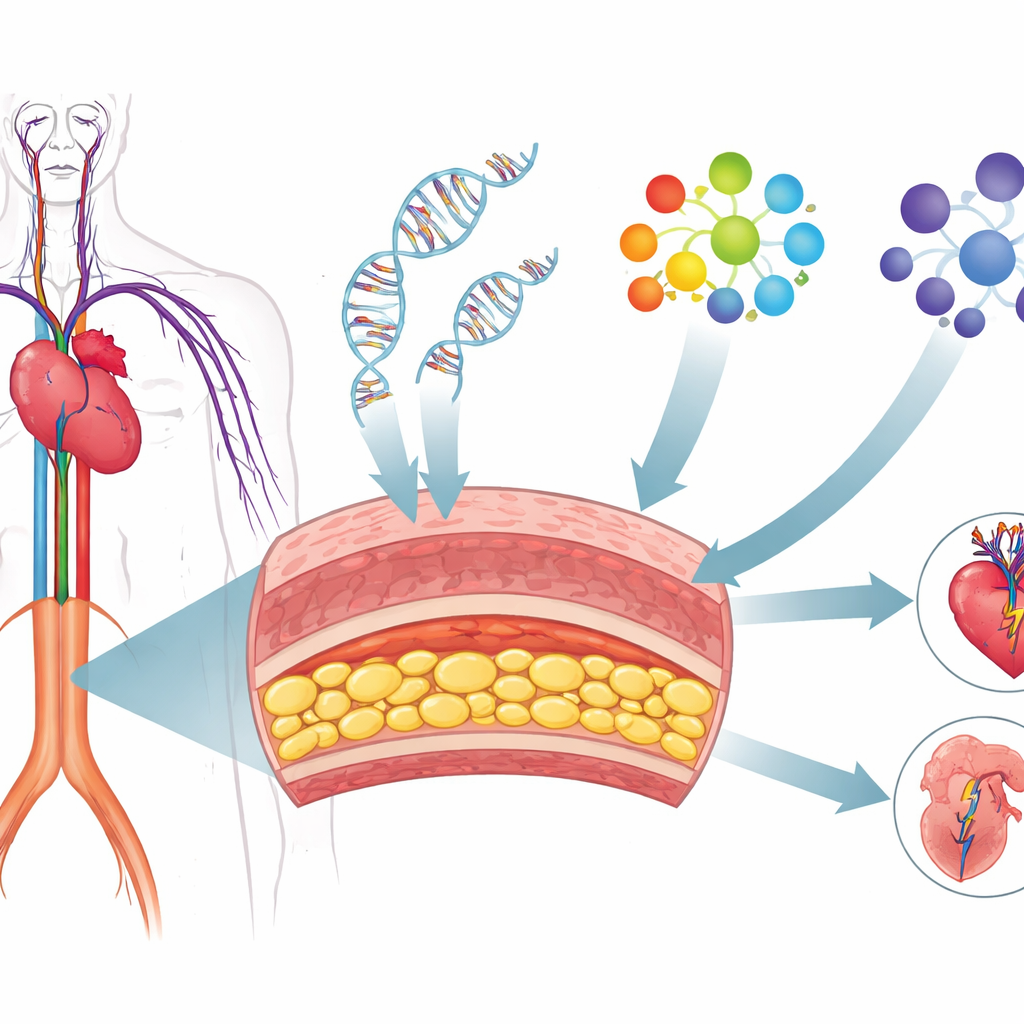
Van DNA-sporen naar werkbare genlijsten
In het afgelopen decennium hebben omvangrijke genetische onderzoeken honderden locaties in ons DNA aangemerkt die verband houden met coronaire hartziekte, hoge bloeddruk, beroerte en abdominaal aorta-aneurysma. De meeste van deze DNA-veranderingen liggen niet in de eiwitcoderende delen van genen; ze bevinden zich in regulerende regio’s die bepalen wanneer en waar genen worden ingeschakeld. Daardoor is het lastig vast te stellen welke specifieke genen de boosdoeners zijn en hoe ze handelen. De onderzoekers losten dit op door deze grote genetische kaarten te combineren met gedetailleerde metingen van genactiviteit in een belangrijke celsoort: vasculaire gladde spiercellen, de contractiele cellen die de middelste laag van de vaatwand vormen en helpen het vaattonus en de structuur te regelen.
Inzoomen op spiercellen van bloedvaten
Om te zien hoe erfelijke varianten deze cellen beïnvloeden, bouwde het team een grote biobank met gladde spiercellen afkomstig uit de naveladers van 1.486 pasgeborenen. Van elk monster bepaalden ze de DNA-volgorde over het hele genoom en maten ze de activiteit van duizenden genen. Zo konden ze varianten aanwijzen die consequent de activiteit van nabijgelegen genen in deze cellen verhogen of verlagen. Daarna onderzochten ze welke van deze varianten overlappen met bekende risicoregio’s voor vaatziekten, met behulp van statistische methoden die testen of dezelfde DNA-verandering waarschijnlijk zowel de veranderde genactiviteit als het ziekterisico aandrijft. Deze integratieve benadering bracht meer dan 130 waarschijnlijke causale genen voor coronaire hartziekte aan het licht, tientallen voor hoge bloeddruk en aneurysma, en een kleinere set voor beroerte.
Gedeelde genen bij meerdere ziekten
Veel van de aangetoonde genen werden al verdacht als spelers in de vaatbiologie, wat vertrouwen geeft in de methode, maar anderen waren geheel nieuw. Door genlijsten tussen ziekten te vergelijken, vonden de onderzoekers 18 pleiotrope genen—genen die schijnbaar invloed hebben op meer dan één vaataandoening. Deze gedeelde genen suggereren dat gemeenschappelijke defecten in het gedrag van gladde spiercellen, zoals overmatige groei, bewegen of verlies van hun gebruikelijke contractiele identiteit, het ontstaan van uiteenlopende aandoeningen kunnen aansturen, van pijn op de borst tot aneurysma. Het team raadpleegde ook geneesmiddelendatabases en ontdekte dat meerdere van de waarschijnlijke causale genen, inclusief enkele gedeelde, eiwitten coderen die al door bestaande medicijnen worden aangesproken of chemisch hanteerbaar lijken, wat deuren opent voor herbestemming of nieuwe medicijnontwikkeling.
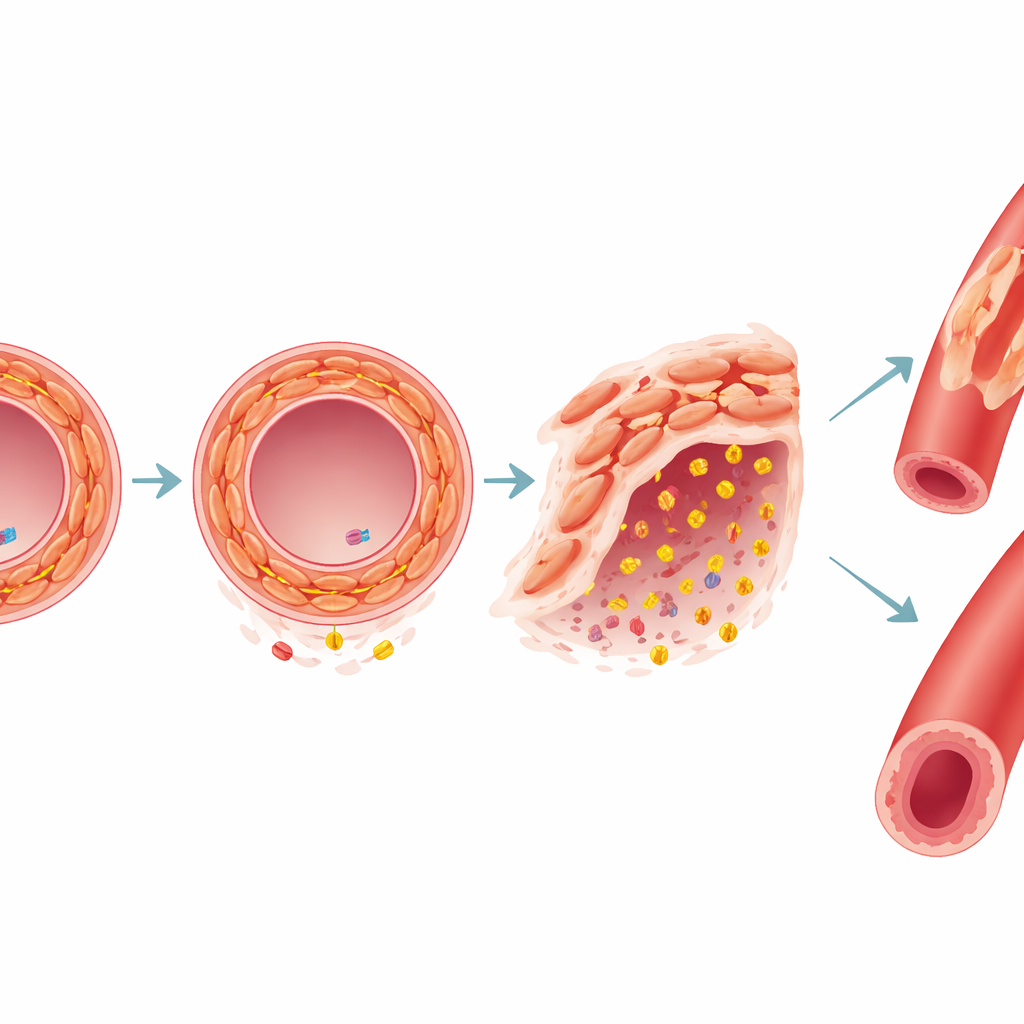
Een belangrijk gen volgen van cellen naar dieren
Een van de meest opvallende gedeelde genen was FES, dat varianten draagt die gekoppeld zijn aan zowel coronaire hartziekte als hoge bloeddruk. In in-vitro gekweekte gladde spiercellen maakte het verlagen van FES de cellen beweeglijker en verschuiven ze van een kalme, contractiele staat naar een meer agressieve, remodellerende toestand. Het verhoogde ook de productie van enzymen die de ondersteunende matrix rond cellen afbreken, waardoor de vaatwand verandert. Muizen die zo waren gefokt dat het verwante Fes-gen ontbrak, ontwikkelden grotere vetrijke plaques in de aorta en hadden hogere bloeddruk dan hun nestgenoten, met een verminderde capaciteit van hun vaten om te ontspannen. Gegevens uit de UK Biobank toonden bovendien aan dat zeldzame, schadelijke veranderingen in FES bij mensen geassocieerd waren met verhoogde bloeddruk, hogere kans op hypertensie en ongeveer een verdubbeling van het risico op hartaanval en angina pectoris.
Wat dit betekent voor toekomstige behandelingen
Samen vormt dit werk een vollediger kaart die specifieke genen, met name in gladde spiercellen, koppelt aan meerdere grote vaataandoeningen. Het laat zien dat veel risicovarianten werken door subtiel signaleringsroutes binnen deze cellen te herschikken, waardoor ze gedrag aannemen dat vaatwanden verdikt, plaquegroei bevordert of arterieën verstijft. Door pleiotrope genen zoals FES te identificeren en aan te geven welke mogelijk drugbaar zijn, biedt de studie een gerichte set doelen die, op termijn, kunnen helpen om hartaanvallen, beroertes, hoge bloeddruk en aneurysma’s gezamenlijk te voorkomen of behandelen in plaats van elke ziekte afzonderlijk.
Bronvermelding: Solomon, C.U., McVey, D.G., Andreadi, C. et al. Integrative functional genomics analysis identifies pleiotropic genes for vascular diseases. Nat Commun 17, 3376 (2026). https://doi.org/10.1038/s41467-026-69273-8
Trefwoorden: vaatgenetica, gladde spiercellen, coronaire hartziekte, hypertensie, atherosclerose