Clear Sky Science · fr
Une analyse intégrative de génomique fonctionnelle identifie des gènes pléiotropes pour les maladies vasculaires
Pourquoi nos vaisseaux sanguins comptent pour la santé de tous les jours
Les infarctus, les AVC, l’hypertension et les dilatations de l’artère principale (anévrismes de l’aorte abdominale) sont des causes majeures de maladie et de décès dans le monde. On sait que le mode de vie joue un rôle important, mais l’histoire familiale compte aussi : certaines personnes sont plus susceptibles de développer ces affections en raison des gènes hérités. Cette étude visait à déterminer quels gènes sont réellement responsables d’une élévation du risque pour plusieurs maladies vasculaires majeures à la fois, et comment ils agissent sur les cellules qui construisent et entretiennent nos vaisseaux sanguins.
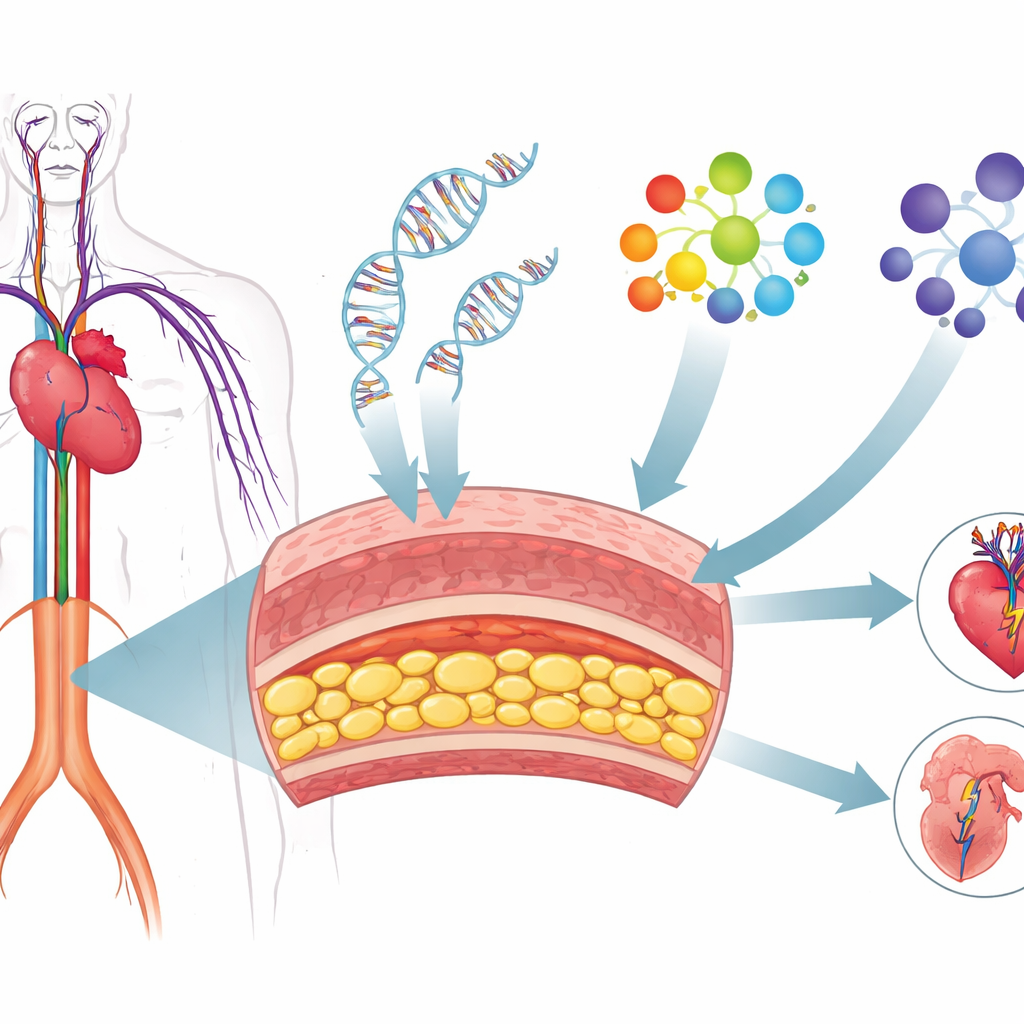
Des indices ADN aux listes de gènes fonctionnels
Au cours de la dernière décennie, d’imposantes enquêtes génétiques ont identifié des centaines d’emplacements dans notre ADN associés à la maladie coronarienne, à l’hypertension, aux accidents vasculaires cérébraux et aux anévrismes de l’aorte abdominale. La plupart de ces variations ne se trouvent pas dans les régions codantes des gènes ; elles sont plutôt situées dans des régions régulatrices qui influencent quand et où les gènes sont activés. Cela rend difficile de savoir quels gènes précis sont en cause et comment ils agissent. Les chercheurs ont abordé ce problème en combinant ces larges cartes génétiques avec des mesures détaillées de l’activité génique dans un type cellulaire clé : les cellules musculaires lisses vasculaires, les cellules contractiles qui forment la couche médiane des parois artérielles et contribuent au tonus et à la structure des vaisseaux.
Se concentrer sur les cellules musculaires des vaisseaux
Pour voir comment les variants hérités affectent ces cellules, l’équipe a constitué une grande « biobanque » de cellules musculaires lisses prélevées dans les artères ombilicales de 1 486 nouveau‑nés. Pour chaque échantillon, ils ont séquencé l’ADN sur l’ensemble du génome et mesuré l’activité de milliers de gènes. Cela leur a permis d’identifier des variants qui modifient de façon cohérente l’activité de gènes voisins dans ces cellules. Ils ont ensuite vérifié lesquels de ces variants se superposaient aux régions de risque connues pour les maladies vasculaires, en utilisant des outils statistiques qui testent si la même variation d’ADN est probablement à l’origine à la fois de l’altération de l’activité génique et du risque de maladie. Cette approche intégrative a mis en évidence plus de 130 gènes probablement causaux pour la maladie coronarienne, des dizaines pour l’hypertension et l’anévrisme, et un ensemble plus restreint pour l’AVC.
Gènes partagés entre plusieurs maladies
Beaucoup des gènes identifiés étaient déjà suspectés d’intervenir dans la biologie vasculaire, ce qui renforce la fiabilité de la méthode, mais d’autres étaient entièrement nouveaux. En comparant les listes de gènes entre les maladies, les chercheurs ont trouvé 18 gènes « pléiotropes » — des gènes qui semblent influencer plus d’une maladie vasculaire. Ces gènes partagés suggèrent que des défauts communs du comportement des cellules musculaires lisses, tels qu’une croissance excessive, une mobilité accrue ou la perte de leur identité contractile habituelle, contribuent à des affections très différentes, de la poitrine douloureuse aux anévrismes. L’équipe a également consulté des bases de données de médicaments et constaté que plusieurs des gènes probablement causaux, y compris certains des gènes partagés, codent des protéines déjà ciblées par des médicaments existants ou présentent des caractéristiques chimiques exploitables, ouvrant la voie au repositionnement ou au développement de nouvelles thérapeutiques.
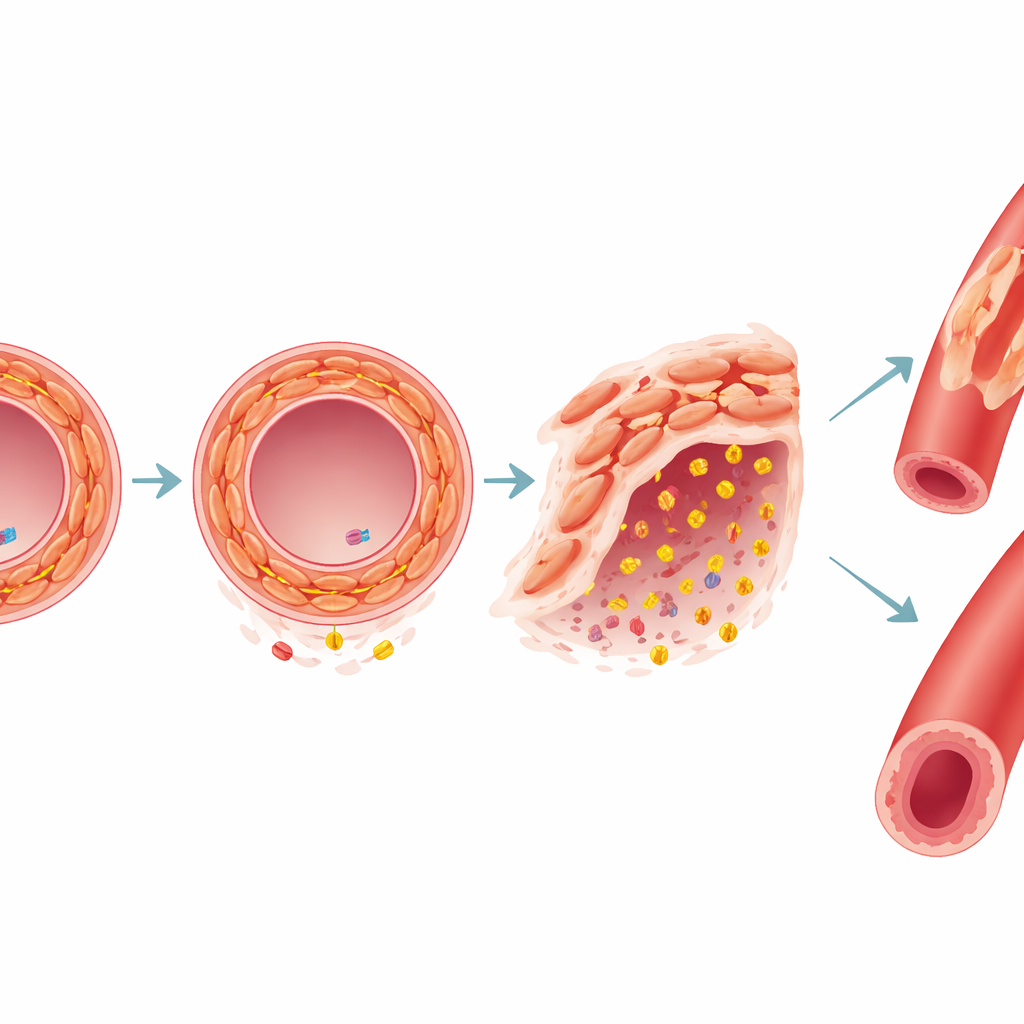
Suivre un gène clé des cellules aux animaux
L’un des gènes partagés les plus marquants était FES, qui porte des variants liés à la fois à la maladie coronarienne et à l’hypertension. Dans des cellules musculaires lisses cultivées en laboratoire, la diminution de l’expression de FES rendait les cellules plus mobiles et les faisait passer d’un état calme et contractile vers un état plus agressif et remodelant. Cela augmentait aussi la production d’enzymes qui dégradent la matrice de soutien autour des cellules, modifiant ainsi la paroi vasculaire. Chez des souris privées du gène apparenté Fes, les animaux développaient des plaques adipeuses plus importantes dans l’aorte et présentaient une tension artérielle plus élevée que leurs congénères, avec une capacité réduite des vaisseaux à se relâcher. Les données humaines issues de l’UK Biobank ont en outre montré que des variants rares et délétères de FES étaient associés à une pression artérielle plus élevée, à des risques accrus d’hypertension, et à environ le double du risque d’infarctus et d’angine.
Ce que cela signifie pour les traitements futurs
Dans l’ensemble, ces travaux fournissent une carte plus complète reliant des gènes spécifiques, en particulier dans les cellules musculaires lisses, à plusieurs grandes maladies vasculaires. Ils montrent que de nombreux variants de risque agissent en réorientant subtilement les voies de signalisation à l’intérieur de ces cellules, les incitant à adopter des comportements qui épaississent la paroi des vaisseaux, favorisent la croissance des plaques ou rigidifient les artères. En identifiant des gènes pléiotropes comme FES et en signalant ceux qui sont potentiellement « druggables », l’étude propose un ensemble ciblé de cibles qui pourrait, à terme, aider à prévenir ou traiter les infarctus, les AVC, l’hypertension et les anévrismes de manière conjointe plutôt que maladie par maladie.
Citation: Solomon, C.U., McVey, D.G., Andreadi, C. et al. Integrative functional genomics analysis identifies pleiotropic genes for vascular diseases. Nat Commun 17, 3376 (2026). https://doi.org/10.1038/s41467-026-69273-8
Mots-clés: génétique vasculaire, cellules musculaires lisses, maladie coronarienne, hypertension, athérosclérose