Clear Sky Science · de
Integrative funktionale Genomik-Analyse identifiziert pleiotrope Gene für Gefäßerkrankungen
Warum unsere Blutgefäße für die alltägliche Gesundheit wichtig sind
Herzinfarkte, Schlaganfälle, Bluthochdruck und Aussackungen der Hauptschlagader (Aortenaneurysmen) gehören weltweit zu den führenden Ursachen von Krankheit und Tod. Wir wissen, dass der Lebensstil eine wichtige Rolle spielt, doch auch die Familiengeschichte zählt: Manche Menschen sind aufgrund ihrer erblichen Anlagen anfälliger für diese Erkrankungen. Diese Studie hatte zum Ziel herauszufinden, welche Gene tatsächlich das Risiko für mehrere wichtige Gefäßerkrankungen gleichzeitig erhöhen und wie sie auf die Zellen wirken, die unsere Blutgefäße aufbauen und erhalten.
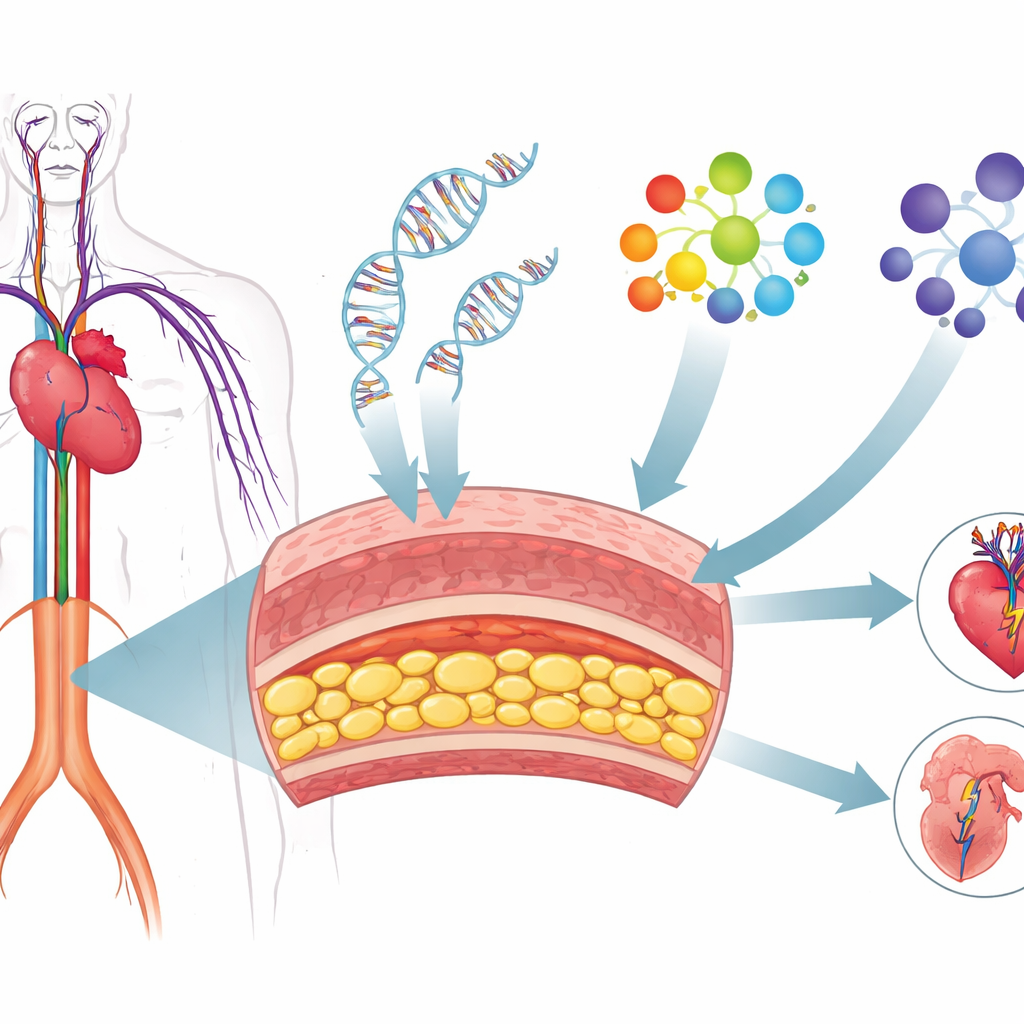
Von DNA-Hinweisen zu funktionalen Genlisten
In den letzten zehn Jahren haben groß angelegte genetische Studien Hunderte Stellen in unserer DNA identifiziert, die mit koronarer Herzkrankheit, Bluthochdruck, Schlaganfall und Bauchaortenaneurysma in Verbindung stehen. Die meisten dieser DNA-Varianten liegen nicht in den proteinkodierenden Abschnitten von Genen, sondern in regulatorischen Regionen, die beeinflussen, wann und wo Gene ein- oder ausgeschaltet werden. Das erschwert die Zuordnung, welche konkreten Gene verantwortlich sind und wie sie wirken. Die Forschenden gingen dieses Problem an, indem sie diese umfassenden genetischen Karten mit detaillierten Messungen der Genaktivität in einer zentralen Zellart kombinierten: vaskulären glatten Muskelzellen, den kontraktilen Zellen, die die mittlere Schicht der Arterienwand bilden und die Gefäßspannung sowie -struktur mitsteuern.
Genauer Blick auf die Muskelzellen der Blutgefäße
Um zu untersuchen, wie ererbte Varianten diese Zellen beeinflussen, bauten die Forscher eine große „Biobank“ von glatten Muskelzellen auf, die aus den Nabelschnurarterien von 1.486 Neugeborenen gewonnen wurden. Für jede Probe bestimmten sie die DNA-Sequenz im gesamten Genom und maßen die Aktivität Tausender Gene. So konnten sie Varianten lokalisieren, die in diesen Zellen konstant die Aktivität benachbarter Gene erhöhen oder senken. Anschließend prüften sie, welche dieser Varianten mit bekannten Risikoregionen für Gefäßerkrankungen überlappten, mithilfe statistischer Verfahren, die testen, ob dieselbe DNA-Veränderung wahrscheinlich sowohl die veränderte Genaktivität als auch das Krankheitsrisiko antreibt. Dieser integrative Ansatz hob mehr als 130 wahrscheinlich kausale Gene für koronare Herzkrankheit, mehrere Dutzend für Bluthochdruck und Aneurysma sowie eine kleinere Gruppe für Schlaganfall hervor.
Gemeinsame Gene über mehrere Erkrankungen hinweg
Viele der identifizierten Gene galten bereits als vermutete Akteure in der Gefäßbiologie, was der Methode Vertrauen gab, andere waren völlig neu. Durch den Vergleich der Genlisten über die Erkrankungen hinweg fanden die Forschenden 18 „pleiotrope“ Gene — also Gene, die offenbar mehr als eine Gefäßerkrankung beeinflussen. Diese gemeinsamen Gene deuten darauf hin, dass grundlegende Störungen im Verhalten glatter Muskelzellen, etwa übermäßiges Wachstum, vermehrte Beweglichkeit oder der Verlust ihrer typischen kontraktilen Identität, unterschiedliche Krankheitsbilder von Brustschmerz bis zum Aneurysma begünstigen. Das Team durchsuchte außerdem Wirkstoffdatenbanken und fand, dass mehrere der wahrscheinlich kausalen Gene, einschließlich einiger gemeinsamer Gene, Proteine kodieren, die bereits von bestehenden Medikamenten adressiert werden oder chemisch zugänglich erscheinen, was Möglichkeiten für Wirkstoffumschichtung oder neue Arzneimittelentwicklung eröffnet.
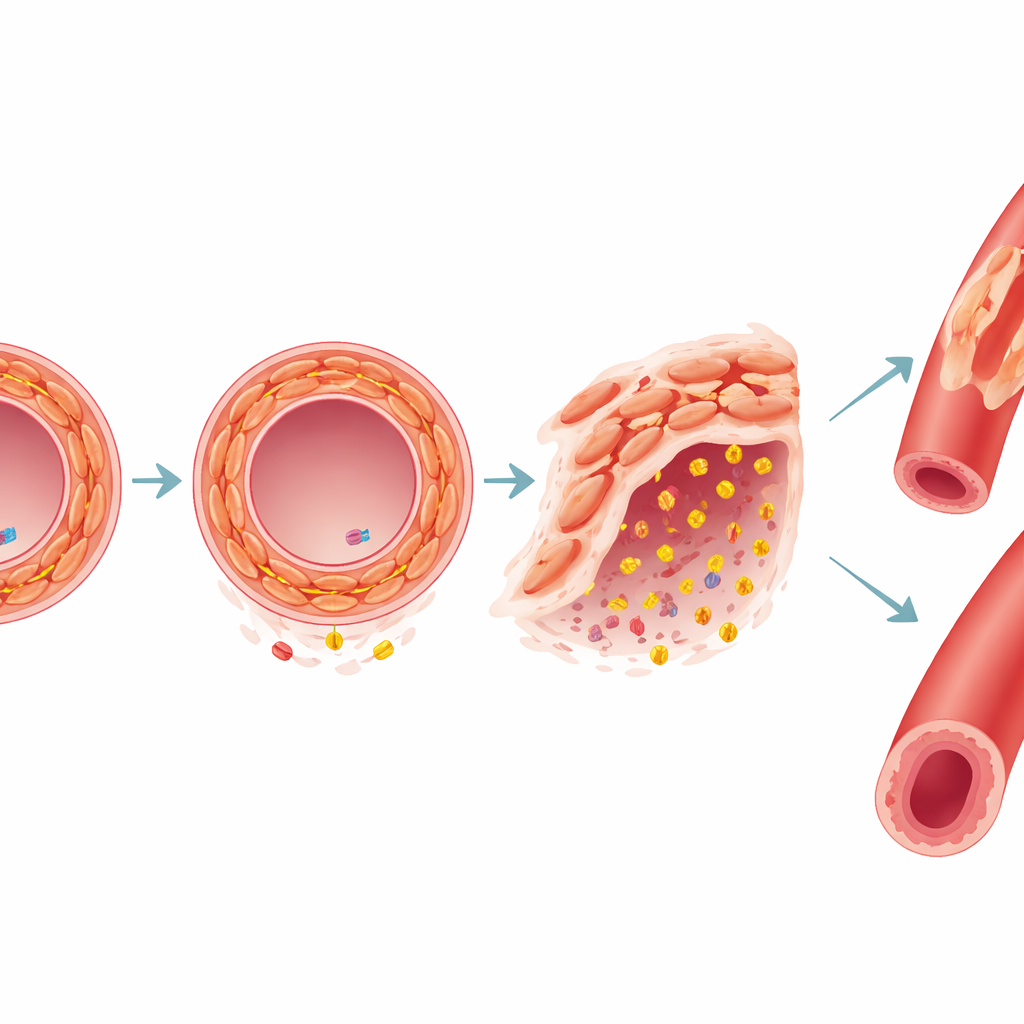
Einem Schlüsselgen von der Zelle zum Tier folgen
Eines der auffälligsten gemeinsamen Gene war FES, das Varianten trägt, die mit sowohl koronarer Herzkrankheit als auch Bluthochdruck verbunden sind. In im Labor kultivierten glatten Muskelzellen führte die Herunterregulierung von FES zu erhöhter Mobilität der Zellen und verschob deren Zustand von ruhig und kontraktil hin zu einem aktiveren, umbauenden Phänotyp. Außerdem steigerten sich die Mengen an Enzymen, die die stützende Matrix um die Zellen abbauen, wodurch die Gefäßwand verändert wurde. Mäuse, denen das verwandte Gen Fes fehlte, entwickelten größere fetthaltige Plaques in der Aorta und hatten höheren Blutdruck als ihre Wurfgeschwister sowie eine eingeschränkte Fähigkeit der Gefäße, sich zu entspannen. Daten des UK Biobank zeigten weiter, dass seltene, schädigende Veränderungen in FES beim Menschen mit erhöhtem Blutdruck, höheren Chancen für Hypertonie und etwa doppelt so hohem Risiko für Herzinfarkt und Angina assoziiert sind.
Was das für künftige Behandlungen bedeutet
In der Summe liefert die Arbeit eine umfassendere Karte, die spezifische Gene — insbesondere in glatten Muskelzellen — mit mehreren wichtigen Gefäßerkrankungen verknüpft. Sie zeigt, dass viele Risikovarianten wirken, indem sie Signalwege innerhalb dieser Zellen fein umschalten und sie zu Verhaltensweisen führen, die Gefäßwände verdicken, Plaquebildung fördern oder Arterien versteifen. Indem sie pleiotrope Gene wie FES herausstellen und verdeutlichen, welche davon potenziell medikamentös angreifbar sind, bietet die Studie eine fokussierte Reihe von Zielmolekülen, die mittelfristig helfen könnten, Herzinfarkte, Schlaganfälle, Bluthochdruck und Aneurysmen gemeinsam statt nur einzeln zu verhindern oder zu behandeln.
Zitation: Solomon, C.U., McVey, D.G., Andreadi, C. et al. Integrative functional genomics analysis identifies pleiotropic genes for vascular diseases. Nat Commun 17, 3376 (2026). https://doi.org/10.1038/s41467-026-69273-8
Schlüsselwörter: Gefäßgenetik, glatte Muskelzellen, Koronare Herzkrankheit, Hypertonie, Atherosklerose