Clear Sky Science · it
Analisi integrativa di genomica funzionale identifica geni pleiotropici per le malattie vascolari
Perché i nostri vasi sanguigni contano per la salute di tutti i giorni
Infarti, ictus, ipertensione e dilatazioni dell’aorta addominale sono tra le principali cause di malattia e morte a livello globale. Sappiamo che lo stile di vita ha un ruolo importante, ma conta anche la storia familiare: alcune persone sono semplicemente più predisposte a queste patologie a causa dei geni ereditati. Questo studio si è proposto di scoprire quali geni sono davvero responsabili dell’aumento del rischio di diverse malattie vascolari contemporaneamente e in che modo agiscono sulle cellule che costruiscono e mantengono i nostri vasi sanguigni.
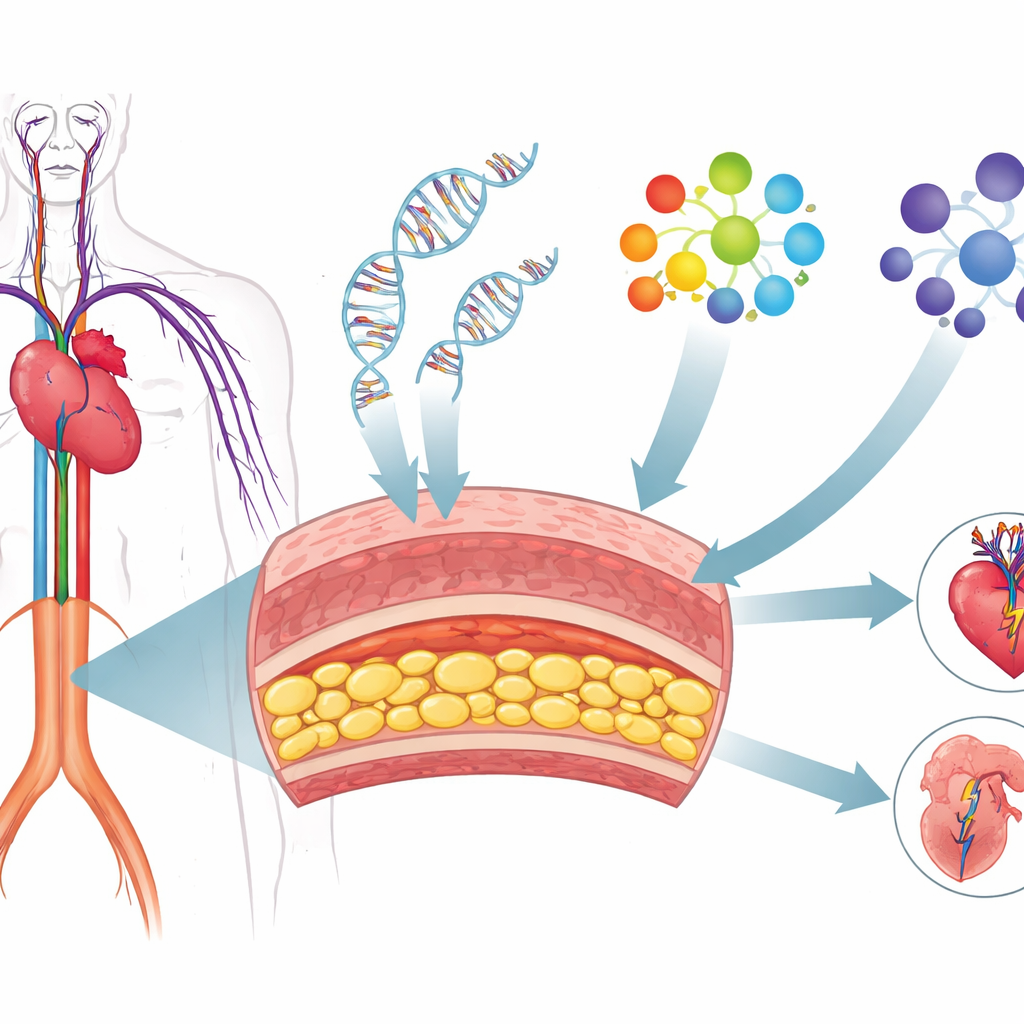
Dai segnali del DNA a elenchi di geni funzionali
Nel corso dell’ultimo decennio, ampie indagini genetiche hanno individuato centinaia di punti nel nostro DNA collegati a malattia coronarica, ipertensione, ictus e aneurisma aortico addominale. La maggior parte di queste variazioni non ricade nelle porzioni di geni che codificano proteine; si trovano piuttosto in regioni regolatorie che influenzano quando e dove i geni vengono attivati. Questo rende difficile capire quali geni specifici siano implicati e come agiscano. I ricercatori hanno affrontato il problema combinando queste mappe genetiche con misure dettagliate dell’attività genica in un tipo cellulare chiave: le cellule muscolari lisce vascolari, le cellule contrattili che formano lo strato mediale delle pareti arteriose e aiutano a controllare tono e struttura del vaso.
Avvicinarsi alle cellule muscolari dei vasi
Per vedere come le varianti ereditarie influenzano queste cellule, il gruppo ha costruito un ampio «biobanca» di cellule muscolari lisce ricavate dalle arterie ombelicali di 1.486 neonati. Per ogni campione hanno letto la sequenza del DNA su tutto il genoma e misurato l’attività di migliaia di geni. Questo ha permesso di identificare varianti che aumentano o diminuiscono in modo coerente l’attività dei geni vicini in queste cellule. Hanno quindi verificato quali di queste varianti si sovrapponevano a regioni di rischio note per le malattie vascolari, utilizzando strumenti statistici che testano se lo stesso cambiamento nel DNA è probabilmente responsabile sia della variazione nell’attività genica sia del rischio di malattia. Questo approccio integrativo ha evidenziato più di 130 geni probabilmente causali per la malattia coronarica, diverse decine per ipertensione e aneurisma, e un numero minore per l’ictus.
Geni condivisi tra più patologie
Molti dei geni individuati erano già considerati attori nella biologia vascolare, a conferma dell’approccio, ma altri erano del tutto nuovi. Confrontando gli elenchi di geni tra le malattie, i ricercatori hanno trovato 18 geni «pleiotropici»—geni che sembrano influenzare più di una malattia vascolare. Questi geni condivisi suggeriscono che difetti comuni nel comportamento delle cellule muscolari lisce, come crescita eccessiva, mobilità aumentata o perdita della loro abituale identità contrattilе, contribuiscono a condizioni molto diverse, dal dolore toracico all’aneurisma. Il gruppo ha inoltre consultato banche dati sui farmaci e ha rilevato che diversi dei geni probabilmente causali, inclusi alcuni condivisi, codificano proteine già bersaglio di medicinali esistenti o risultano chimicamente trattabili, aprendo la porta a riposizionamenti farmacologici o a nuovi sviluppi terapeutici.
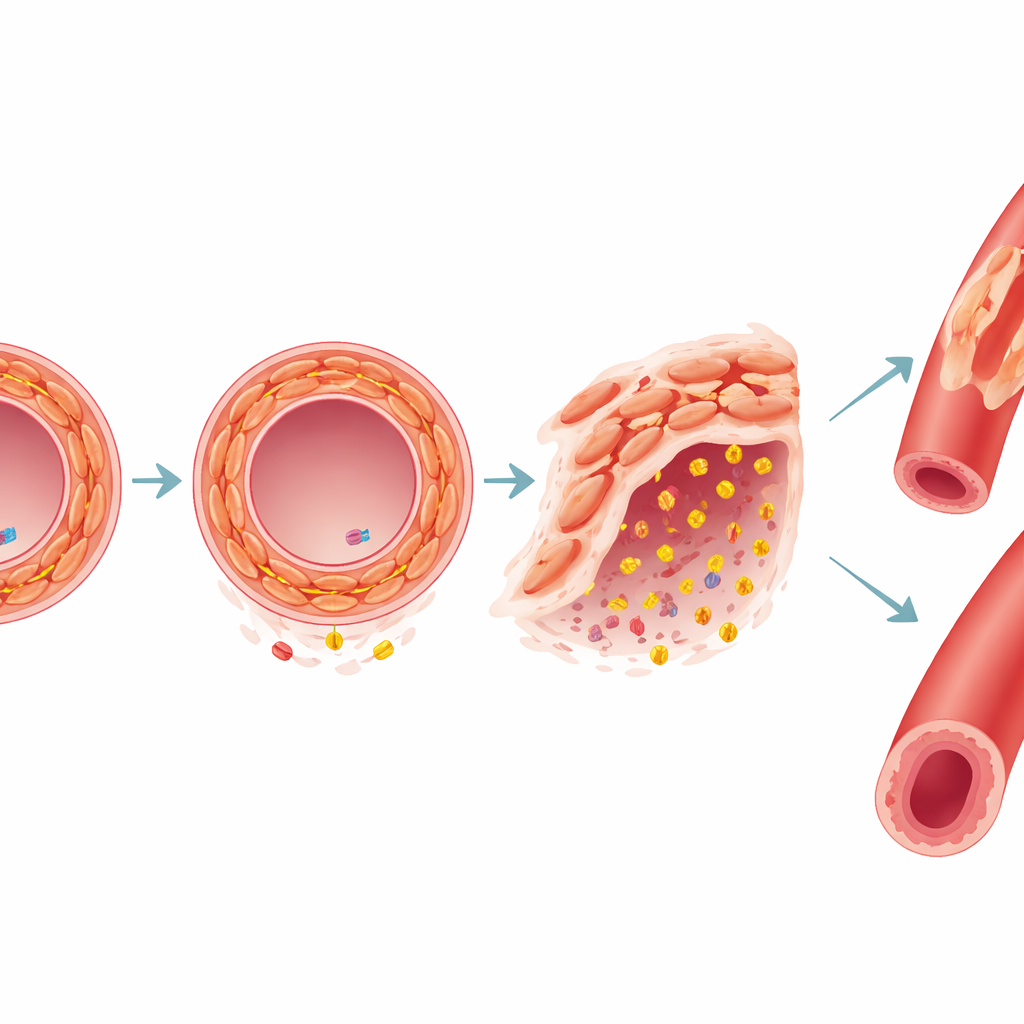
Seguire un gene chiave dalle cellule agli animali
Uno dei geni condivisi più rilevanti è risultato FES, che porta varianti collegate sia alla malattia coronarica sia all’ipertensione. Nelle cellule muscolari lisce coltivate in laboratorio, la riduzione dell’espressione di FES ha reso le cellule più mobili e le ha spostate da uno stato calmo e contrattilе verso uno stato più aggressivo e di rimodellamento. Ha inoltre aumentato la produzione di enzimi che degradano la matrice di supporto intorno alle cellule, alterando la parete vascolare. In topi privi del gene correlato Fes, gli animali hanno sviluppato placche lipidiche più estese nell’aorta e hanno mostrato pressione arteriosa più elevata rispetto ai fratelli di cucciolata, con una ridotta capacità dei vasi di rilassarsi. Dati umani provenienti dall’UK Biobank hanno ulteriormente mostrato che rare varianti dannose in FES erano associate a pressione arteriosa aumentata, maggiore probabilità di ipertensione e circa il doppio del rischio di infarto e angina.
Cosa significa per i trattamenti futuri
Nel complesso, il lavoro fornisce una mappa più completa che collega geni specifici, soprattutto nelle cellule muscolari lisce, a diverse grandi malattie vascolari. Mostra che molte varianti di rischio agiscono rimodellando sottilmente le vie di segnalazione all’interno di queste cellule, spingendole verso comportamenti che ispessiscono le pareti vascolari, favoriscono la crescita della placca o irrigidiscono le arterie. Identificando geni pleiotropici come FES e mettendo in evidenza quali siano potenzialmente bersagliabili farmacologicamente, lo studio propone un insieme mirato di obiettivi che potrebbero, nel tempo, contribuire a prevenire o curare infarti, ictus, ipertensione e aneurismi non più singolarmente ma insieme.
Citazione: Solomon, C.U., McVey, D.G., Andreadi, C. et al. Integrative functional genomics analysis identifies pleiotropic genes for vascular diseases. Nat Commun 17, 3376 (2026). https://doi.org/10.1038/s41467-026-69273-8
Parole chiave: genetica vascolare, cellule muscolari lisce, malattia delle arterie coronarie, ipertensione, aterosclerosi