Clear Sky Science · nl
Single-cell imaginganalyse, therapeutische modellering en een fase Ib-proef valideren BCL-2 als doelwit bij heterogene castratieresistente prostaatkanker
Waarom dit onderzoek ertoe doet
Veel mannen met gevorderde prostaatkanker komen uiteindelijk in een stadium waarin standaard hormoonremmende medicijnen niet meer werken. Deze studie stelt een eenvoudig maar dringend vraagstuk: wanneer tumoren leren zonder mannelijke hormonen te leven, vertrouwen ze dan allemaal op een gemeenschappelijke “overlevingsschakelaar” die artsen kunnen richten? Door individuele kankercellen te volgen, geneesmiddelen in modellen te testen en een vroege klinische proef uit te voeren, identificeren de onderzoekers zo’n schakelaar — een eiwit genaamd BCL-2 — en tonen ze aan dat het blokkeren ervan kan helpen bij de behandeling van anderszins resistente ziekte.
Het probleem van hardnekkige prostaattumoren
Moderne middelen die mannelijke hormonen uitschakelen of hun receptor blokkeren hebben het leven van veel mannen verlengd. Toch overlijden er nog steeds duizenden mensen per jaar aan gemetastaseerde castratieresistente prostaatkanker, een vorm die blijft groeien ondanks deze behandelingen. Een belangrijke reden is variatie: binnen één tumor zijn sommige cellen sterk afhankelijk van hormoonsignalen, terwijl andere ze nauwelijks gebruiken. Wanneer hormoonblokkerende middelen worden gegeven, sterven of krimpen de gevoelige cellen, maar de hardere cellen overleven, passen zich aan en domineren uiteindelijk. Artsen vermoeden al langer dat deze overlevers steunen op reserve-overlevingsprogramma’s, maar het was onduidelijk welke programma’s gedeeld worden tussen verschillende resistente tumortypen.
De overlevingsschakelaar vinden in enkele cellen
Het team richtte zich op BCL-2, een eiwit dat cellen helpt geprogrammeerde celdood te vermijden. Met geavanceerde beeldvormingstools die vele eiwitten in duizenden cellen tegelijk kunnen meten, onderzochten ze goedaardig prostaatweefsel, onbehandelde primaire tumoren en resistente tumoren van patiënten, evenals meerdere muismodellen. In gezonde klieren bevinden de hormoonreceptoren en BCL-2 zich grotendeels in aparte cellagen. In onbehandelde kankers tonen de meeste cellen sterke hormoonreceptoren maar weinig BCL-2. Na langdurige hormoonblokkade keert dat patroon zich echter om: resistente kankers raken rijk aan BCL-2–positieve cellen, inclusief cellen die nog de hormoonreceptor dragen en cellen die die receptor grotendeels verloren hebben. In meerdere datasets nam BCL-2-activiteit toe naarmate hormoonsignaal afnam, wat wijst op een nauwe, wipbrugachtige relatie tussen de twee.
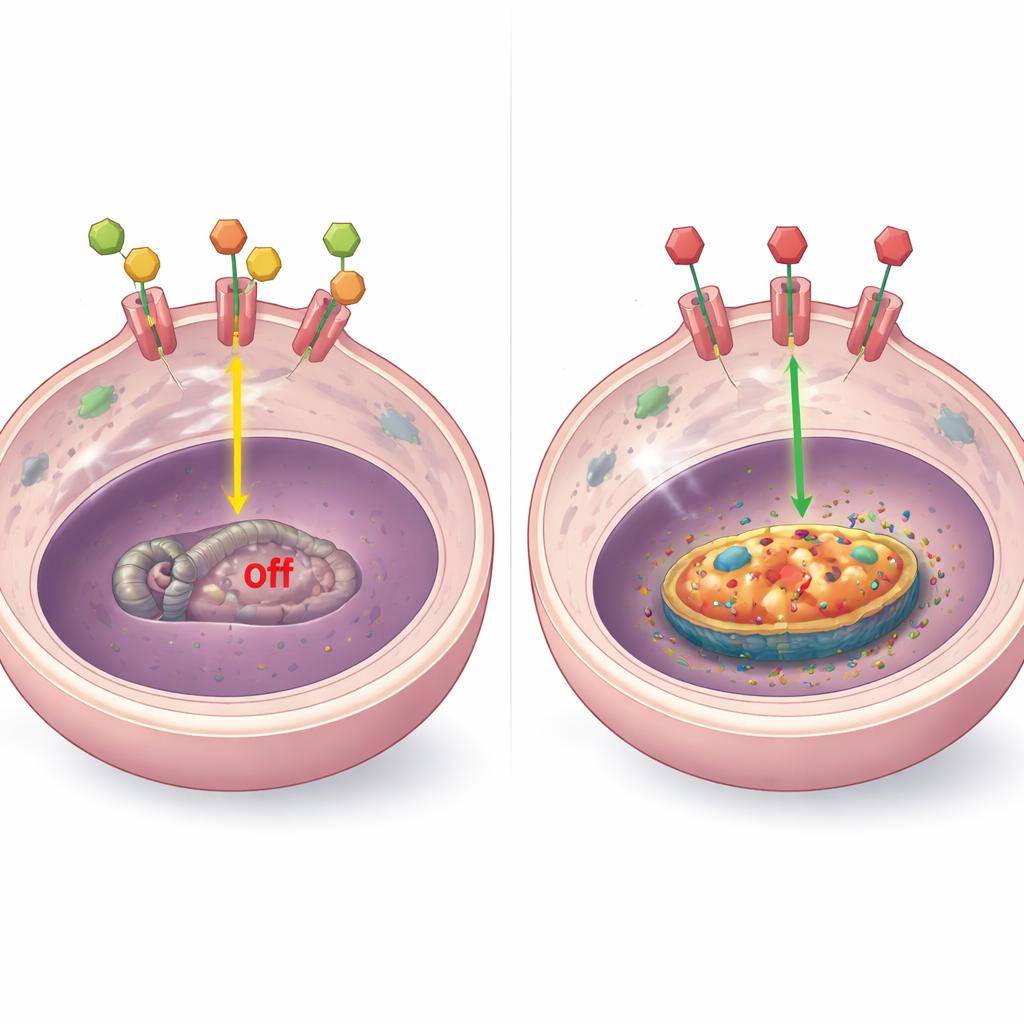
Hoe hormoonsignalen BCL-2 beheersen
Om het mechanisme te begrijpen onderzochten de onderzoekers hoe de hormoonreceptor inwerkt op het BCL-2-gen. In laboratoriummodellen vonden ze dat, wanneer hormonen aanwezig zijn, de receptor fysiek bindt aan meerdere plaatsen nabij het BCL-2-gen en het geviseerd gen onderdrukt. Wanneer hormonen worden verwijderd of de receptor door medicijnen wordt geblokkeerd, verdwijnt deze binding, wordt het lokale DNA meer “open” en stijgen de BCL-2-niveaus. Dit patroon verscheen in diverse resistente tumortypen, inclusief die met hoge receptorwaarden, lage of afwezige receptor en receptor die uit de kern is verschoven. In enkele bijzondere gevallen beïnvloedden andere factoren zoals gewijzigde receptorfragmenten of de stress-responsreceptor (GR) ook BCL-2, maar het centrale thema bleef: het uitschakelen van normale hormoonsignalering haalt de rem van dit overlevingsproteïne.
BCL-2 testen als zwakke plek
Gewapend met dit inzicht vroeg het team zich af of BCL-2 slechts een merker van resistentie is of een echte kwetsbaarheid die ze kunnen benutten. Ze gebruikten organoïden (mini-tumoren gekweekt in gel) en muistumoren die drie belangrijke resistente subtypen vertegenwoordigden: die nog rijk zijn aan nucleaire hormoonreceptor, die met lage receptor en die met receptor grotendeels vastgehouden in het cellichaam in plaats van de kern. In alle drie verminderde de klinisch gebruikte BCL-2-remmer venetoclax (ABT-199) tumorgrootte of vertraagde de groei, vaak effectiever dan hormoonblokkerende middelen alleen. In modellen die nog enige hormoonsignalering hadden, gaf de combinatie van venetoclax met de anti-androgeen enzalutamide sterkere effecten dan elk middel afzonderlijk, terwijl hormoononafhankelijke tumoren nog steeds reageerden op alleen BCL-2-blokkade.
Vroege aanwijzingen bij patiënten
Om te zien of deze ideeën naar mensen te vertalen zijn, voerden de onderzoekers een kleine fase Ib-proef uit met enzalutamide en venetoclax bij mannen met gevorderde resistente prostaatkanker. Met een apparaat om zeldzame tumoren uit bloed te scheiden, volgden ze BCL-2, hormoongerelateerde genen en een merker van tumorcelbelastning in de loop van de tijd. Enkele patiënten die veel cycli op de behandeling bleven hadden dalende BCL-2- en hormoonsignalen in hun circulerende tumorcellen, een afname in het aantal van deze cellen en dalende PSA-waarden in het bloed. Daarentegen hadden patiënten die niet profiteerden vaak van meet af aan zeer lage BCL-2-waarden en tekenen dat een alternatieve stresshormoonroute het overnam. Hoewel deze vroege proef klein was en de geneesmiddelconcentraties werden beperkt door medicijn–medicijninteracties, ondersteunt het het idee dat BCL-2–gedreven tumoren bijzonder kwetsbaar zijn voor deze aanpak.
Wat dit vooruit betekent
Dit werk schetst een samenhangend beeld: wanneer krachtige hormoonblokkerende behandelingen druk uitoefenen op prostaattumoren, schakelen veel overlevende cellen BCL-2 in als een gedeelde ontsnappingsroute. Door gedetailleerde single-cell beeldvorming, genetische analyse, dierexperimenten en een pilotklinische studie te combineren, leveren de auteurs sterk bewijs dat BCL-2 meer is dan een bijstander — het is een gemeenschappelijke overlevingsgreep in verschillende resistente tumorsmaken. Voor patiënten is de langetermijnbelofte een meer gerichte strategie waarin artsen zowel hormoonreceptor- als BCL-2-status meten en mannen waarvan de tumoren op deze schakelaar leunen koppelen aan behandelingen die deze direct uitschakelen.
Bronvermelding: Jamroze, A., Liu, X., Hou, S. et al. Single-cell imaging analysis, therapeutic modeling and a Phase Ib trial validate BCL-2 as a target across heterogeneous castration-resistant prostate cancer. Sig Transduct Target Ther 11, 161 (2026). https://doi.org/10.1038/s41392-026-02700-w
Trefwoorden: prostaatkanker, drugresistentie, BCL-2, hormoontherapie, gerichte therapie