Clear Sky Science · ar
تحليل التصوير خلية بخلية، نمذجة علاجية وتجربة سريرية مرحلة Ib تؤكد أن BCL-2 هدف قابل للاستهداف عبر سرطان البروستاتا المقاوم للخصي والمتغاير
لماذا هذا البحث مهم
يصاب العديد من الرجال المصابين بسرطان البروستاتا المتقدم في نهاية المطاف بمرحلة تتوقف فيها أدوية حجب الهرمونات القياسية عن العمل. يطرح هذا البحث سؤالاً بسيطاً لكنه عاجلاً: عندما تتعلم الأورام العيش من دون الهرمونات الذكرية، هل تعتمد كلها على «مفتاح بقاء» مشترك يمكن للأطباء استهدافه؟ من خلال تتبع الخلايا السرطانية الفردية، واختبار الأدوية في نماذج، وإجراء تجربة سريرية مبكرة، يحدد الباحثون أحد هذه المفاتيح — بروتين يُسمى BCL-2 — ويظهرون أن حظره قد يساعد في علاج أمراض مقاومة خلاف ذلك.
مشكلة الأورام العنيدة في البروستاتا
لقد مددّت الأدوية الحديثة التي تقطع تدفق الهرمونات الذكرية أو تحجب مستقبلاتها حياة الكثير من الرجال. ومع ذلك، لا يزال الآلاف يموتون كل سنة بسبب سرطان البروستاتا المقاوم للخصي النقيلي، شكل ينمو رغم هذه العلاجات. أحد الأسباب الرئيسة هو التنوع: داخل ورم واحد، تعتمد بعض الخلايا اعتماداً كبيراً على إشارات الهرمونات، بينما تكاد خلايا أخرى لا تستخدمها إطلاقاً. عند إعطاء أدوية حجب الهرمونات، تموت الخلايا الحسّاسة أو تنكمش، لكن الخلايا الأشد تبقى، تتكيّف، وفي النهاية تهيمن. لطالما اشتبه الأطباء أن هؤلاء الناجون يعتمدون على برامج بديلة للبقاء، لكن لم يكن واضحاً أي البرامج مشتركة عبر أنواع الأورام المقاومة المختلفة.
العثور على مفتاح البقاء في الخلايا الفردية
ركز الفريق على BCL-2، وهو بروتين يساعد الخلايا على تجنب الموت المبرمج. باستخدام أدوات تصوير متقدمة يمكنها قياس العديد من البروتينات في آلاف الخلايا دفعة واحدة، فحصوا نسيج البروستاتا السليم، والأورام الأولية غير المعالجة، والأورام المقاومة من المرضى، بالإضافة إلى عدة نماذج فأرية. في الغدد السليمة، توجد مستقبلات الهرمونات وBCL-2 في طبقات خلوية منفصلة إلى حد كبير. في السرطانات غير المعالجة، تُظهر معظم الخلايا مستقبلات هرمونية قوية لكن مستويات منخفضة من BCL-2. بعد حجب الهرمونات لفترات طويلة، ومع ذلك، ينقلب هذا النمط: تصبح الأورام المقاومة غنية بالخلايا الموجبة لـ BCL-2، بما في ذلك خلايا ما زالت تحمل مستقبل الهرمون وتلك التي فقدته إلى حد كبير. عبر مجموعات بيانات متعددة، ارتفعت نشاطات BCL-2 مع هبوط إشارات الهرمونات، مما يشير إلى علاقة متقابلة محكمة بين الاثنين.
كيف تتحكم إشارات الهرمون في BCL-2
لفهم الآلية، فحص الباحثون كيف يتفاعل مستقبل الهرمون مع جين BCL-2. في النماذج المخبرية، وجدوا أنه عندما تكون الهرمونات حاضرة، يرتبط المستقبل جسدياً بعدة مواقع بالقرب من جين BCL-2 ويبقيه مُكَبَّحاً. عندما تُزال الهرمونات أو يُحجب المستقبل بواسطة أدوية، يُفقد هذا الارتباط، ويصبح الحمض النووي المحلي أكثر «انفتاحاً»، وترتفع مستويات BCL-2. ظهر هذا النمط في أنواع أورام مقاومة متنوعة، بما في ذلك تلك ذات مستويات مستقبل عالية، وتلك ذات مستقبل منخفض أو غائب، وتلك التي انتقل فيها المستقبل خارج النواة. في بعض الحالات الخاصة، أثرت عوامل أخرى مثل شظايا مستقبل معدلة أو مستقبل استجابة الإجهاد (GR) على BCL-2 أيضاً، لكن الفكرة المركزية بقيت: إيقاف الإشارات الهرمونية الطبيعية يزيل مكابح هذا البروتين الباقي.
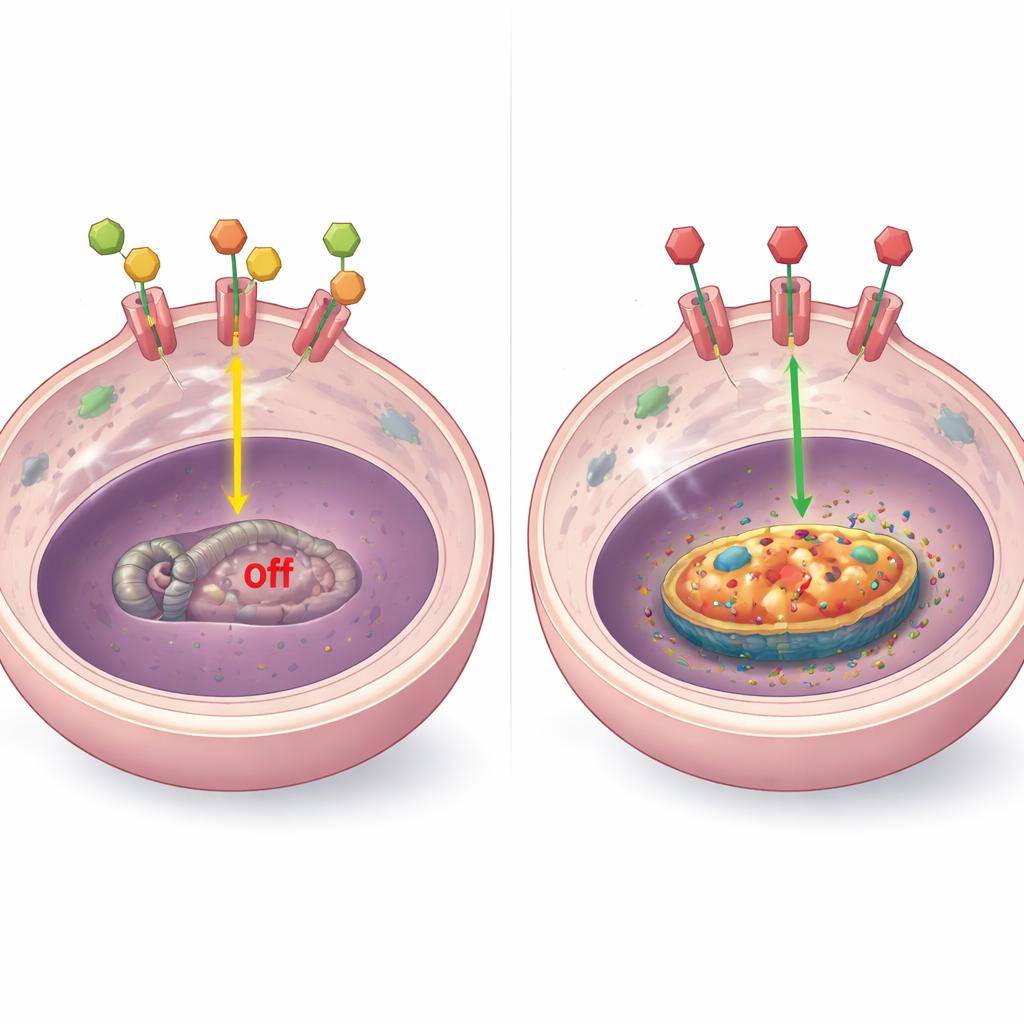
اختبار BCL-2 كنقطة ضعف
مسلحين بهذا الفهم، سأل الفريق ما إذا كان BCL-2 مجرد علامة للمقاومة أم ضعف حقيقي يمكن استغلاله. استخدموا الأوردنويدات (أورام مصغرة تُنمى في هلام) وأوراماً فأرية تمثل ثلاثة أنماط رئيسية مقاومة: تلك التي لا تزال غنية بمستقبل الهرمون النووي، وتلك ذات المستقبل المنخفض، وتلك التي يكون فيها المستقبل محتجزاً في جسد الخلية بدلاً من النواة. في الثلاثة جميعها، قلّص أو أبطأ مُثبِّط BCL-2 المستخدم في العيادة، فينِتوكلاكس (ABT-199)، الأورام أو أبطأ نموها، غالباً بفاعلية أكبر من أدوية حجب الهرمونات وحدها. في النماذج التي لا تزال فيها بعض الإشارات الهرمونية موجودة، أدى الجمع بين فينِتوكلاكس والدواء المضاد للأندروجين إنزالوتاميد إلى تأثيرات أقوى من أي دواء منهما بمفرده، بينما استمرت الأورام المستقلة عن الهرمونات في الاستجابة لحجب BCL-2 لوحده.
دلالات مبكرة من المرضى
لرؤية ما إذا كانت هذه الأفكار قد تُترجم إلى البشر، أجرى الباحثون تجربة مرحلة Ib صغيرة جمعت بين إنزالوتاميد وفينيتوكلاكس في رجال مصابين بسرطان البروستاتا المقاوم المتقدم. باستخدام جهاز لانتقاء الخلايا الورمية النادرة من الدم، تتبعوا BCL-2، والجينات المتعلقة بالهرمونات، وعلامة لعبء الخلايا الورمية عبر الزمن. أظهر بعض المرضى الذين استمروا في العلاج لدوائر علاجية عديدة انخفاضاً في إشارات BCL-2 والهرمونات في خلايا الأورام الدائرة لديهم، وتراجعاً في أعداد هذه الخلايا، وانخفاضات في مستوي PSA في الدم. في المقابل، كان لدى المرضى الذين لم يستفيدوا ميول لأن تكون مستويات BCL-2 لديهم منخفضة جداً في البداية ودلائل على أن مسار هرمون الإجهاد البديل قد بدأ يحل محله. على الرغم من أن هذه التجربة المبكرة كانت صغيرة وكانت مستويات الدواء محدودة بتداخلات بين الأدوية، فإنها تدعم فكرة أن الأورام المدفوعة بـ BCL-2 عرضة بشكل خاص لهذا النهج.
ماذا يعني هذا للمستقبل
يرسم هذا العمل صورة متماسكة: عندما تضغط علاجات حجب الهرمونات القوية على أورام البروستاتا، تشغّل العديد من الخلايا الناجية BCL-2 كطريق هروب مشترك. من خلال الجمع بين تصوير خلية بخلية مفصل، وتحليل جيني، وتجارب حيوانية، ودراسة سريرية تجريبية، يقدم المؤلفون حجة قوية بأن BCL-2 أكثر من مجرد مرافق — إنه مقبض بقاء مشترك عبر عدة نكهات من الأورام المقاومة. بالنسبة للمرضى، الوعد طويل الأمد هو استراتيجية أكثر تفصيلاً حيث يقيس الأطباء كل من حالة مستقبل الهرمون وBCL-2، ثم يطابقون الرجال الذين تعتمد أورامهم على هذا المفتاح بعلاجات تطفئه مباشرة.
الاستشهاد: Jamroze, A., Liu, X., Hou, S. et al. Single-cell imaging analysis, therapeutic modeling and a Phase Ib trial validate BCL-2 as a target across heterogeneous castration-resistant prostate cancer. Sig Transduct Target Ther 11, 161 (2026). https://doi.org/10.1038/s41392-026-02700-w
الكلمات المفتاحية: سرطان البروستاتا, مقاومة الأدوية, BCL-2, العلاج الهرموني, العلاج الموجه