Clear Sky Science · fr
Analyse par imagerie unicellulaire, modélisation thérapeutique et essai de phase Ib valident BCL-2 comme cible à travers l’hétérogénéité du cancer de la prostate résistant à la castration
Pourquoi cette recherche est importante
De nombreux hommes atteints d’un cancer de la prostate avancé finissent par atteindre un stade où les traitements standards visant à bloquer les hormones mâles cessent d’être efficaces. Cette étude pose une question simple mais urgente : lorsque les tumeurs apprennent à vivre sans hormones mâles, s’appuient‑elles toutes sur un « interrupteur de survie » commun que les cliniciens pourraient cibler ? En suivant des cellules cancéreuses individuelles, en testant des médicaments dans des modèles et en menant un essai clinique précoce, les chercheurs identifient un tel interrupteur — une protéine appelée BCL-2 — et montrent que le bloquer pourrait aider à traiter des maladies autrement résistantes.
Le problème des tumeurs prostatiques récalcitrantes
Les médicaments modernes qui inhibent les hormones mâles, ou bloquent leur récepteur, ont prolongé la vie de nombreux hommes. Pourtant, des milliers continuent de mourir chaque année d’un cancer de la prostate métastatique résistant à la castration, une forme qui progresse malgré ces traitements. Une raison clé est la diversité : au sein d’une même tumeur, certaines cellules dépendent fortement des signaux hormonaux, tandis que d’autres y font peu appel. Lorsqu’on administre des traitements anti‑hormonaux, les cellules sensibles meurent ou régressent, mais les plus résistantes survivent, s’adaptent et finissent par dominer. Les médecins ont longtemps supposé que ces survivantes s’appuient sur des programmes de survie de secours, mais on ignorait lesquels étaient partagés entre les différents types de tumeurs résistantes.
Repérer l’interrupteur de survie au niveau unicellulaire
L’équipe s’est concentrée sur BCL-2, une protéine qui aide les cellules à échapper à la mort programmée. À l’aide d’outils d’imagerie avancés capables de mesurer de nombreuses protéines dans des milliers de cellules simultanément, ils ont examiné des tissus prostatiques bénins, des tumeurs primaires non traitées et des tumeurs résistantes de patients, ainsi que plusieurs modèles murins. Dans les glandes saines, les récepteurs hormonaux et BCL-2 se trouvent principalement dans des couches cellulaires séparées. Dans les cancers non traités, la plupart des cellules présentent des récepteurs hormonaux forts mais peu de BCL-2. Après un blocage hormonal prolongé, toutefois, ce schéma s’inverse : les cancers résistants deviennent riches en cellules positives pour BCL-2, y compris des cellules qui conservent le récepteur hormonal et d’autres qui l’ont largement perdu. Dans plusieurs jeux de données, l’activité de BCL-2 augmentait à mesure que la signalisation hormonale diminuait, suggérant une relation de balancier étroite entre les deux.
Comment les signaux hormonaux contrôlent BCL-2
Pour comprendre le mécanisme, les chercheurs ont examiné comment le récepteur hormonal interagit avec le gène BCL-2. Dans des modèles de laboratoire, ils ont montré que lorsque les hormones sont présentes, le récepteur se lie physiquement à plusieurs sites proches du gène BCL-2 et le maintient réprimé. Lorsque les hormones sont retirées ou que le récepteur est bloqué par des médicaments, cette liaison disparaît, l’ADN local devient plus « ouvert » et les niveaux de BCL-2 augmentent. Ce schéma est apparu dans des types de tumeurs résistantes variés, y compris celles avec un niveau élevé de récepteur, un récepteur bas ou absent, ou un récepteur déplacé hors du noyau. Dans certains cas particuliers, d’autres facteurs comme des fragments altérés du récepteur ou le récepteur de la réponse au stress (GR) ont aussi influencé BCL-2, mais le thème central restait le même : l’arrêt de la signalisation hormonale normale retire un frein sur cette protéine de survie.
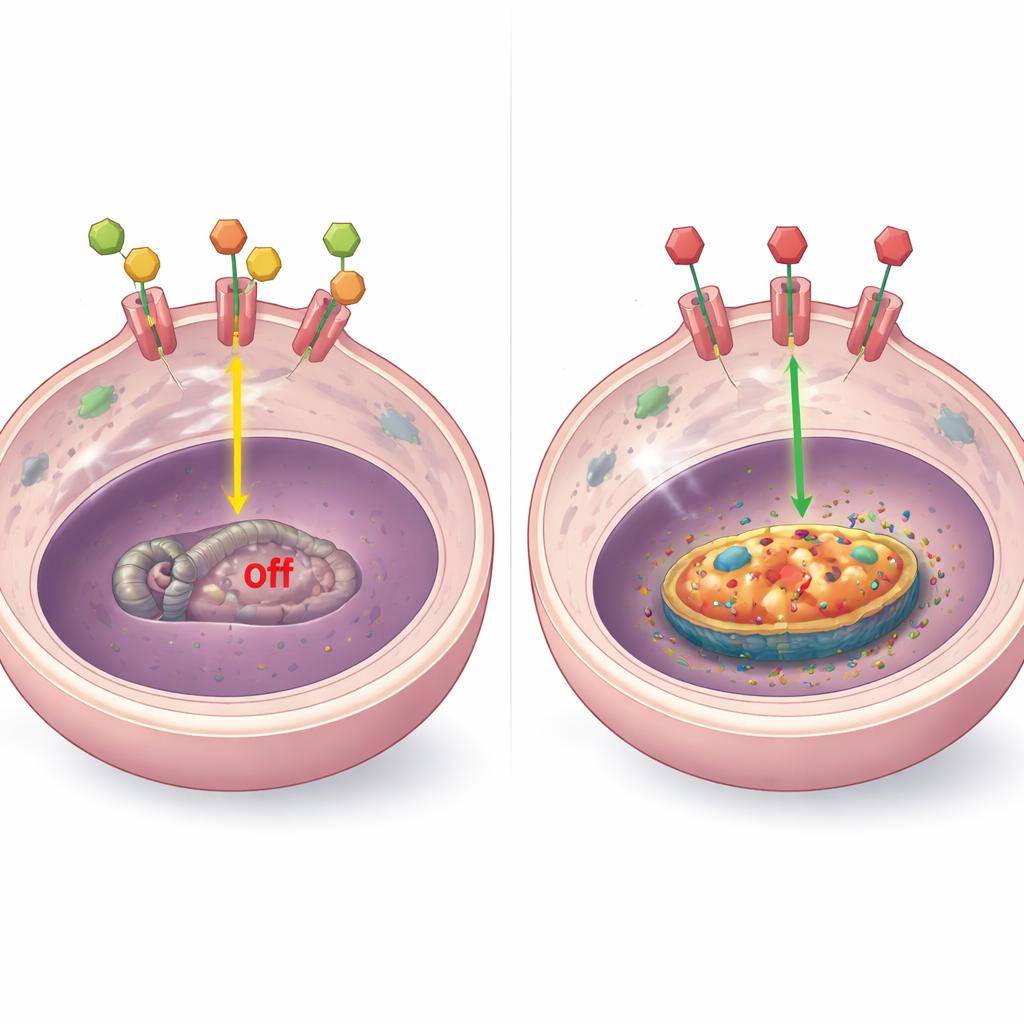
Tester BCL-2 comme point faible
Fort de cette compréhension, l’équipe a cherché à savoir si BCL-2 n’était qu’un marqueur de résistance ou une réelle faiblesse exploitable. Ils ont utilisé des organoïdes (mini‑tumeurs cultivées dans un gel) et des tumeurs murines représentant trois sous‑types résistants majeurs : ceux encore riches en récepteur hormonal nucléaire, ceux à récepteur faible, et ceux dont le récepteur est principalement cantonné au cytoplasme plutôt qu’au noyau. Dans les trois, le bloqueur de BCL-2 utilisé en clinique, le venetoclax (ABT‑199), a réduit les tumeurs ou ralenti leur croissance, souvent plus efficacement que les seuls traitements anti‑hormonaux. Dans les modèles conservant une certaine signalisation hormonale, l’association du venetoclax avec l’anti‑androgène enzalutamide a produit des effets plus marqués que chaque médicament isolé, tandis que les tumeurs indépendantes des hormones répondaient encore au blocage de BCL-2 seul.
Premiers indices chez les patients
Pour vérifier si ces idées pouvaient se traduire chez l’homme, les investigateurs ont mené un petit essai de phase Ib combinant enzalutamide et venetoclax chez des hommes atteints de cancer de la prostate avancé et résistant. En utilisant un dispositif pour trier les rares cellules tumorales circulantes dans le sang, ils ont suivi BCL-2, des gènes liés aux hormones et un marqueur de charge tumorale au fil du temps. Quelques patients restés sous traitement pendant de nombreux cycles ont montré une baisse de BCL-2 et des signaux hormonaux dans leurs cellules tumorales circulantes, une diminution du nombre de ces cellules et une baisse des taux de PSA sanguin. En revanche, les patients qui n’ont pas bénéficié du traitement avaient tendance à présenter un BCL-2 très faible dès le départ et des signes qu’une voie hormonale de stress alternative prenait le relais. Bien que cet essai précoce fût de petite taille et que les niveaux de médicament aient été limités par des interactions médicamenteuses, il soutient l’idée que les tumeurs pilotées par BCL-2 sont particulièrement vulnérables à cette approche.
Ce que cela signifie pour l’avenir
Ce travail dresse un tableau cohérent : lorsque des traitements anti‑hormonaux puissants exercent une pression sur les tumeurs prostatiques, de nombreuses cellules survivantes activent BCL-2 comme voie d’échappement commune. En combinant imagerie unicellulaire détaillée, analyses génétiques, expériences animales et une étude clinique pilote, les auteurs fournissent des arguments solides que BCL-2 n’est pas un simple spectateur — c’est une poignée de survie commune à plusieurs variantes de tumeurs résistantes. Pour les patients, la promesse à long terme est une stratégie plus personnalisée dans laquelle les cliniciens mesurent à la fois le statut du récepteur hormonal et de BCL-2, puis proposent aux hommes dont les tumeurs dépendent de cet interrupteur des traitements qui le désactivent directement.
Citation: Jamroze, A., Liu, X., Hou, S. et al. Single-cell imaging analysis, therapeutic modeling and a Phase Ib trial validate BCL-2 as a target across heterogeneous castration-resistant prostate cancer. Sig Transduct Target Ther 11, 161 (2026). https://doi.org/10.1038/s41392-026-02700-w
Mots-clés: cancer de la prostate, résistance aux médicaments, BCL-2, thérapie hormonale, thérapie ciblée