Clear Sky Science · de
Einzelzell-Bildgebungsanalyse, therapeutisches Modellieren und eine Phase-Ib-Studie bestätigen BCL-2 als Ziel bei heterogenem kastrationsresistentem Prostatakrebs
Warum diese Forschung wichtig ist
Viele Männer mit fortgeschrittenem Prostatakrebs erreichen schließlich einen Punkt, an dem die üblichen hormonblockierenden Medikamente nicht mehr wirken. Diese Studie stellt eine einfache, aber dringliche Frage: Wenn Tumoren lernen, ohne männliche Hormone zu überleben, verlassen sie sich dann alle auf denselben „Überlebensschalter“, den Ärzte anvisieren können? Durch das Verfolgen einzelner Krebszellen, das Testen von Wirkstoffen in Modellen und eine frühe klinische Studie identifizieren die Forschenden einen solchen Schalter — ein Protein namens BCL-2 — und zeigen, dass dessen Blockade helfen kann, sonst resistente Erkrankungen zu behandeln.
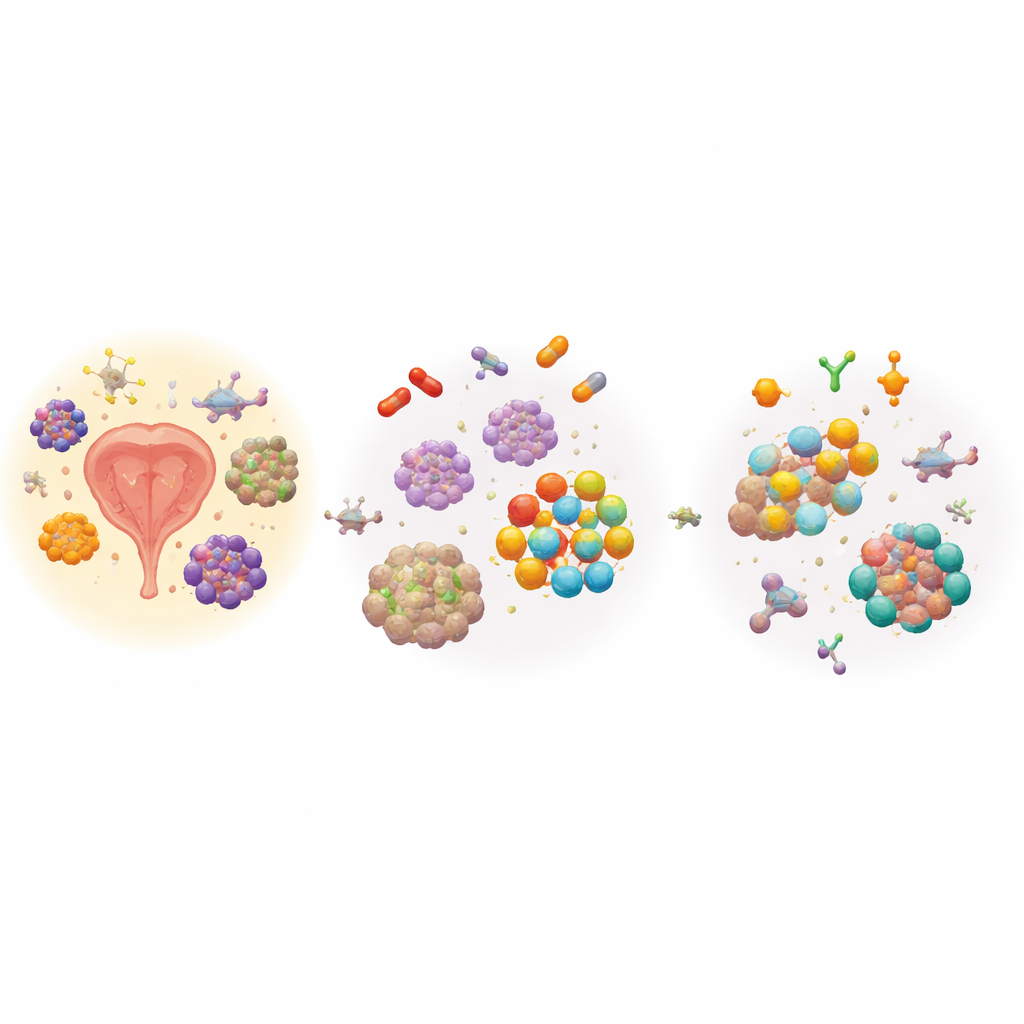
Das Problem hartnäckiger Prostatatumoren
Moderne Medikamente, die männliche Hormone unterdrücken oder ihren Rezeptor blockieren, haben vielen Männern das Leben verlängert. Dennoch sterben weiterhin Tausende jährlich an metastasiertem kastrationsresistentem Prostatakrebs, einer Form, die trotz dieser Behandlungen wächst. Ein wichtiger Grund ist Heterogenität: Innerhalb eines einzelnen Tumors sind einige Zellen stark auf Hormonsignale angewiesen, andere nutzen sie kaum. Wenn hormonblockierende Medikamente verabreicht werden, sterben oder schrumpfen die empfindlichen Zellen, während die widerstandsfähigeren überleben, sich anpassen und schließlich dominieren. Ärztinnen und Ärzte vermuteten lange, dass diese Überlebenden auf Ersatzprogramme zum Überleben bauen, doch es war unklar, welche Programme bei verschiedenen resistenten Tumortypen geteilt werden.
Den Überlebensschalter in Einzelzellen finden
Das Team konzentrierte sich auf BCL-2, ein Protein, das Zellen hilft, programmierter Zelltod zu entgehen. Mit fortschrittlichen Bildgebungswerkzeugen, die viele Proteine in tausenden Zellen gleichzeitig messen können, untersuchten sie gutartiges Prostatagewebe, unbehandelte Primärtumoren und resistente Tumoren von Patientinnen und Patienten sowie mehrere Mausmodelle. In gesunden Drüsen liegen Hormonrezeptoren und BCL-2 meist in getrennten Zellschichten. In unbehandelten Krebserkrankungen zeigen die meisten Zellen starke Hormonrezeptoren, aber wenig BCL-2. Nach langfristiger Hormonblockade kehrt sich dieses Muster jedoch um: Resistente Tumoren werden reich an BCL-2-positiven Zellen, einschließlich Zellen, die noch den Hormonrezeptor tragen, und solchen, die ihn weitgehend verloren haben. Über mehrere Datensätze hinweg stieg die BCL-2-Aktivität, während die Hormonsignalgebung fiel, was auf eine enge Kipppendel-Beziehung zwischen beiden hindeutet.
Wie Hormonsignale BCL-2 steuern
Um den Mechanismus zu verstehen, untersuchten die Forschenden, wie der Hormonrezeptor mit dem BCL-2-Gen interagiert. In Labormodellen fanden sie, dass der Rezeptor bei vorhandenen Hormonen physisch an mehrere Stellen in der Nähe des BCL-2-Gens bindet und dessen Aktivität dämpft. Werden Hormone entzogen oder der Rezeptor durch Medikamente blockiert, geht diese Bindung verloren, die lokale DNA wird „offener“ und die BCL-2-Spiegel steigen. Dieses Muster trat in verschiedenen resistenten Tumortypen auf, einschließlich solcher mit hohem Rezeptorniveau, niedrigem oder fehlendem Rezeptor und Rezeptor, der aus dem Zellkern verlagert ist. In einigen Sonderfällen beeinflussten auch andere Faktoren wie veränderte Rezeptorfragmente oder der Stressantwortrezeptor (GR) BCL-2, doch das zentrale Thema blieb: Das Abschalten normaler Hormonsignalwege entfernt eine Bremse dieses Überlebensproteins.
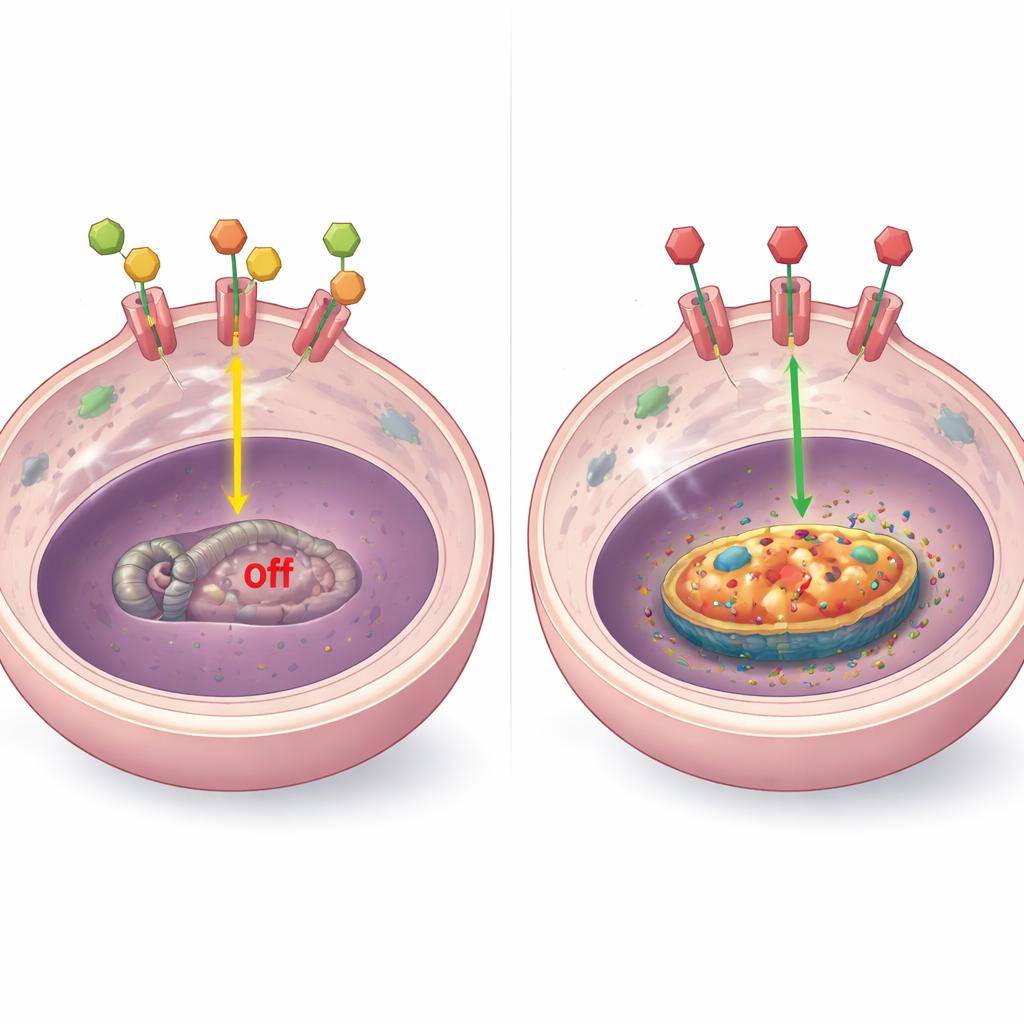
BCL-2 als Schwachstelle testen
Mithilfe dieser Erkenntnis prüfte das Team, ob BCL-2 nur ein Resistenzmarker oder eine tatsächlich ausnutzbare Schwachstelle ist. Sie verwendeten Organoide (Mini-Tumoren im Gel) und Maustumoren, die drei wichtige resistente Subtypen repräsentieren: solche mit noch reichlich nukleärem Hormonrezeptor, solche mit niedrigem Rezeptor und solche mit Rezeptor, der größtenteils im Zellkörper statt im Kern gefangen ist. In allen drei Typen verkleinerte oder verlangsamte der klinisch eingesetzte BCL-2-Blocker Venetoclax (ABT-199) die Tumoren häufig stärker als alleinige Hormonblockade. In Modellen mit noch vorhandener Hormonsignalgebung ergab die Kombination aus Venetoclax und dem Antiandrogen Enzalutamid stärkere Effekte als jedes Medikament allein, während hormonunabhängige Tumoren weiterhin auf alleinige BCL-2-Blockade ansprachen.
Frühe Hinweise von Patientinnen und Patienten
Um zu prüfen, ob sich diese Ideen auf Menschen übertragen lassen, führten die Forschenden eine kleine Phase-Ib-Studie durch, die Enzalutamid und Venetoclax bei Männern mit fortgeschrittenem resistentem Prostatakrebs kombinierte. Mit einem Verfahren zur Isolierung seltener Tumorzellen aus dem Blut verfolgten sie BCL-2, hormonbezogene Gene und einen Marker der Tumorzelllast über die Zeit. Einige Patientinnen und Patienten, die viele Zyklen auf der Therapie blieben, zeigten sinkende BCL-2- und Hormonsignale in ihren zirkulierenden Tumorzellen, eine Abnahme der Anzahl dieser Zellen und fallende PSA-Werte im Blut. Im Gegensatz dazu hatten nicht ansprechende Patientinnen und Patienten tendenziell von Beginn an sehr niedrige BCL-2-Werte und Anzeichen dafür, dass ein alternatives Stresshormonsignal den Ton angab. Obwohl diese frühe Studie klein war und die Medikamentenspiegel durch Wechselwirkungen begrenzt wurden, stützt sie die Idee, dass BCL-2-getriebene Tumoren besonders verwundbar für diesen Ansatz sind.
Was das für die Zukunft bedeutet
Diese Arbeit zeichnet ein stimmiges Bild: Wenn starke hormonblockierende Behandlungen auf Prostatatumoren einwirken, schalten viele überlebende Zellen BCL-2 als gemeinsamen Fluchtweg ein. Durch die Kombination detaillierter Einzelzellbildgebung, genetischer Analysen, Tierexperimente und einer Pilotklinischen Studie liefern die Autorinnen und Autoren stichhaltige Belege, dass BCL-2 mehr als ein Begleiter ist — es ist ein gemeinsamer Überlebensgriff über mehrere resistente Tumorvarianten hinweg. Für Patientinnen und Patienten liegt das langfristige Versprechen in einer gezielteren Strategie, bei der Ärzte sowohl Hormonrezeptor- als auch BCL-2-Status messen und Männer, deren Tumoren auf diesen Schalter angewiesen sind, gezielt mit Behandlungen ansprechen, die ihn direkt ausschalten.
Zitation: Jamroze, A., Liu, X., Hou, S. et al. Single-cell imaging analysis, therapeutic modeling and a Phase Ib trial validate BCL-2 as a target across heterogeneous castration-resistant prostate cancer. Sig Transduct Target Ther 11, 161 (2026). https://doi.org/10.1038/s41392-026-02700-w
Schlüsselwörter: Prostatakrebs, Medikamentenresistenz, BCL-2, Hormontherapie, zielgerichtete Therapie