Clear Sky Science · ja
ドキソルビシンは乳酸脱水素酵素Aを活性化して腫瘍随伴マクロファージの炎症性サイトカイン産生を促進する
がん薬を免疫増強剤に変える
膠芽腫は最も致命的な脳腫瘍の一つであり、その一因は腫瘍を免疫から隠す「友好的な」支持細胞の保護にあります。本研究は、長年使われてきた化学療法薬ドキソルビシンが、これらの支持細胞を目覚めさせ、腫瘍を保護する代わりに攻撃させるよう再利用できることを示しています。細胞の糖代謝の使い方を書き換えることで、静かで免疫抑制的な腫瘍のニッチを、より攻撃的で腫瘍に不利な環境へと変える助けとなります。
静かな腫瘍周辺の課題
標準的な膠芽腫治療—手術、放射線、テモゾロミド—は何十年にもわたり生存率を大きく改善していません。その主な理由の一つが腫瘍の局所環境、すなわち腫瘍微小環境で、ここには腫瘍随伴マクロファージやミクログリアと呼ばれる免疫関連細胞が豊富に存在します。これらの細胞は激しい防御者(炎症性の「戦闘員」)として働くことも、落ち着いて傷を修復する援助者(抑制的な「治癒者」)として働くこともあります。膠芽腫ではこれらが治癒者状態に強く偏り、免疫を抑制し腫瘍の治療抵抗性を助長します。著者らは、免疫応答を刺激することが知られている古典的な化学療法薬ドキソルビシンが、これらの細胞を戦闘員に再プログラムし、既存の治療の効果を高められるかを調べました。
マウスの延命と腫瘍の友好度の低下
膠芽腫マウスモデルを用いて、研究チームは放射線とテモゾロミドにドキソルビシンを組み合わせました。三剤併用を受けたマウスは放射線+テモゾロミドのみを受けた群より長く生存しましたが、腫瘍内の免疫様細胞の総数は変わりませんでした。変化したのはその挙動です。抑制的で腫瘍を助ける状態に関連するマーカーは低下し、活性化された抗腫瘍状態に関連するマーカーは上昇しました。同時に、IL‑6、TNF‑α、IL‑1βなどの炎症性メッセンジャー蛋白のレベルが腫瘍内、治療を受けたマウスの骨髄由来マクロファージ、そして血中で高くなっていました。これらの変化は、ドキソルビシンが単に免疫細胞を増やすのではなく、既存の細胞をより攻撃的で腫瘍に対抗するモードへ切り替えることを示しています。
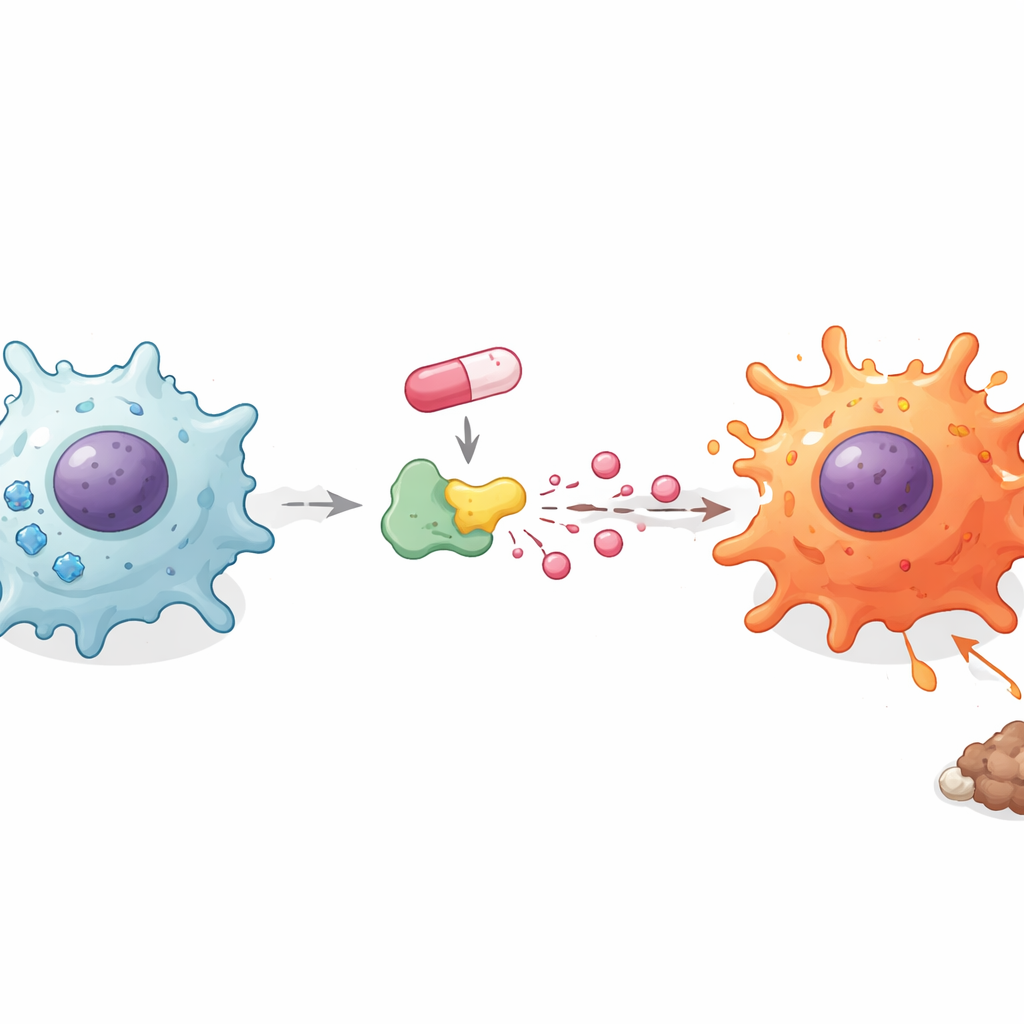
糖代謝と酸が免疫覚醒を駆動する仕組み
マクロファージは静的な状態と炎症状態の間で燃料の使い方を変えます。研究者たちはドキソルビシンがこの隠れた代謝層にどのように影響するかを探りました。驚くべきことに、薬は細胞の糖取り込みを全体的に増やしたわけではありませんが、糖の分解を標準的な阻害剤で遮断すると炎症性メッセンジャーの増加が失われました。これにより、細胞内に入った糖がその後どう処理されるかに注目が集まりました。ドキソルビシンは細胞のエネルギー貯蔵を低下させる一方で、周囲へ放出される乳酸の量を増加させていました。乳酸を単独で追加するとマクロファージやミクログリアはより多くの炎症性メッセンジャーを分泌し、乳酸輸送を遮断すると逆の効果が観察されました。これらの発見は、単なる糖消費ではなく、糖が乳酸へと変換される過程がマクロファージを戦闘員へ切り替えるのに重要であることを示唆しています。
薬の代謝レバーとしての重要な酵素
ドキソルビシンを乳酸産生により直接つなげるために、チームは糖分解生成物を乳酸に変える中心的酵素である乳酸脱水素酵素A(LDHA)を調べました。コンピュータシミュレーションはドキソルビシンが特定のアミノ酸に結合し得ることを示し、実験では処理後にマクロファージやミクログリアでLDH活性が上昇することが示されました。小分子阻害剤でLDHAを遮断したり遺伝学的手法で減少させると、ドキソルビシンはもはや高いレベルの炎症性メッセンジャーを駆動できませんでした。対照的に、LDHAを増強するとこれらのシグナルはより強くなりました。重要なのは、LDHAを阻害するとドキソルビシンが抑制的マーカーを除去し活性化マーカーを高める能力が部分的に逆転し、細胞のアイデンティティ変化がこの酵素制御の乳酸急増に結び付くことです。
患者にとっての意味
簡潔に言えば、この研究はドキソルビシンが腫瘍DNAを損傷する以上の作用を持つこと、すなわち近傍の支持細胞に代謝スイッチを押し、糖を乳酸へと処理させることで強力な炎症シグナルを生じさせることを明らかにしています。これによりマクロファージやミクログリアは腫瘍を守る側から攻撃する側へとシフトし、マウスでは放射線やテモゾロミドの効果を高めました。脳への安全なドキソルビシン送達などの課題は残るものの、本研究は腫瘍の周辺環境を免疫の避難所から戦場へ変える代謝標的の併用戦略が膠芽腫治療の新たな方向となり得ることを示しています。
引用: Liu, B., Yang, W., Feng, S. et al. Doxorubicin promotes the production of inflammatory cytokines in tumor-associated macrophages through activating lactate dehydrogenase A. Cell Death Discov. 12, 208 (2026). https://doi.org/10.1038/s41420-026-03014-0
キーワード: 膠芽腫, 腫瘍微小環境, 腫瘍随伴マクロファージ, ドキソルビシン, 乳酸代謝