Clear Sky Science · he
WTAP המתייצב על ידי USP7 תורם לעמידות לאנזאלוטמיד בסרטן הערמונית באמצעות תיווך שינוי m6A ב-AKT
מדוע חלק מסרטנים של הערמונית עוקפים תרופה מרכזית
אנזאלוטמיד היא גלולה נפוצה המשמשת לשליטה בסרטן הערמונית מתקדם על ידי השתקת אותות ההורמונים הזכרים שמזינים את תאי הגידול. רבים מהחולים מגיבים היטב בתחילה, אך עם הזמן הסרטן לעיתים קרובות לומד לגדול שוב למרות התרופה. מחקר זה חושף "טריק" מולקולרי שתאי הגידול משתמשים בו כדי להימלט מאנזאלוטמיד, ומצביע על דרכים חדשות שבהן ניתן לחסום נתיב בריחה זה.
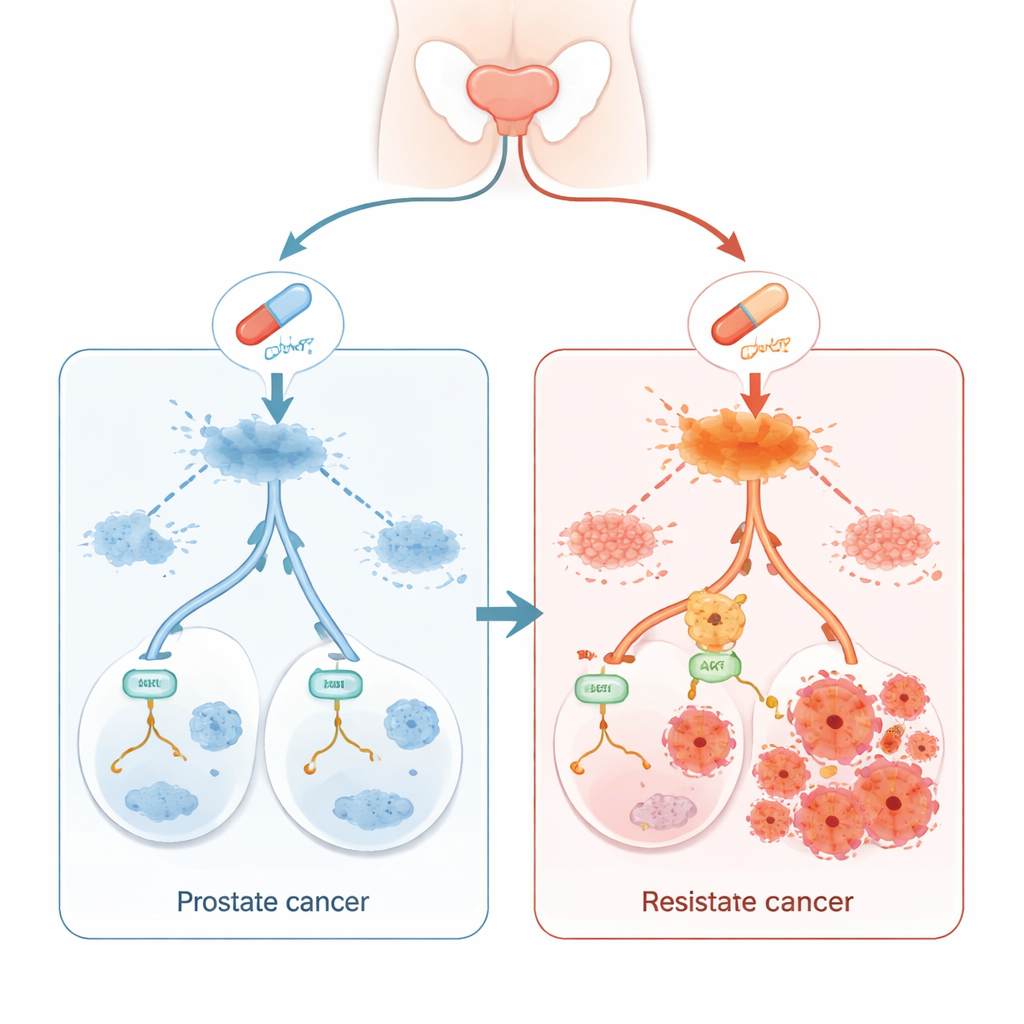
מסייע לגידול המתחבא במקום גלוי
החוקרים התמקדו בחלבון בשם WTAP, שמוכר כבר כמעורב בוויסות עיבוד המסרים הגנטיים בתוך התאים. בבחינת דגימות רקמה מ-60 גברים עם סרטן הערמונית והשוואתן לרקמה סמוכה שאינה סרטנית, הם מצאו שרמות WTAP היו גבוהות בעקביות בגידולים. כאשר הגבירו במחשבית את WTAP בתאי סרטן הערמונית שנגודלו במעבדה, התאים יצרו יותר קולוניות וכאשר הושתלו בעכברים ייצרו גידולים שגדלו מהר יותר. לעומת זאת, הורדת WTAP האטה את גדילת תאי הגידול. תוצאות אלה מראות כי WTAP פועל כמעודד גדילה בסרטן הערמונית.
כיצד אותות הורמונים מעצימים את המסייע הזה
סרטן הערמונית מונע במידה רבה על ידי קולטן האנדרוגן, חלבון החוש את הורמוני המין הזכריים ומדליק או מכבה גנים רבים. הצוות גילה כי WTAP עצמו הוא אחד הגנים הנשלטים על ידי קולטן זה. כאשר הפעילו את קולטן האנדרוגן באמצעות תרכובת הדומה להורמון, רמות WTAP עלו; כאשר חסמו או הפחיתו את הקולטן, WTAP ירד. ניסויי קשירה ל-DNA ודיווח מדוקדקים הראו שהקולטן יכול להיצמד ישירות לאזור הבקרה של גן WTAP ולשפר את ביטויו. במילים אחרות, אותות הורמונים סטנדרטיים מעודדים חלקית את גדילת הגידול על ידי העלאת WTAP.
כשחסימת ההורמונים כבר לא מספיקה
אנזאלוטמיד נועד להשקיט את קולטן האנדרוגן, ובשלבים המוקדמים של הטיפול הוא אכן מוריד את רמות WTAP. אך הסיפור משתנה בתאים עמידים לתרופה. בתאי סרטן ערמונית שנחשפו לאנזאלוטמיד במשך חודשים והפכו לעמידים, רמות WTAP שבהו והיו שוב גבוהות, אף על פי שאותות ההורמון נשארו חסומים. החוקרים עקבו אחר ההתהוות הזו ומצאו חלבון אחר, USP7, הפועל כמעין שומר ראש מולקולרי. בדרך כלל WTAP יכול להיות מסומן להשמדה ולהיות מפורק; בתאים העמידים USP7 נקשר ל-WTAP ומסיר את הסימונים הללו, מונע את פירוקו ומאפשר הצטברות WTAP. עיכוב USP7 הפחית את רמות WTAP והגביר את הסימונים הכימיים שמאותתים על פירוקו.
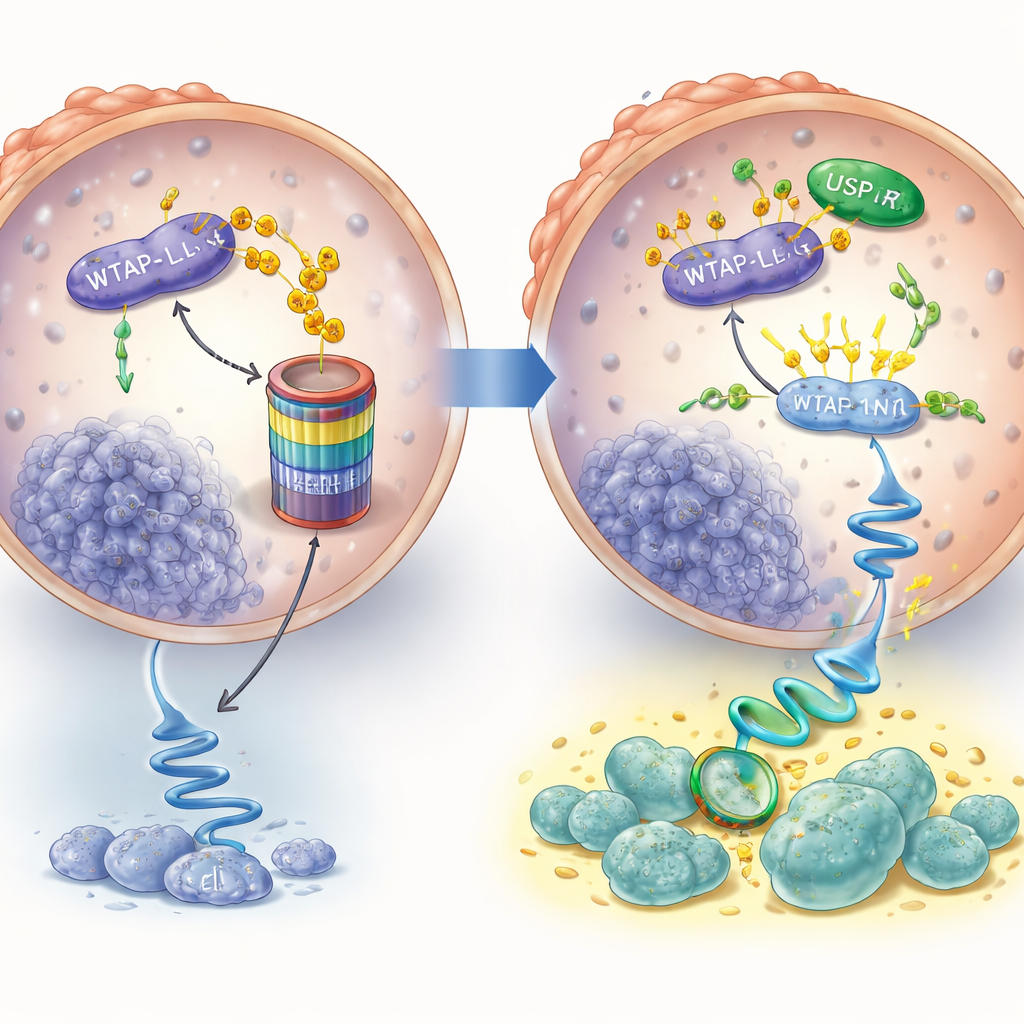
חיבור מחדש של המסרים שמפעיל מסלול הישרדות
רמות גבוהות של WTAP לא היו משמעותיות אילולא הן שינו את התנהגות תאי הסרטן. הצוות השתמש בניתוח RNA בקנה מידה גדול וגילה שמסלול מרכזי של גדילה והישרדות הנשלט על ידי חלבון בשם AKT היה פעיל במיוחד בתאים עמידים. הם הראו כי WTAP מסייע לשנות את המסר הגנטי של AKT באופן המייצב את המסר, כך שהתאים מייצרים יותר חלבון AKT. כאשר חסמו את WTAP או את אנזימי הפרטנרים שלו, רמות AKT ירדו והמסר דעך מהר יותר. מבחינה פונקציונלית, רמות נוספות של WTAP אפשרו לתאי סרטן להמשיך להתרבות גם בנוכחות אנזאלוטמיד, אך הוספת תרופה החוסמת AKT ביטלה את היתרון הזה. בדומה לכך, הפחתת WTAP או חסימת AKT הפכה את התאים העמידים לרגישים יותר לאנזאלוטמיד.
מה המשמעות עבור החולים
במבט כולל, העבודה מתארת שרשרת אירועים: תאי סרטן הערמונית מגבירים WTAP להזנת הגדילה; טיפול ארוך טווח באנזאלוטמיד מסיר את הבקרה ההורמונלית הראשונית על WTAP, אך תאים עמידים מפצים באמצעות USP7 המגן על WTAP מפירוק; בתמורה WTAP מסייע לייצוב מסרים שמגבירים את AKT, מתג הישרדות מרכזי, ומאפשר לגידולים להתעלם מהתרופה. עבור חולים, משמעות הדבר היא כי מדידת WTAP או USP7 עשויה לסייע בזיהוי סרטנים שסביר שיתנגדו לאנזאלוטמיד, וכי תרופות המכוונות ל-USP7 או ל-AKT, בשילוב עם טיפול חסימת הורמונים, עשויות להציע דרך עמידה יותר לשלוט בסרטן הערמונית המתקדם.
ציטוט: Shi, R., Gu, K., Li, H. et al. WTAP stabilized by USP7 contributes to enzalutamide resistance in prostate cancer via mediating AKT m6A-modification. Cancer Gene Ther 33, 277–288 (2026). https://doi.org/10.1038/s41417-026-01013-y
מילות מפתח: סרטן הערמונית, עמידות לתרופות, אנזאלוטמיד, אותות AKT, שינויי RNA