Clear Sky Science · ar
استقرار WTAP بواسطة USP7 يساهم في مقاومة الإنزالاتاميد في سرطان البروستاتا عبر التوسط في تعديل m6A لبروتين AKT
لماذا تتغلّب بعض سرطانات البروستاتا على دواء رئيسي
الإنزالاتاميد هو عقار شائع الاستخدام يساعد على السيطرة على سرطان البروستاتا المتقدم عن طريق تعطيل إشارات الهرمونات الذكرية التي تغذي خلايا الورم. يستجيب العديد من المرضى في البداية بشكل جيد، لكن مع مرور الوقت غالبًا ما يتعلم السرطان أن ينمو مجددًا بالرغم من الدواء. تكشف هذه الدراسة عن «خدعة» جزيئية تستخدمها خلايا الورم للهروب من الإنزالاتاميد، وتشير إلى طرق جديدة قد يحاول الأطباء بها سد هذا المسار الهروبي.
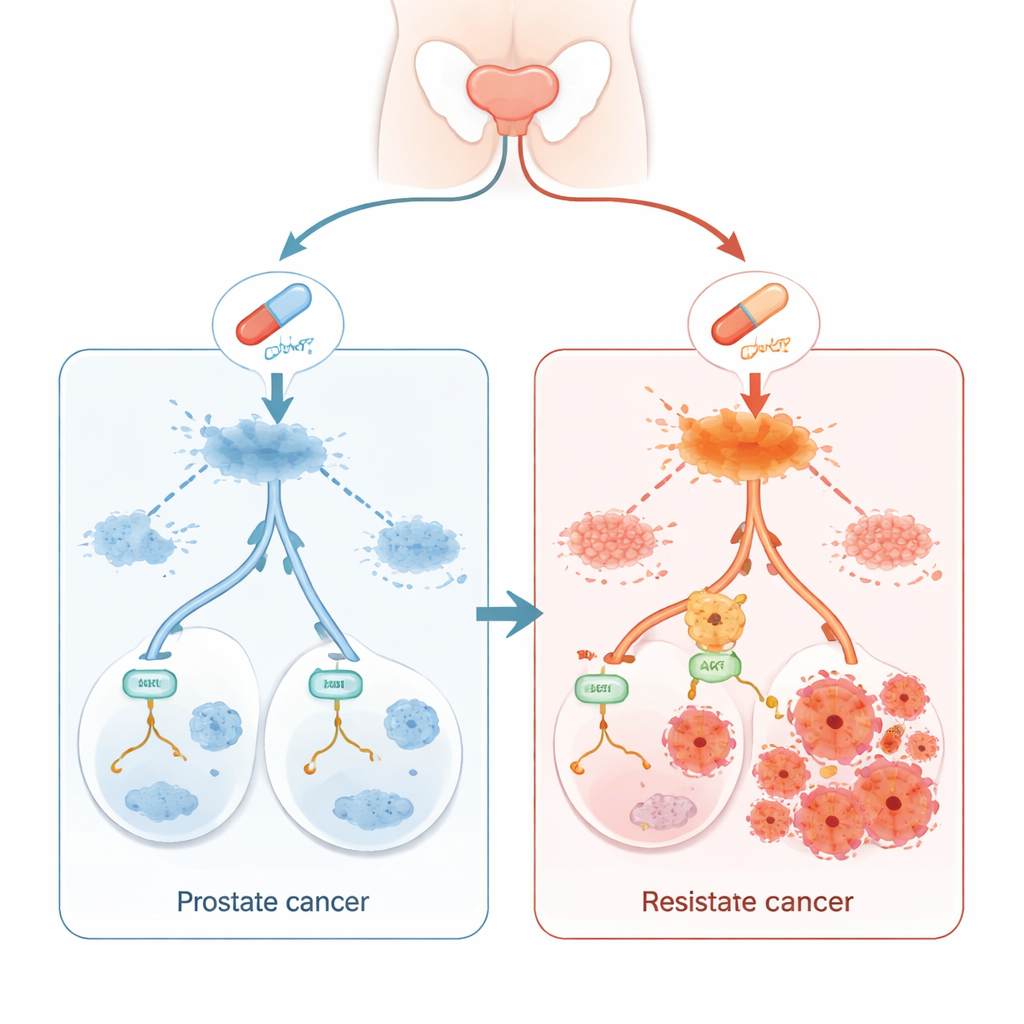
مساعد للنمو مخفي في العلن
ركز الباحثون على بروتين يدعى WTAP، المعروف بدوره في تنظيم كيفية معالجة الرسائل الجينية داخل الخلايا. من خلال فحص عينات نسيجية من 60 رجلاً مصابًا بسرطان البروستاتا ومقارنتها بالنسيج السليم المجاور، وجدوا أن مستويات WTAP كانت أعلى باستمرار في الأورام. عندما زادوا WTAP مصطنعًا في خلايا سرطان البروستاتا المزروعة في المختبر، شكلت الخلايا مستعمرات أكثر وعند زرعها في الفئران أنتجت أورامًا أسرع نموًا. وبالمقابل، أدى خفض WTAP إلى إبطاء نمو الخلايا الورمية. تظهر هذه النتائج أن WTAP يعمل كمساعد للنمو لسرطان البروستاتا.
كيف تعزّز إشارات الهرمونات هذا المساعد
يُدفع سرطان البروستاتا بقوة بواسطة مستقبل الأندروجين، وهو بروتين يستشعر الهرمونات الذكرية ويشغّل أو يوقف العديد من الجينات. اكتشف الفريق أن WTAP نفسه هو أحد الجينات التي يتحكم بها هذا المستقبل. عندما نشطوا مستقبل الأندروجين بمركب يشبه الهرمون ارتفعت مستويات WTAP؛ وعندما حجبوا أو قللوا نشاط المستقبل انخفض WTAP. أظهرت تجارب ربط الحمض النووي وتجارب المراسل أن المستقبل يمكنه الالتحام مباشرة بمنطقة التحكم في جين WTAP وزيادة تعبيره. بعبارة أخرى، تشجع إشارات الهرمونات التقليدية نمو الورم جزئيًا عن طريق رفع مستوى WTAP.
عندما لا تكفي معاوقة الهرمونات
صُمم الإنزالاتاميد لإسكات مستقبل الأندروجين، وفي المراحل المبكرة من العلاج يخفض بالفعل مستويات WTAP. لكن القصة تتغير في الخلايا المقاومة للدواء. في خلايا سرطان البروستاتا التي تعرّضت للإنزالاتاميد لأشهر وأصبحت مقاومة، تعافت مستويات WTAP وارتفعت مجددًا، رغم أن إشارات الهرمون كانت لا تزال محجوبة. تتبع الباحثون هذا الانتعاش إلى بروتين آخر، USP7، الذي يعمل كحارس جزيئي. عادة يمكن وضع علامة على WTAP للتخلص منه وتحطيمه؛ في الخلايا المقاومة يرتبط USP7 بـWTAP ويزيل هذه العلامات، مانعًا إتلافه ومتيحًا تراكمه. أدى تثبيط USP7 إلى خفض مستويات WTAP وزيادة العلامات الكيميائية التي تشير إلى تكسيره.
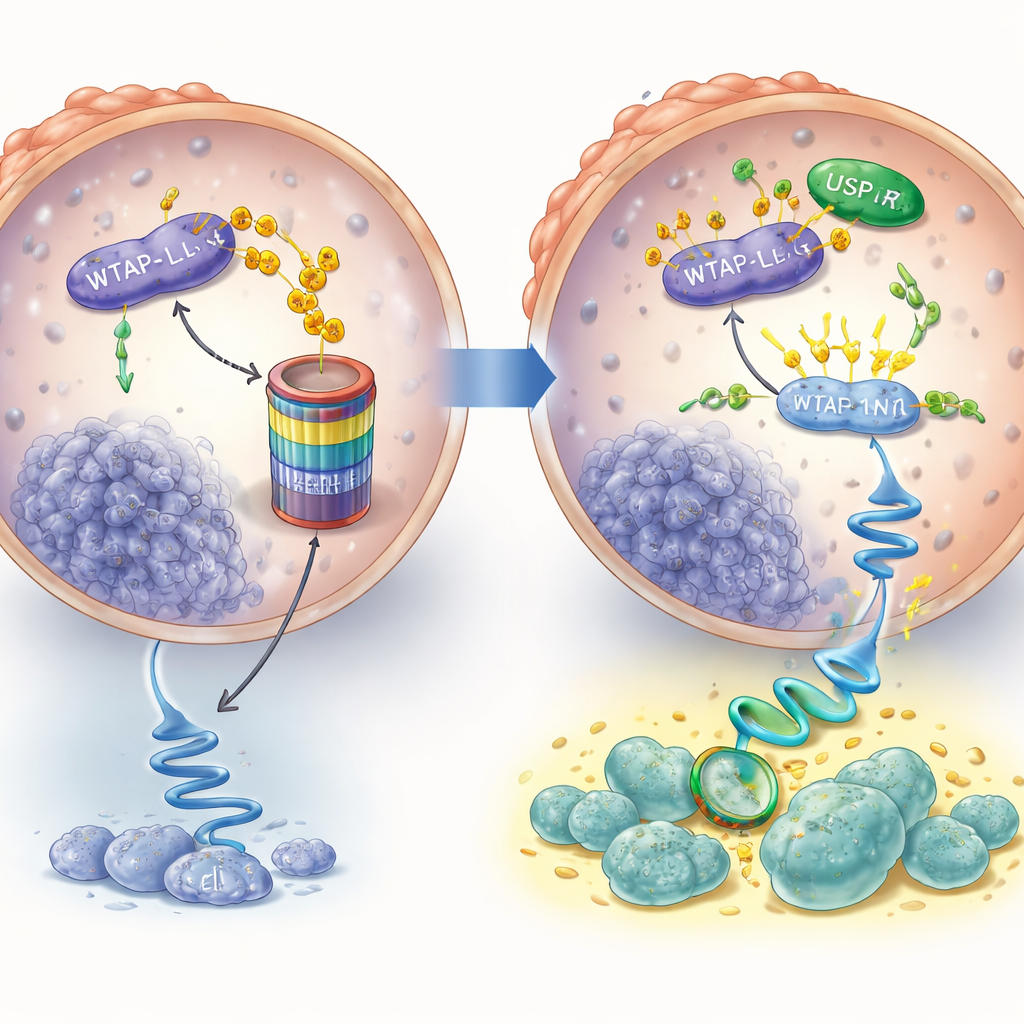
إعادة توصيل الرسائل لتشغيل مسار بقاء
لن يكون لارتفاع مستويات WTAP تأثير كبير ما لم يغيّر سلوك خلايا السرطان. استخدم الفريق تحليلاً واسع النطاق للحمض النووي الريبوزي ووجد أن مسارًا رئيسيًا للنمو والبقاء يتحكم بواسطة بروتين يدعى AKT كان نشطًا بشكل خاص في الخلايا المقاومة. أظهروا أن WTAP يساعد في تعديل الرسالة الجينية الخاصة بـAKT بطريقة تجعل هذه الرسالة أكثر استقرارًا، فتنتج الخلايا بروتين AKT بكميات أكبر. عندما تم تعطيل WTAP أو إنزيماته الشريكة انخفضت مستويات AKT وتلاشت الرسالة بشكل أسرع. وظيفيًا، سمح WTAP الزائد لخلايا السرطان بالاستمرار في التكاثر حتى في وجود الإنزالاتاميد، لكن إضافة دواء يثبط AKT محا هذه الميزة. بالمثل، جعل تقليل WTAP أو حجب AKT الخلايا المقاومة أكثر حساسية للإنزالاتاميد.
ماذا يعني ذلك للمرضى
مجتمعة، توضح هذه الدراسة سلسلة من الأحداث: ترفع خلايا سرطان البروستاتا WTAP لتغذية النمو؛ ومع العلاج طويل الأمد بالإنزالاتاميد يزول التحكم الهرموني الأولي في WTAP، لكن الخلايا المقاومة تعوّض ذلك باستخدام USP7 لحماية WTAP من التحلل؛ بدوره يساعد WTAP في تثبيت الرسائل التي تعزز AKT، وهو مفتاح بقاء الخلايا، مما يسمح للأورام بتجاهل الدواء. بالنسبة للمرضى، يوحي ذلك بأن قياس WTAP أو USP7 قد يساعد في تحديد الأورام المرجَّح أن تقاوم الإنزالاتاميد، وأن الأدوية المستهدفة لـUSP7 أو AKT، بالاشتراك مع العلاج المعطل للهرمونات، قد توفر وسيلة أكثر متانة للتحكم في سرطان البروستاتا المتقدم.
الاستشهاد: Shi, R., Gu, K., Li, H. et al. WTAP stabilized by USP7 contributes to enzalutamide resistance in prostate cancer via mediating AKT m6A-modification. Cancer Gene Ther 33, 277–288 (2026). https://doi.org/10.1038/s41417-026-01013-y
الكلمات المفتاحية: سرطان البروستاتا, مقاومة الأدوية, إنزالاتاميد, إشارات AKT, تعديل الحمض النووي الريبوزي