Clear Sky Science · de
WTAP, stabilisiert durch USP7, trägt zur Enzalutamid‑Resistenz beim Prostatakrebs bei, indem es die m6A‑Modifikation von AKT vermittelt
Warum manche Prostatakrebse ein wichtiges Medikament austricksen
Enzalutamid ist eine weit verbreitete Tablette, die fortgeschrittenen Prostatakrebs kontrolliert, indem sie die männlichen Hormonsignale abschaltet, die Tumorzellen nähren. Viele Patientinnen und Patienten sprechen anfangs gut darauf an, doch im Laufe der Zeit lernt der Krebs häufig, trotz des Medikaments wieder zu wachsen. Diese Studie deckt einen molekularen „Trick“ auf, den Tumorzellen zur Umgehung von Enzalutamid nutzen, und zeigt mögliche neue Ansätze, wie man diese Fluchtroute blockieren könnte.
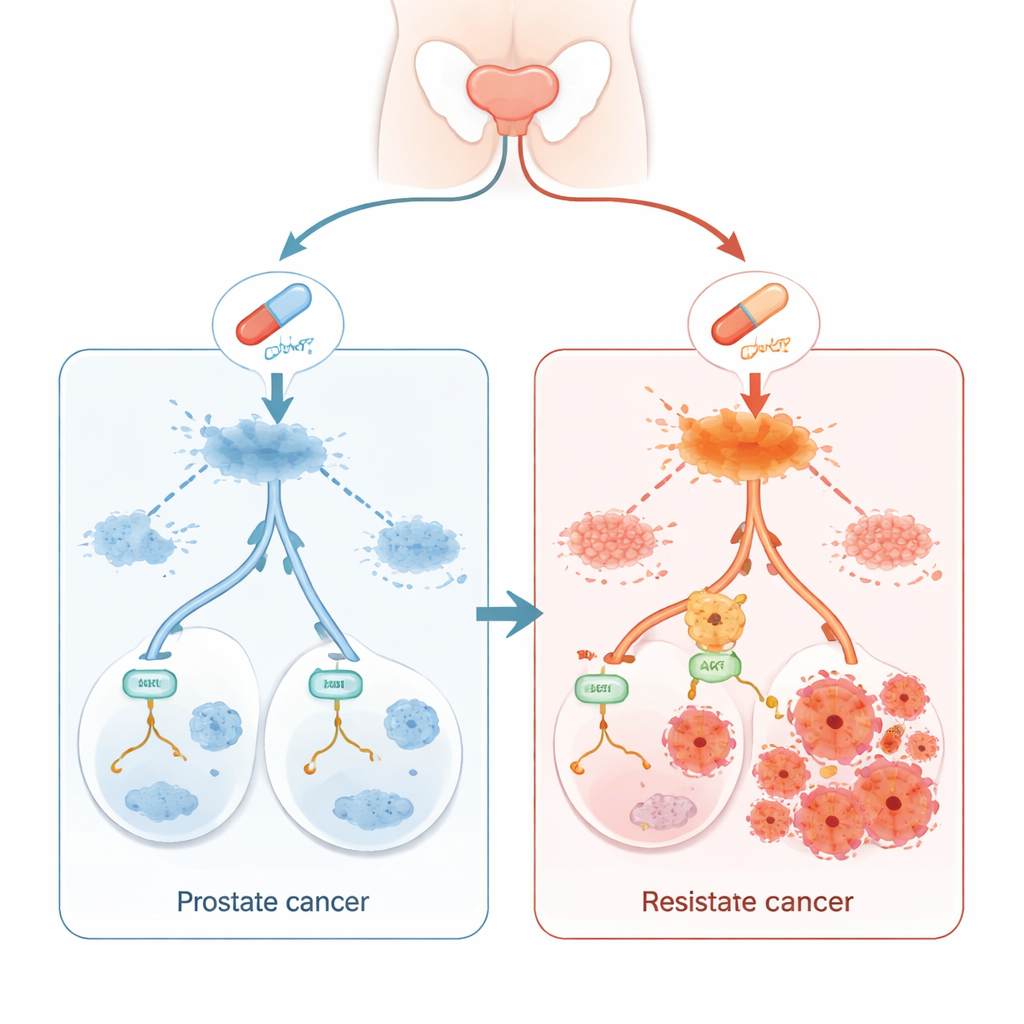
Ein Wachstumshelfer, der offen sichtbar ist
Die Forschenden konzentrierten sich auf ein Protein namens WTAP, das bereits dafür bekannt ist, an der Regulierung der Verarbeitung genetischer Botschaften innerhalb der Zellen beteiligt zu sein. Durch die Untersuchung von Gewebeproben von 60 Männern mit Prostatakrebs und dem Vergleich mit angrenzendem nicht‑tumoralem Gewebe stellten sie fest, dass die WTAP‑Spiegel in den Tumoren durchgängig erhöht waren. Wenn sie WTAP in im Labor gezüchteten Prostatakrebszellen künstlich erhöhten, bildeten die Zellen mehr Kolonien und erzeugten bei Implantation in Mäuse schneller wachsende Tumore. Umgekehrt verlangsamte das Herunterregeln von WTAP das Tumorzellwachstum. Diese Ergebnisse zeigen, dass WTAP als Wachstumsunterstützer für Prostatakrebs wirkt.
Wie Hormonsignale diesen Wachstumshelfer ankurbeln
Prostatakrebs wird stark vom Androgenrezeptor getrieben, einem Protein, das männliche Hormone wahrnimmt und viele Gene an‑ oder abschaltet. Das Team entdeckte, dass WTAP selbst eines der vom Rezeptor gesteuerten Gene ist. Wenn sie den Androgenrezeptor mit einer hormonähnlichen Verbindung aktivierten, stiegen die WTAP‑Spiegel; wenn sie den Rezeptor blockierten oder reduzierten, sanken die WTAP‑Spiegel. Detaillierte DNA‑Bindungs‑ und Reporter‑Experimente zeigten, dass der Rezeptor direkt an die Kontrollregion des WTAP‑Gens binden und dessen Aktivität erhöhen kann. Mit anderen Worten: Übliche Hormonsignale fördern das Tumorwachstum zum Teil durch Erhöhung von WTAP.
Wenn das Blockieren von Hormonen nicht mehr ausreicht
Enzalutamid ist darauf ausgelegt, den Androgenrezeptor zu stilllegen, und zu Beginn der Behandlung senkt es tatsächlich die WTAP‑Spiegel. Doch die Situation ändert sich in medikamentenresistenten Zellen. In Prostatakrebszellen, die über Monate Enzalutamid ausgesetzt waren und resistent wurden, erholten sich die WTAP‑Spiegel und waren wieder hoch, obwohl die Hormonsignale weiterhin blockiert waren. Die Forschenden führten diese Erholung auf ein anderes Protein namens USP7 zurück, das wie ein molekularer Bodyguard wirkt. Normalerweise kann WTAP für den Abbau markiert und zersetzt werden; in den resistenten Zellen bindet USP7 an WTAP und entfernt diese Markierungen, verhindert somit dessen Abbau und erlaubt die Anreicherung von WTAP. Die Hemmung von USP7 reduzierte WTAP‑Spiegel und erhöhte die chemischen Markierungen, die WTAP zum Abbau kennzeichnen.
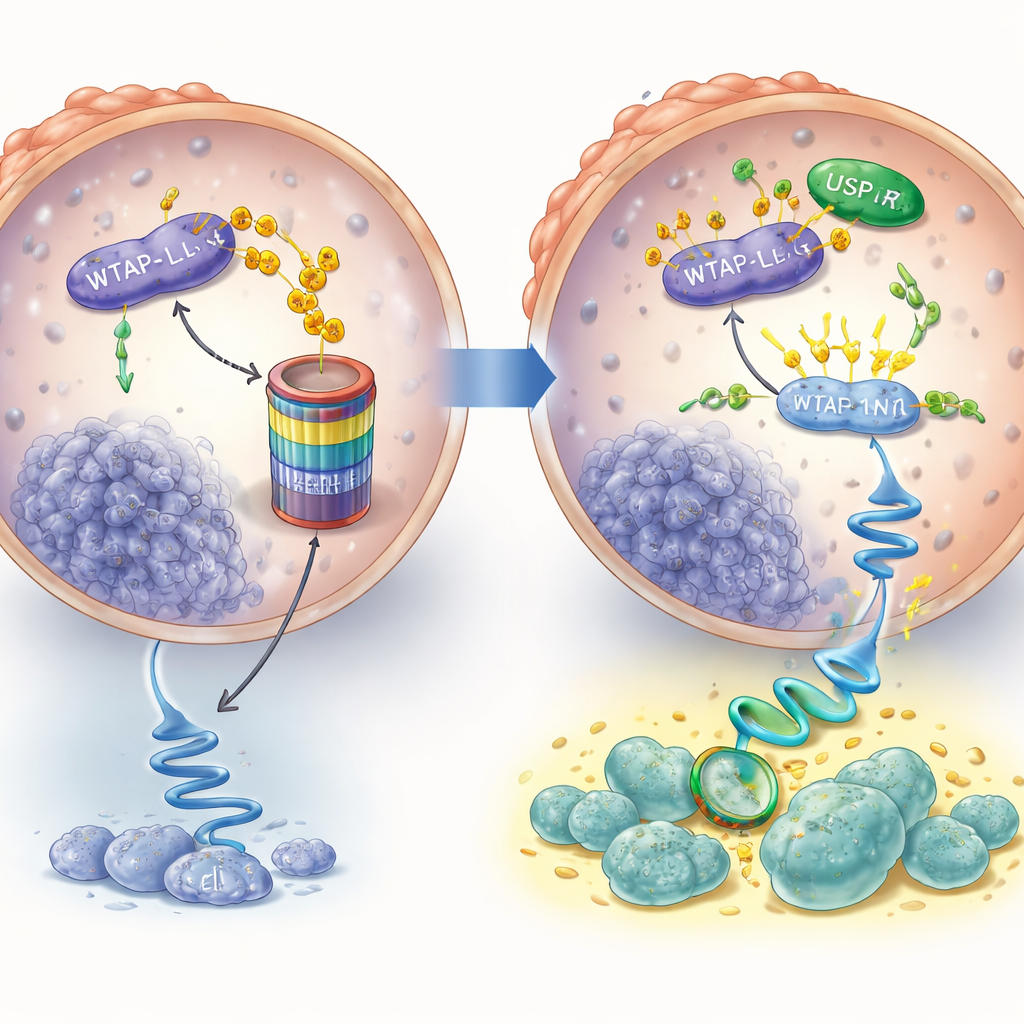
Umschalten von Botschaften, um einen Überlebensweg einzuschalten
Hohe WTAP‑Spiegel wären wenig bedeutend, wenn sie das Verhalten der Krebszellen nicht veränderten. Das Team nutzte groß angelegte RNA‑Analysen und fand, dass ein wichtiger Wachstums‑ und Überlebensweg, gesteuert durch ein Protein namens AKT, in den resistenten Zellen besonders aktiv war. Sie zeigten, dass WTAP dabei hilft, die genetische Botschaft für AKT so zu modifizieren, dass diese Botschaft stabiler wird, wodurch die Zellen mehr AKT‑Protein produzieren. Wenn WTAP oder seine Partnerenzyme blockiert wurden, sanken die AKT‑Spiegel und die Botschaft zerfiel schneller. Funktionell erlaubte zusätzliches WTAP den Krebszellen, sich weiter zu vermehren, selbst in Gegenwart von Enzalutamid, doch die Zugabe eines AKT‑blockierenden Medikaments beseitigte diesen Vorteil. In ähnlicher Weise machten das Reduzieren von WTAP oder das Blockieren von AKT resistente Zellen empfindlicher gegenüber Enzalutamid.
Was das für Patientinnen und Patienten bedeutet
Zusammengefasst skizziert die Arbeit eine Ereigniskette: Prostatakrebszellen erhöhen WTAP, um Wachstum zu fördern; eine langfristige Enzalutamid‑Behandlung beseitigt die anfängliche hormonelle Kontrolle über WTAP, aber resistente Zellen kompensieren dies, indem sie USP7 nutzen, um WTAP vor dem Abbau zu schützen; wiederum hilft WTAP, Botschaften zu stabilisieren, die AKT, einen zentralen Überlebensschalter, steigern, sodass Tumore das Medikament ignorieren. Für Patientinnen und Patienten legt dies nahe, dass die Messung von WTAP oder USP7 helfen könnte, Tumore zu identifizieren, die wahrscheinlich gegen Enzalutamid resistent werden, und dass Arzneimittel, die USP7 oder AKT gezielt hemmen, kombiniert mit hormonblockierenden Therapien, eine dauerhaftere Möglichkeit bieten könnten, fortgeschrittenen Prostatakrebs in Schach zu halten.
Zitation: Shi, R., Gu, K., Li, H. et al. WTAP stabilized by USP7 contributes to enzalutamide resistance in prostate cancer via mediating AKT m6A-modification. Cancer Gene Ther 33, 277–288 (2026). https://doi.org/10.1038/s41417-026-01013-y
Schlüsselwörter: Prostatakrebs, Medikamentenresistenz, Enzalutamid, AKT‑Signalweg, RNA‑Modifikation