Clear Sky Science · fr
H3K4me1 dirige le dépôt de H3K36me2 et H3K36me3 chez les plantes terrestres
Comment les plantes se souviennent et réagissent
Les plantes ne peuvent pas fuir la sécheresse, la chaleur ou les saisons changeantes. Elles s’appuient plutôt sur une couche cachée de marques chimiques sur leurs protéines empaquetant l’ADN pour ajuster finement quels gènes s’activent ou se désactivent. Cette étude révèle comment une de ces marques chez les plantes terrestres agit comme un panneau moléculaire, aidant à positionner une autre marque qui façonne la croissance, le moment de la floraison et les réponses à l’environnement.

Un code écrit sur l’emballage de l’ADN
Dans chaque cellule végétale, l’ADN est enroulé autour de protéines appelées histones, formant des structures en perles le long du fil génétique. Ces histones portent de petits tags chimiques qui, ensemble, forment un code pour l’activité des gènes. L’équipe s’est concentrée sur deux de ces marques sur l’histone H3, connues sous les noms H3K4me1 et H3K36me2/3. Chez les animaux, H3K4me1 est célèbre pour marquer des régions d’ADN qui stimulent l’activité des gènes, appelées enhancers. Mais chez les plantes, son rôle restait énigmatique. En comparant algues, mousses, plantes à fleurs, levures, drosophiles, souris et humains, les chercheurs ont montré que les plantes terrestres présentent un motif distinct : H3K4me1 s’étend le long des corps de gènes et présente une relation unique avec l’intensité d’expression des gènes.
Une protéine lecteur qui repère la première marque
Les marques chimiques sur les histones n’ont d’effet que si d’autres protéines peuvent les « lire ». Les scientifiques ont cherché dans les génomes végétaux des protéines contenant une unité de lecture particulière appelée doigt PHD, connue pour reconnaître les modifications de H3K4. Ils se sont concentrés sur une protéine de riz nommée Early heading date 3 (Ehd3), déjà connue pour influencer la floraison. Des tests biochimiques utilisant des fragments d’histones artificiels ont montré qu’Ehd3 préfère fortement H3K4me1 aux autres marques apparentées. Des travaux structuraux à haute résolution ont ensuite expliqué pourquoi : Ehd3 utilise une paire de doigts PHD étroitement liés pour former une poche mince qui accueille un seul groupe méthyle sur la lysine 4, mais entrerait en conflit avec des versions plus volumineuses. Cette conception inhabituelle à double poche rend Ehd3 très sélective pour H3K4me1.
Du lecteur à la réécriture du code
La question suivante était ce qui se passe après qu’Ehd3 se lie à H3K4me1 sur la chromatine. Grâce à des expériences d’interaction protéique dans le riz, l’équipe a découvert qu’Ehd3 s’associe physiquement à SDG724, une enzyme qui ajoute des groupes méthyle à une autre position de l’histone H3, générant H3K36me2 et H3K36me3. Les plantes dépourvues d’Ehd3 ou de SDG724 fleurissaient tard et montraient des changements similaires dans l’activité génétique à l’échelle du génome. Le cartographie des marques d’histones a révélé que la perte d’Ehd3 ou de SDG724 laisse H3K4me1 globalement intacte mais réduit fortement H3K36me2/3 sur les gènes affectés. Dans des essais in vitro, SDG724 montrait peu d’activité seule, mais fonctionnait bien mieux sur des nucléosomes marqués par H3K4me1 lorsque Ehd3 était présent, indiquant qu’Ehd3 non seulement amène SDG724 au bon endroit mais en renforce aussi le pouvoir catalytique.
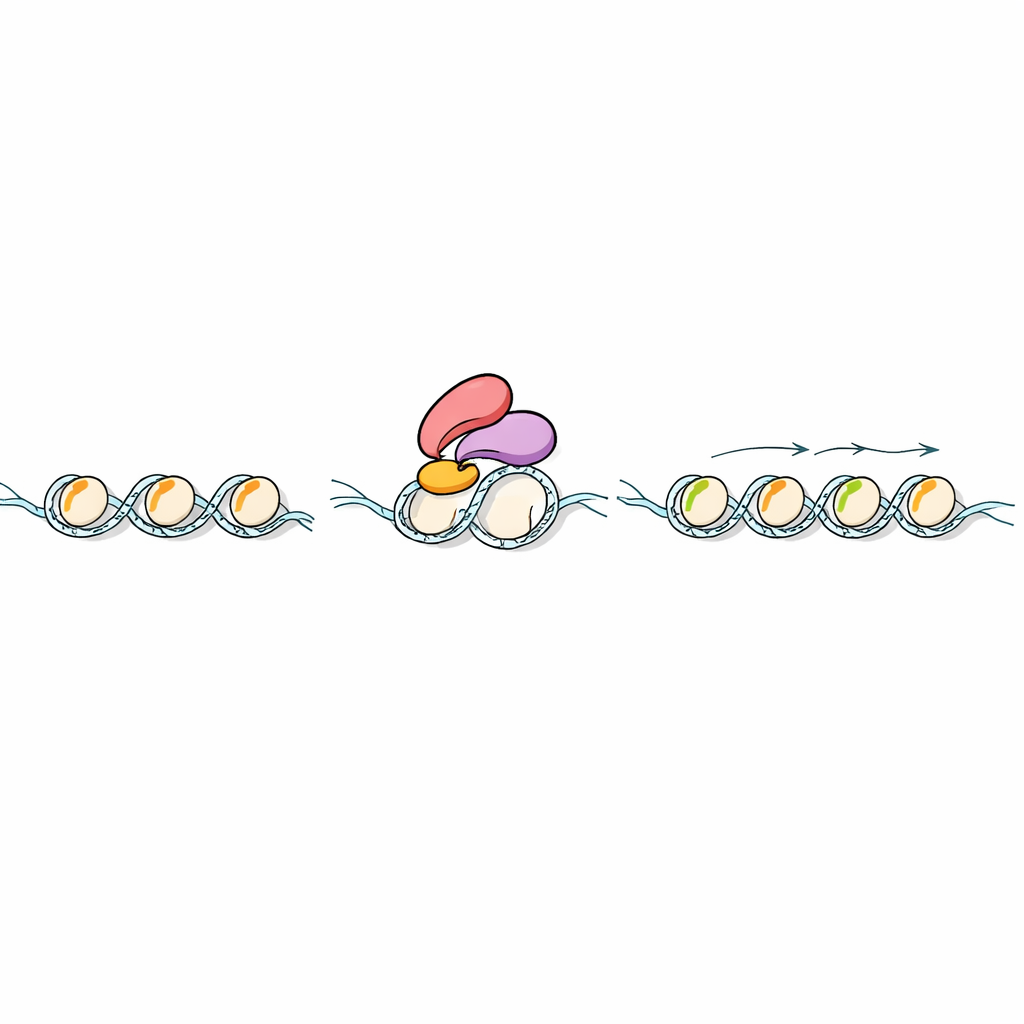
Un fil évolutif à travers les plantes terrestres
Les chercheurs ont étendu leur analyse au-delà du riz. Ils ont montré que des homologues proches d’Ehd3 chez d’autres plantes terrestres partagent des structures de doigts PHD similaires et, dans de nombreux cas, la même préférence pour H3K4me1. Des données à l’échelle du génome provenant de mousse, Arabidopsis, riz et d’autres espèces ont révélé un motif récurrent : partout où H3K4me1 se trouve le long des gènes, H3K36me2 et H3K36me3 ont tendance à se localiser dans les mêmes régions. Ce couplage étroit est beaucoup plus faible ou absent chez les algues et les animaux, ce qui suggère qu’à mesure que les plantes ont colonisé la terre ferme, elles ont évolué un lecteur dédié de H3K4me1 pour aider à établir la méthylation de H3K36. Le résultat est un système de marquage intégré qui aide probablement les plantes à régler la transcription pendant le développement et en situation de stress.
Pourquoi ce système caché est important
Pour les non-spécialistes, le message clé est que les plantes utilisent un code chimique à plusieurs couches sur leurs protéines empaquetant l’ADN pour coordonner l’activité des gènes. Ce travail montre qu’une marque, H3K4me1, sert de signal de départ qui recrute une protéine lectrice, Ehd3, laquelle active à son tour une enzyme pour installer une seconde marque, H3K36me2/3, le long des gènes. Ensemble, ces marques liées influencent la croissance des plantes, le moment de la floraison et les réponses au stress. Comprendre cette chaîne d’évènements ouvre des pistes pour sélectionner ou concevoir des cultures mieux adaptées aux environnements changeants en modulant la façon dont elles lisent et réécrivent leur propre code de chromatine.
Citation: Wu, J., Wang, J., Du, K. et al. H3K4me1 directs H3K36me2 and H3K36me3 deposition in land plants. Nat Commun 17, 2831 (2026). https://doi.org/10.1038/s41467-026-69632-5
Mots-clés: épigénétique végétale, méthylation des histones, régulation de la chromatine, moment de floraison, gènes réagissant au stress