Clear Sky Science · de
H3K4me1 steuert die Ablagerung von H3K36me2 und H3K36me3 in Landpflanzen
Wie Pflanzen sich merken und reagieren
Pflanzen können vor Dürre, Hitze oder wechselnden Jahreszeiten nicht fliehen. Stattdessen nutzen sie eine verborgene Schicht chemischer Markierungen an ihren DNA-verpackenden Proteinen, um fein zu steuern, welche Gene an- oder abgeschaltet werden. Diese Studie zeigt, wie eine solche Markierung in Landpflanzen wie ein molekulares Wegweisschild wirkt und hilft, eine andere Markierung zu platzieren, die Wachstum, Blühverhalten und Umweltreaktionen prägt.

Ein Code auf der DNA-Verpackung
In jeder Pflanzenzelle ist die DNA um Proteine namens Histone gewickelt und bildet Perlen-ähnliche Strukturen entlang des genetischen Fadens. An diesen Histonen sitzen winzige chemische Anhängsel, die zusammen wie ein Code für Genaktivität wirken. Das Team konzentrierte sich auf zwei dieser Markierungen auf Histon H3, kurz H3K4me1 und H3K36me2/3 genannt. Bei Tieren ist H3K4me1 bekannt dafür, Bereiche zu markieren, die die Genaktivität steigern (Enhancer). In Pflanzen aber war seine Rolle rätselhaft. Durch den Vergleich von Algen, Moosen, Blütenpflanzen, Hefe, Fliegen, Mäusen und Menschen zeigten die Forschenden, dass Landpflanzen ein charakteristisches Muster aufweisen: H3K4me1 breitet sich über Genkörper in Pflanzen aus und zeigt eine spezielle Beziehung zur Genexpressionsstärke.
Ein Leserprotein, das die erste Markierung erkennt
Chemische Markierungen auf Histonen sind nur dann relevant, wenn andere Proteine sie „lesen“ können. Die Wissenschaftler suchten in Pflanzengenomen nach Proteinen mit einer bestimmten Leser-Einheit, dem PHD-Finger, der für die Erkennung von H3K4-Modifikationen bekannt ist. Sie konzentrierten sich auf ein Reisprotein namens Early heading date 3 (Ehd3), das bereits als Einflussfaktor für die Blütezeit bekannt war. Biochemische Tests mit künstlichen Histonteilen zeigten, dass Ehd3 H3K4me1 deutlich gegenüber verwandten Markierungen bevorzugt. Hochauflösende Strukturuntersuchungen erklärten anschließend warum: Ehd3 nutzt ein Paar eng verbundener PHD-Finger, die eine enge Tasche bilden, die genau eine Methylgruppe an Lysin 4 aufnimmt, während größere Varianten räumlich stören würden. Dieses ungewöhnliche Doppel-Taschen-Design macht Ehd3 hochselektiv für H3K4me1.
Vom Lesen zum Umschreiben des Codes
Die nächste Frage war, was passiert, nachdem Ehd3 H3K4me1 auf dem Chromatin bindet. Mit „Proteinangel“-Experimenten in Reis fanden die Forschenden, dass Ehd3 physisch mit SDG724 assoziiert, einem Enzym, das Methylgruppen an einer anderen Position von Histon H3 anbringt und H3K36me2 sowie H3K36me3 erzeugt. Pflanzen ohne Ehd3 oder SDG724 blühten spät und zeigten ähnliche Veränderungen der Genaktivität im gesamten Genom. Kartierungen der Histonmarken ergaben, dass der Verlust von Ehd3 oder SDG724 H3K4me1 weitgehend unberührt lässt, aber H3K36me2/3 über betroffenen Genen stark reduziert. In Reagenzglasversuchen zeigte SDG724 alleine nur geringe Aktivität, arbeitete jedoch deutlich besser an H3K4me1-markierten Nukleosomen, wenn Ehd3 vorhanden war, was darauf hindeutet, dass Ehd3 nicht nur SDG724 an den richtigen Ort bringt, sondern auch seine katalytische Leistung steigert.
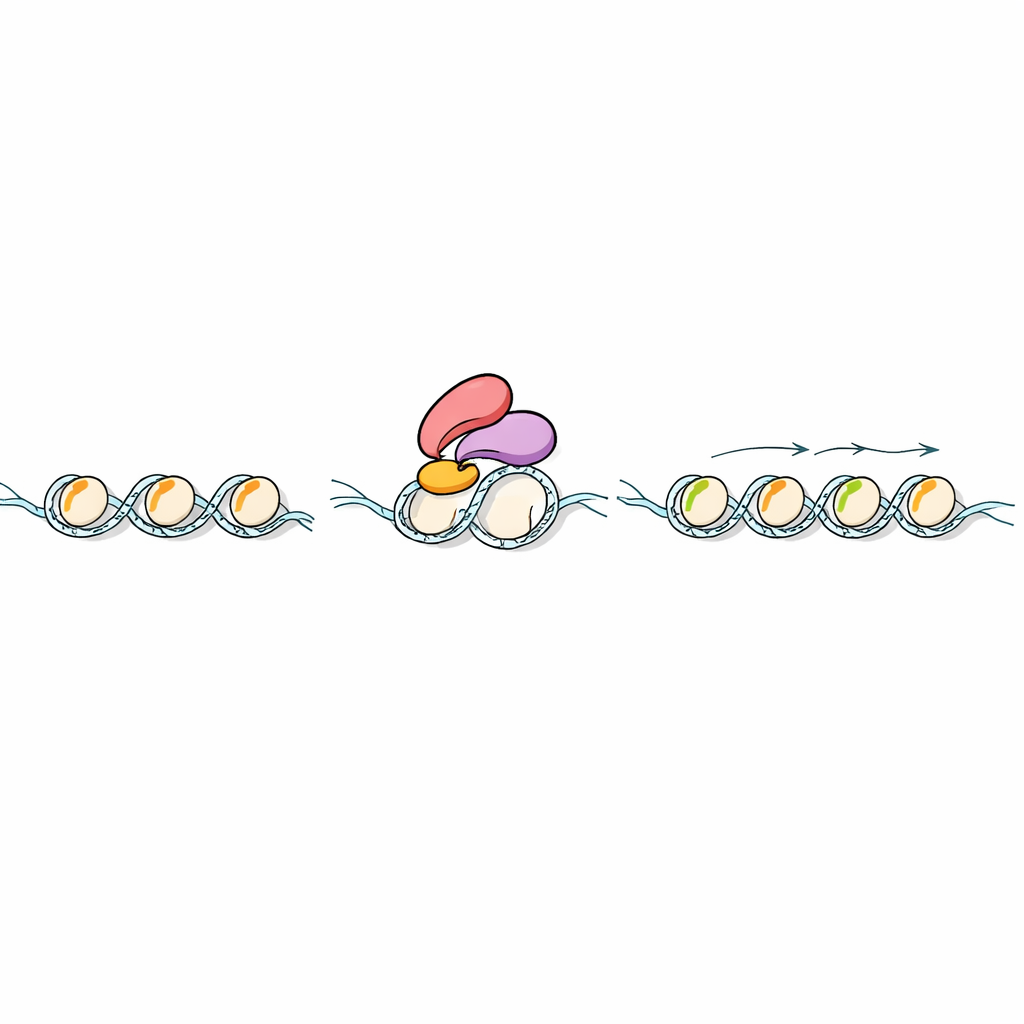
Ein evolutionärer Faden in Landpflanzen
Die Forschenden weiteten ihre Analyse über Reis hinaus aus. Sie zeigten, dass nahe Verwandte von Ehd3 in anderen Landpflanzen ähnliche PHD-Finger-Strukturen aufweisen und in vielen Fällen die gleiche Präferenz für H3K4me1 teilen. Genomweite Daten aus Moosen, Arabidopsis, Reis und weiteren Arten zeigten ein wiederkehrendes Muster: Wo immer H3K4me1 entlang von Genen gefunden wird, sitzen H3K36me2 und H3K36me3 häufig in denselben Regionen. Diese enge Kopplung ist in Algen und Tieren deutlich schwächer oder fehlt, was nahelegt, dass Pflanzen bei der Besiedlung des Landes einen spezialisierten H3K4me1-Leser entwickelt haben, um die H3K36-Methylierung zu etablieren. Das Ergebnis ist ein integriertes Markierungssystem, das vermutlich Pflanzen hilft, die Transkription während der Entwicklung und unter Stress fein abzustimmen.
Warum dieses verborgene System wichtig ist
Für Nicht-Fachleute lautet die zentrale Botschaft: Pflanzen nutzen einen geschichteten chemischen Code auf ihren DNA-verpackenden Proteinen, um zu koordinieren, wann Gene aktiv sind. Diese Arbeit zeigt, dass eine Markierung, H3K4me1, als Startsignal fungiert, das ein Leserprotein, Ehd3, anzieht, das wiederum ein Enzym aktiviert, um entlang von Genen eine zweite Markierung, H3K36me2/3, anzubringen. Zusammen formen diese verknüpften Markierungen Wachstum, Blühzeitpunkt und Stressreaktionen von Pflanzen. Das Verständnis dieser Ereigniskette eröffnet Möglichkeiten, Nutzpflanzen durch Züchtung oder Gentechnik widerstandsfähiger gegenüber sich verändernden Umwelten zu machen, indem man beeinflusst, wie sie ihren eigenen Chromatin-Code lesen und umschreiben.
Zitation: Wu, J., Wang, J., Du, K. et al. H3K4me1 directs H3K36me2 and H3K36me3 deposition in land plants. Nat Commun 17, 2831 (2026). https://doi.org/10.1038/s41467-026-69632-5
Schlüsselwörter: Pflanzen-Epigenetik, Histonmethylierung, Chromatinregulation, Blühzeitpunkt, stressreaktive Gene