Clear Sky Science · ar
النشاط المقارن للسلباكتام والسلباكتام/دورلوباكتام ضد عزلات Acinetobacter baumannii المقاومة للكرباپينيم والتي تنتج إنزيمات OXA-23 أو OXA-23 زائد PER-1
لماذا هذا مهم في عدوى المستشفيات
تواجه المستشفيات حول العالم عدواً عنيداً: جرثومة تُسمى Acinetobacter baumannii قادرة على مقاومة العديد من أقوى مضاداتنا الحيوية. غالباً ما تصيب هذه العدوى مرضى وحدات العناية المركزة وقد تكون مميتة عندما تفشل الأدوية القياسية. تستقصي هذه الدراسة ما إذا كان مزيج الدواء المعتمد حديثاً، سلباكتام/دورلوباكتام، قادرًا على التغلب على هذه المقاومة وما الذي قد يسبب فشله في الحالات النادرة التي لا يعمل فيها.
جرثومة خطيرة في وحدة العناية المركزة
يُعد A. baumannii بكتيريا انتهازية تميل إلى إصابة المرضى الأشد مرضاً، خاصة أولئك على أجهزة التنفس أو المصابين بعدوى مجرى الدم. أصبحت العديد من السلالات مقاومة للكرباپينيمات، وهي فئة قوية من المضادات تُعتبر «الملاذ الأخير». وغالباً ما تقف وراء هذه المقاومة إنزيمات خاصة تقوم بتفكيك هذه العقاقير قبل أن تؤدي دورها. في تركيا، حيث أجريت هذه الدراسة، تنتشر مثل هذه السلالات التي يصعب علاجها، وتحتاج حماية المرضى الضعفاء إلى خيارات علاجية جديدة على وجه السرعة.
مساعد قديم وشريك جديد
السلباكتام دواء قديم يمتلك خاصية مفيدة: بخلاف قدرته على تثبيط بعض إنزيمات المقاومة، يمكنه مهاجمة A. baumannii مباشرة عبر الارتباط ببروتينات رئيسية في جدار الخلية. المشكلة أن إنزيمات بكتيرية أخرى قادرة على تدمير السلباكتام مما يحد من فائدته. دورلوباكتام جزيء أحدث صُمم لدرع أدوية مثل السلباكتام من كثير من هذه الإنزيمات المدمرة. عند استخدامهما معاً، تم اعتماد سلباكتام/دورلوباكتام مؤخراً في الولايات المتحدة لالتهابات الرئة الخطيرة التي تسببها هذه المجموعة من البكتيريا، مما أعاد الأمل في استرجاع فعالية الأدوية التي خسرتها المقاومة.
اختبار التركيبة الجديدة على سلالات مقاومة
فحص الباحثون 24 عزلة سريرية شديدة المقاومة من A. baumannii مأخوذة من عينات دم وعينات متعلقة بالتنفس خلال 2020–2021. كانت جميعها تحمل جين مقاومة للكرباپينيم يُسمى OXA-23؛ وكان نصفها يحمل أيضاً جين مقاومة إضافي وهو PER-1. قاس الفريق مقدار السلباكتام وحده ومقدار السلباكتام/دورلوباكتام معاً اللازمين لوقف نمو البكتيريا في المختبر. كانت هناك عزلة واحدة فقط قابلة للعلاج بوضوح بالسلباكتام بمفرده، مما يبرز محدودية هذا الدواء القديم. على النقيض من ذلك، كانت 22 من أصل 24 عزلة (حوالي 92٪) قابلة للعلاج عندما اقترنت السلباكتام بدورلوباكتام، وانخفضت كمية الدواء المطلوبة بشكل حاد عند استخدام التركيبة.
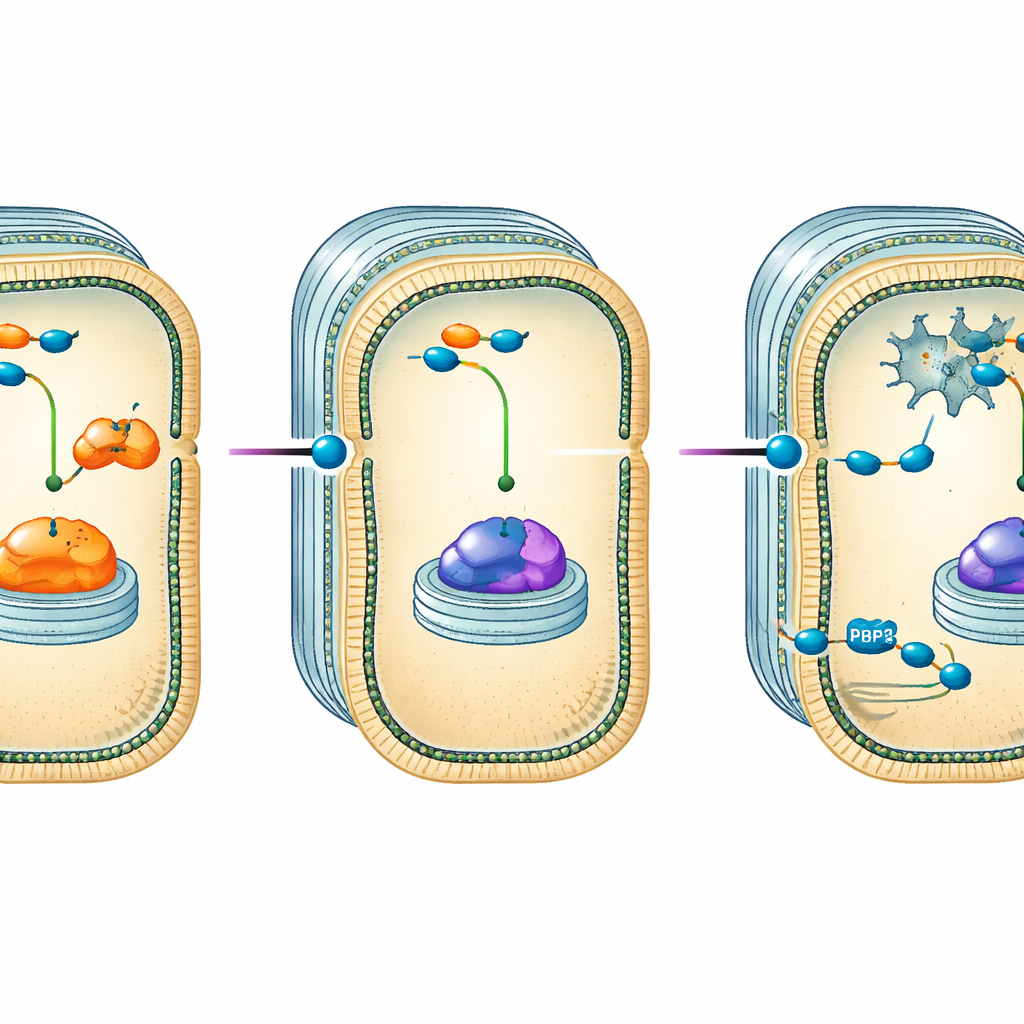
لماذا نَفَت بعض السلالات المقاومة
قاومت عينتان التركيبة الجديدة، بما في ذلك واحدة ذات مقاومة عالية جداً. لفهم السبب، قام العلماء بتسلسل جينوماتهما بالكامل ومقارنتها مع سلالة حساسة. حملت الثلاث سلالات عدة إنزيمات مقاومة نمطية، لكن هذه الإنزيمات وحدها لم تكن كافية لتفسير فشل سلباكتام/دورلوباكتام. بدلاً من ذلك، تبيّن أن كلتا العزلتين المقاومتين احتوتا على تغييرات في بروتين جدار الخلية الحاسم المسمى PBP3، الهدف الرئيسي للسلباكتام. احتوت إحدى السلالات على استبدالات محددة في PBP3 وفقدت منظمًا عادةً ما يكبح نظام ضخ الدواء (مضخّة طرد)، مما سمح على الأرجح للخلايا بطرد مزيد من الدواء. السلالة الثانية احتوت على إدخال حمض أميني إضافي في PBP3، وهو تعديل هيكلي قد يضعف قدرة الدواء على الالتصاق بالهدف بشكل كبير.
ماذا يعني هذا للعلاج المستقبلي
للقارئ العام، الرسالة الأساسية هي أن سلباكتام/دورلوباكتام يبدو خياراً جديداً قوياً ضد هذا الممرض المستشفي المخيف، حيث نجح في تعطيل المقاومة في نحو تسع من كل عشر سلالات شديدة المقاومة في هذه الدراسة. ومع ذلك، لا تزال البكتيريا قادرة على المقاومة عبر إعادة تشكيل دقيقة للبروتين الذي يحتاجه الدواء للوصل إليه، أو عبر طرد الدواء بكفاءة أكبر. تؤكد هذه النتائج على كل من الوعود وهشاشة المضادات الحيوية الجديدة: فهي قادرة على إعادة الأمل حيث تفشل الأدوية القديمة، لكن التطور يبحث دائماً عن ثغرات. سيكون الاستخدام الحذر لسلباكتام/دورلوباكتام والمراقبة المستمرة لظهور المقاومة أمرين أساسيين للحفاظ على فعالية هذا السلاح الجديد للمرضى الذين في أمس الحاجة إليه.
الاستشهاد: Mirza, H.C., Üsküdar Güçlü, A., Ünlü, S. et al. Comparative activity of sulbactam and sulbactam/durlobactam against carbapenem-resistant A. baumannii isolates producing OXA-23 or OXA-23 plus PER-1 enzymes. J Antibiot 79, 402–409 (2026). https://doi.org/10.1038/s41429-026-00919-x
الكلمات المفتاحية: Acinetobacter baumannii, مقاومة المضادات الحيوية, سلباكتام دورلوباكتام, عدوى المستشفيات, بيتا-لاكتاماز