Clear Sky Science · ar
علاج سينوليتك داستينيب والكويرسيتين يؤخر بدء تدهور القرص بين الفقري في فئران SM/J
لماذا تهم هذه الخلفية
ألم الظهر هو أحد أكثر الأسباب شيوعًا لتغيب الناس عن العمل أو مواجهة صعوبات في المهام اليومية، وتُعد الأقراص الشوكية المتآكلة سببًا رئيسًا لذلك. ومع ذلك، فإن العلاجات الحالية تخفف الأعراض في الغالب بدلاً من إبطاء الضرر نفسه. تستكشف هذه الدراسة في الفئران فكرة جديدة: استخدام أدوية تستهدف بشكل انتقائي الخلايا «المسنّة» أو التالفة داخل الأقراص الشوكية لإبطاء التحلل المبكر. وتشير النتائج إلى أن تركيبة دوائية تُجرَّب بالفعل على البشر لحالات أخرى قد تساعد يومًا ما في حماية الأشخاص المعرضين وراثيًا لألم الظهر المرتبط بالأقراص.
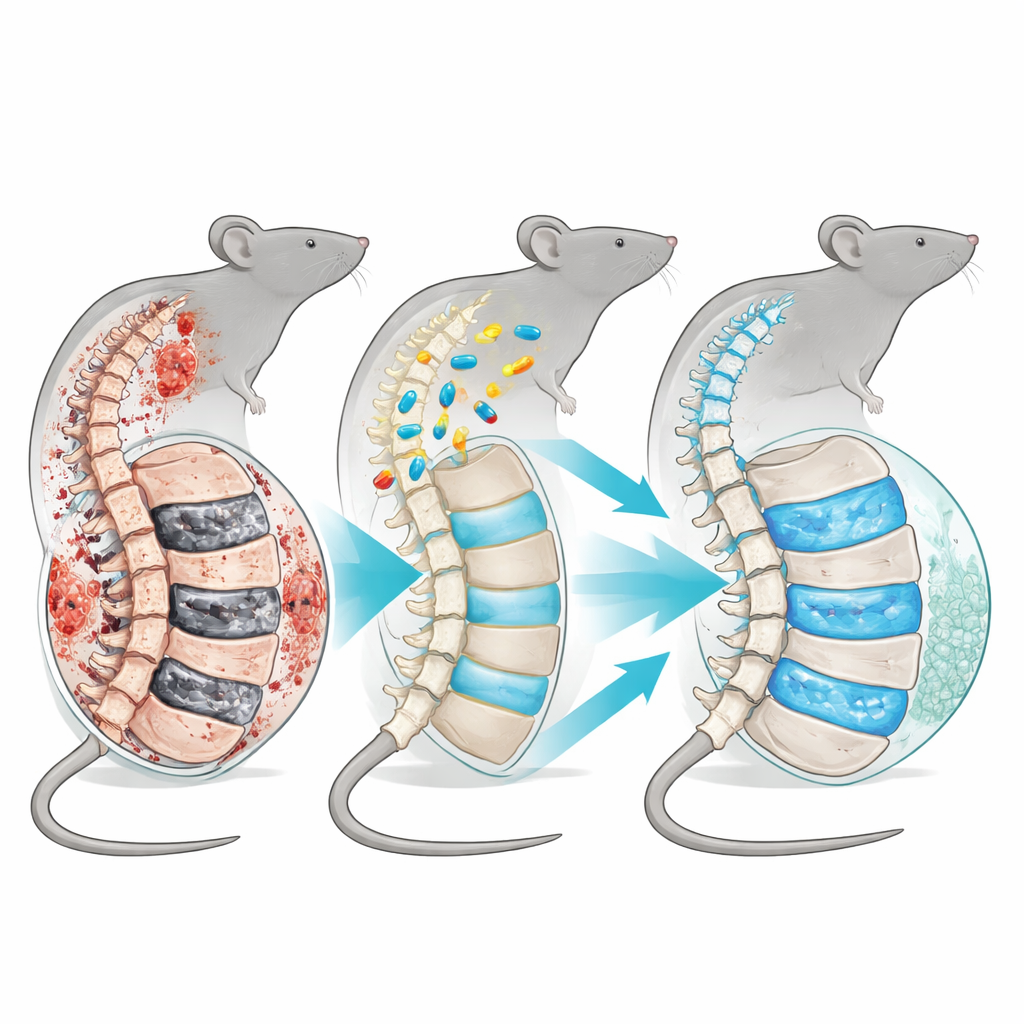
عندما تتآكل الوسائد الشوكية مبكرًا
بين كل فقرتين في العمود الفقري يوجد قرص يعمل كوسادة قوية غنية بالماء. في المركز يوجد لب هلامي (النواة اللبية) محاط بحلقة ليفية ومغطى بلوحات طرفية رقيقة. في بعض سلالات الفئران المسماة SM/J، تبدأ هذه الأقراص بالتدهور في وقت مبكر بشكل غير معتاد من الحياة، مما يُحاكي مرض الأقراص العدواني ذو البداية المبكرة الذي يُرى عند بعض البشر. بحلول عمر 17 أسبوعًا—وهو مرحلة تشبه مرحلة الشباب البالغ عند الفأر—تظهر لدى هذه الحيوانات بالفعل سمات مثل فقدان بنية القرص الطبيعية، وتندب اللب الطري، وتغيرات في سلوك الخلايا تشبه العمود الفقري المسن أو المصاب.
خلايا «قديمة قبل أوانها» داخل القرص
ركز الباحثون على الشيخوخة الخلوية، وهي حالة تتوقف فيها الخلايا عن الانقسام، وتقاوم الموت، وتفرز خليطًا من الجزيئات الالتهابية وإعادة تشكيل النسيج المعروف باسم النمط الإفرازي المرتبط بالشيخوخة (SASP). في أقراص فئران SM/J وجدوا مستويات عالية من علامات الشيخوخة، بما في ذلك بروتينات تسمى p19 وp21، وذلك قبل ظهور التلف البنيوي الواضح بوقت طويل. أظهر تحليل واسع لنشاط الجينات أن أنسجة القرص تشترك في العديد من السمات مع توقيعات جينية معروفة «للخلايا المسنة»: تغيّرات في التحكم بدورة الخلية، ومسارات الاستجابة للإجهاد، وإشارات مرتبطة بالالتهاب، ونمو الأوعية الدموية، والتندب. معًا، تشير هذه البيانات إلى أن الخلايا التي تدخل حالة الشيخوخة مبكرًا تمثل قوة دافعة وراء التحلل المبكر للأقراص في هذا النموذج.
اختبار أدوية تزيل أو تهدئ الخلايا المسنة
اختبر الفريق بعد ذلك نهجين «سينوليتك» جهازيين (يعملان في الجسم كله)—أدوية مصممة لإزالة أو إضعاف الخلايا المسنة. تلقَّت مجموعة من فئران SM/J الشابة حقنًا أسبوعية من نافيتوكلكس، وتلقت مجموعة أخرى مزيجًا من داستينيب مع كويرسيتين (غالبًا ما يُختصر DQ). بدأت المعالجة في عمر أربعة أسابيع، قبل وجود تلف شديد، واستمرت حتى 17 أسبوعًا. لم يُحسّن نافيتوكلكس، رغم نجاحه في أنسجة أخرى وعند حقنه مباشرة في الأقراص في أعمال سابقة، بنية القرص أو يقلل علامات الشيخوخة في هذه الفئران. على النقيض من ذلك، أدت جرعة داستينيب مع كويرسيتين إلى أقراص تبدو بصحة أفضل بشكل ملحوظ: تم الحفاظ على اللب المركزي والحلقة الخارجية بشكل أفضل، وانخفض التندب، وبلغ عدد الأقراص التي وصلت إلى أشد درجات التحلل مستويات أقل.
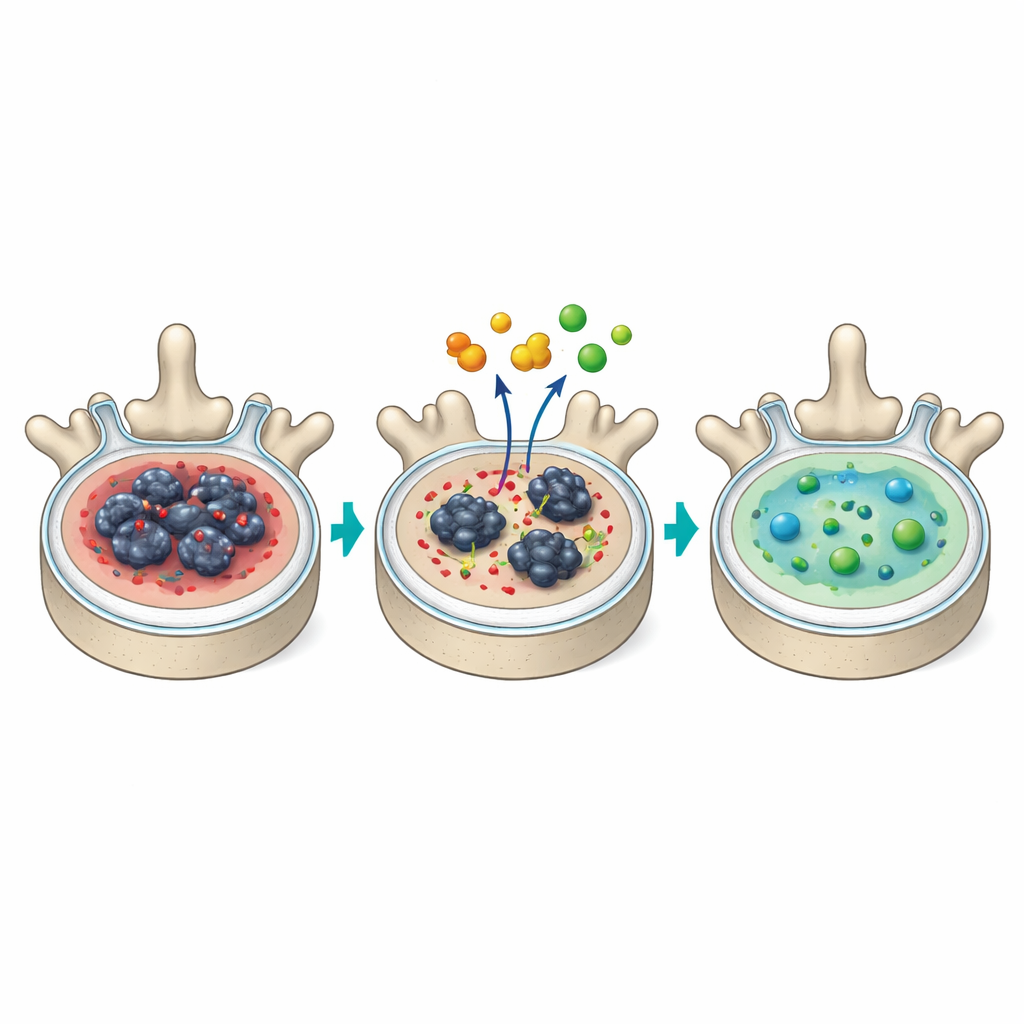
مصفوفة أكثر صحة، وخلايا أكثر صحة
أظهرت الأقراص المعالجة بـDQ عددًا أقل من الخلايا المسنة، ومستويات أدنى من جزيئات SASP الرئيسية مثل IL-6 وMMP13، وكمية أقل من بروتين التندب TGF-β. احتوى اللب المركزي على ألياف كولاجين سميكة أقل—وهي سمة مميزة للتليف—والمزيد من الألياف الرقيقة المنظمة التي تُرى في النسيج الأكثر صحة. احتفظت خلايا اللب في كثير من الأحيان بميزات نمطية للخلايا القرصية الشبابية وكانت أقل ميلًا لتشبه خلايا الغضروف التضخمي المرتبطة بمرحلة التلف النهائية. ومن المهم أن الأقراص المعالجة بـDQ احتوت على خلايا حية أكثر وخلايا ماتت (موجبة لصبغة TUNEL) أقل مع مرور الوقت، مما يوحي بأن هذا النظام يساعد الخلايا الموجودة على البقاء في بيئة أكثر توازنًا وأقل التهابية بدلاً من مجرد القضاء عليها. وعلى مستوى الجسم كله، خفّض العلاج بشكل معتدل بعض الإشارات الالتهابية في الدم لكنه ترك عظام الفقرات دون تغيير كبير، مما يلمّح إلى ملف سلامة مناسب في العمود الفقري.
كشف مفاتيح التحكم الداخلية
لفهم كيف يعيد DQ تشكيل بيولوجيا القرص، قارن المؤلفون نشاط الجينات في الأقراص المعالجة وغير المعالجة. وجدوا تغييرات منسقة في المسارات التي تتحكم بدورة الخلية، واستجابات تلف الحمض النووي، وشبكات إشارات الإجهاد، وبخاصة تلك التي تنطوي على JNK وعائلة عوامل النسخ المسماة JUN. عند مقارنتهم بهذه النتائج بدراسة سابقة في فئران الشيخوخة العادية، ظهر نمط مشترك: في كل من تدهور القرص المبكر المرتبط بالجينات والتدهور المرتبط بالعمر، خفّض DQ باستمرار جينات مثل Junb وZfp36l1 المرتبطة بالشيخوخة والالتهاب والتليف. في خلايا أقراص بشرية نمت في المختبر، أدى حجب JUN بدواء منفصل إلى محاكاة العديد من فوائد DQ، بما في ذلك انخفاض علامات الشيخوخة وتخفيف جينات SASP، مما يربط إشارة JUN بالتأثير الوقائي.
ما الذي قد يعنيه ذلك لرعاية ألم الظهر في المستقبل
بشكل إجمالي، تُظهر الدراسة أنه في نموذج فأري عرضة للتحلل المبكر للأقراص، تظهر الخلايا المسنة مبكرًا وتساهم في دفع المرض، وأن العلاج الجهازِيّ بداستينيب مع كويرسيتين يمكن أن يبطئ التلف البنيوي، ويحد من التندب، ويحافظ على خلايا قرص أكثر شبابًا. كما تشير النتائج إلى أن مسارات مرتبطة بـJUN تعمل كمفاتيح تحكم قد تُخفَّض بواسطة هذه الأدوية. وعلى الرغم من أن هذه النتائج قبل سريرية ولا تُترجم مباشرة بعد إلى علاج للبشر، فإنها تقوّي حجّة استراتيجيات شبيهة بالسينوليتك كطريقة لتعديل مرض القرص نفسه، بدلًا من مجرد معالجة الألم بعد حدوث التلف.
الاستشهاد: Novais, E.J., Ottone, O.K., Jagannath, S. et al. Dasatinib and quercetin senolytic treatment delays early onset intervertebral disc degeneration in SM/J mice. Bone Res 14, 42 (2026). https://doi.org/10.1038/s41413-026-00526-4
الكلمات المفتاحية: تدهور القرص بين الفقري, الشيخوخة الخلوية, علاج سينوليتك, داستينيب وكويرسيتين, ألم الظهر