Clear Sky Science · zh
阿尔茨海默病神经病理学转基因小鼠模型中的甲基组学特征:tau 与淀粉样β
本研究为何有助于理解记忆丧失
阿尔茨海默病会逐步剥夺人的记忆和独立生活能力,但我们仍未完全弄清脑内破坏的驱动机制。本研究考察小鼠模型中 DNA 上的微小化学标记,称为甲基化标记,这些模型模拟了阿尔茨海默病的核心特征。通过追踪这些标记随着有害的 tau 纠结和淀粉样β 斑块积累而发生的变化,研究者希望发现早期预警信号以及在脑细胞死亡前很久就能作为治疗靶点的新线索。 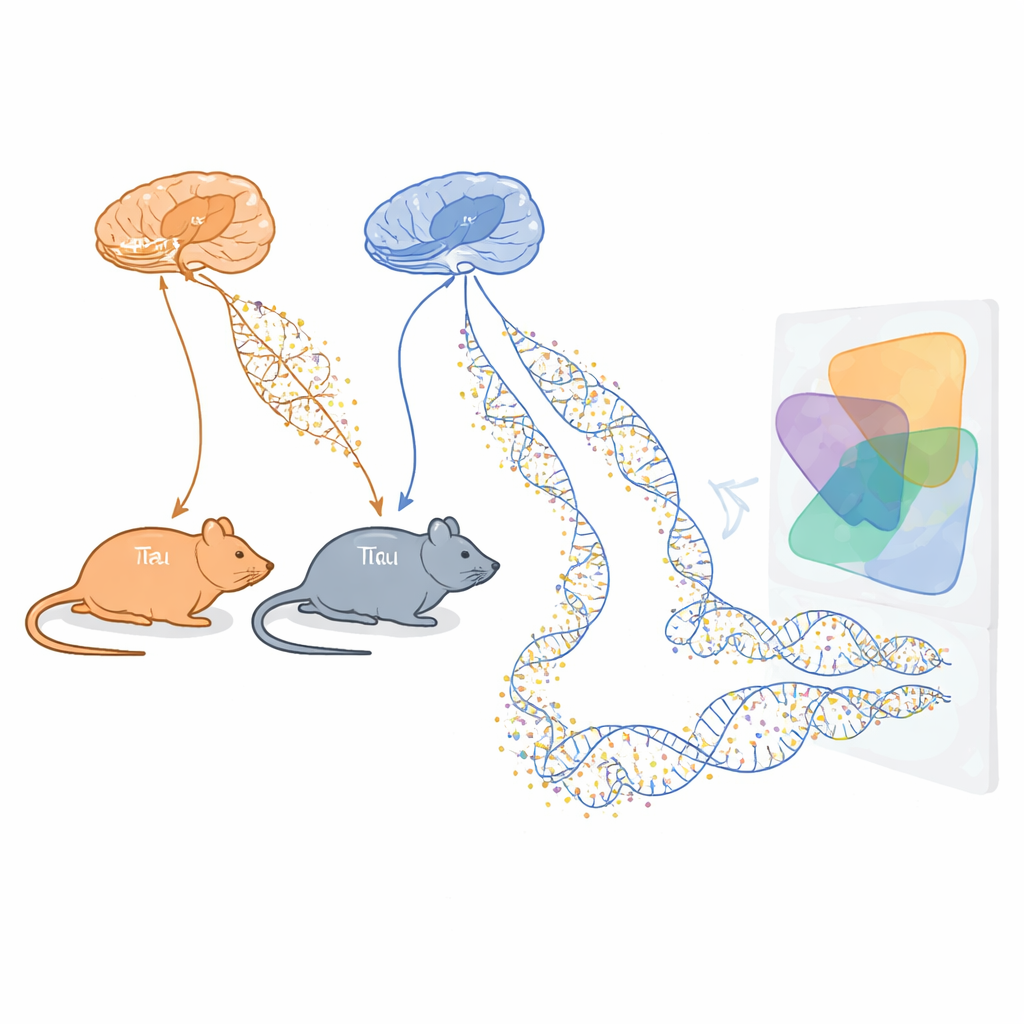
两种代表人类阿尔茨海默病的鼠模型
研究团队使用了两种成熟的小鼠品系,各自模拟阿尔茨海默病的一个主要方面。一种称为 rTg4510,会产生异常的人类 tau 蛋白,在神经元内形成纠结;另一种称为 J20,携带导致过量淀粉样β 的突变,这种蛋白在细胞间聚集成斑块。对于这两种模型,科学家在跨越从早期到更晚期的多个年龄点,从两个与记忆密切相关的大脑区域——内嗅皮层和海马——收集样本。随后他们在全基因组中测量了超过一百万个位点的 DNA 甲基化,结合深度测序和定制芯片,以获得对表观遗传随时间变化的广泛且可靠的视图。
脑内随 tau 纠结而发生的变化
在 tau 小鼠中,DNA 甲基化发生了大量变化,尤其集中在与神经元间通讯、细胞死亡以及脑内脂质相关信号通路有关的基因上。随着 tau 病理恶化,许多位点甲基化水平上升,其中包括那些帮助决定神经元是生存还是自毁的基因。这些基因中的一些,例如参与蛋白质清除系统和维持突触健康的基因,也出现了表达水平的变化,提示甲基化改变可能在开启或关闭病理通路中发挥作用。作为记忆形成关键中心的海马,其甲基化改变比内嗅皮层更为显著,其“表观年龄”也显得较预期更老,暗示 tau 可能加速这一易感区域的分子老化。
淀粉样β 斑块留下了不同的印记
相比之下,淀粉样β 小鼠的甲基化变化较少且幅度通常较小,这些变化更紧密地与免疫反应和细胞内能量工厂有关。位于炎症、线粒体健康和突触结构相关基因附近的位点,随着斑块积累受到的影响尤为明显。内嗅皮层与海马之间的模式差异很大,这表明淀粉样β 引起的表观遗传效应更具区域特异性,可能比 tau 更依赖局部细胞类型或时间顺序。两种模型合在一起暗示,大脑对 tau 纠结和淀粉样β 斑块的反应在分子通路上既有重叠也有差异,而 tau 在基因组上的影响更为广泛。
在小鼠与人类之间共享的表观遗传指纹
为了检验小鼠结果是否真正反映人类疾病,研究者将他们的结果与大型人类阿尔茨海默病脑组织的 DNA 甲基化研究进行了比较,发现了显著的重叠。关键基因如 ANK1 和 PRDM16 在小鼠模型和阿尔茨海默病患者脑组织中显示出相似的甲基化改变。许多共同变化发生在非神经元的支持细胞中,与人类数据中强调的神经胶质细胞在疾病进展中作用相吻合。这些跨物种的共鸣表明,小鼠的甲基化模式并非仅仅是遗传工程的副产物,而是捕捉到了在人类大脑中也起作用的核心机制。 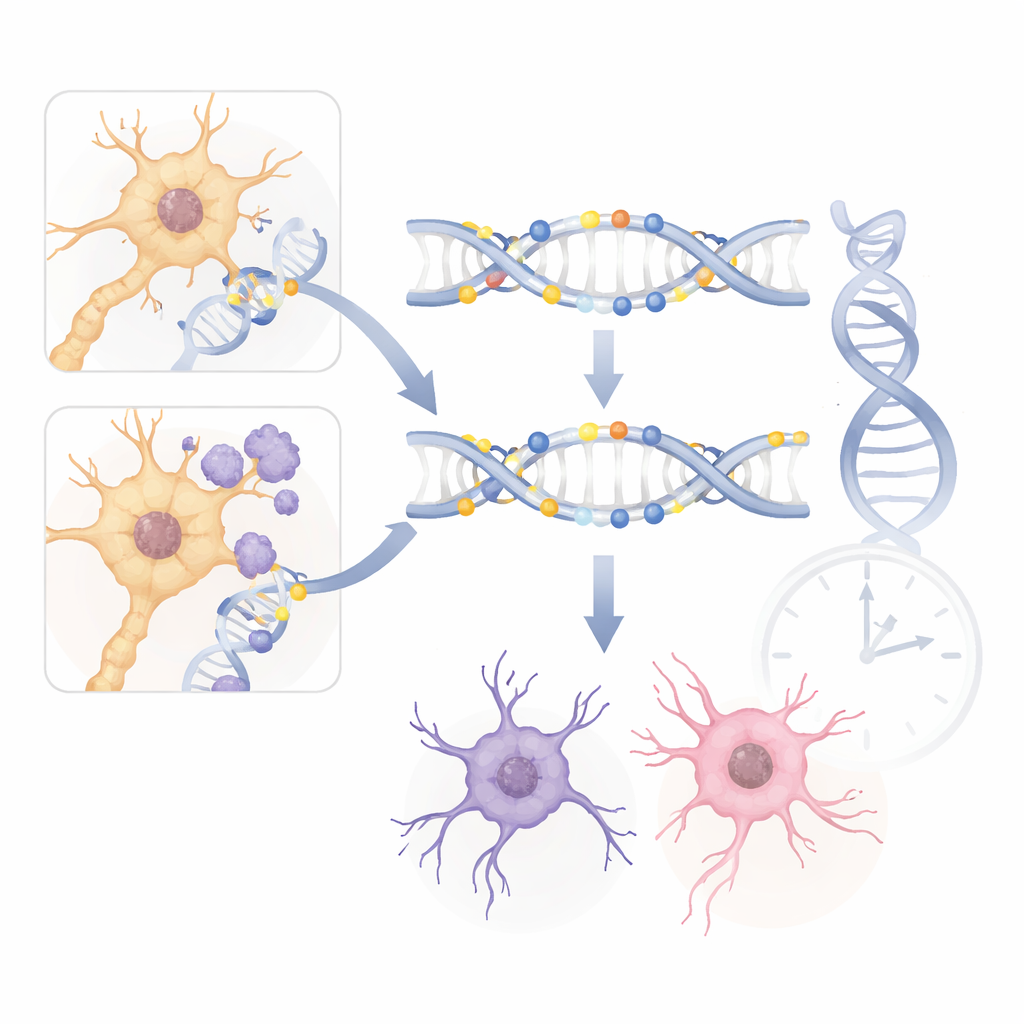
这些发现对未来治疗意味着什么
对非专业读者而言,主要信息是与阿尔茨海默病相关的大脑变化在症状出现很久之前就会在 DNA 上留下可检测的化学印记。特别是 tau 纠结,与广泛的甲基化位点变化相关,这些变化与病情严重程度和加速的分子老化相一致。淀粉样β 斑块则触发另一套变化,尤其影响免疫和能量通路。由于许多这些表观遗传特征在人类大脑中也能找到对应,它们可能帮助科学家识别早期生物标志物,或设计将有害基因程序调整回更健康状态的药物。这项工作尚不能提供治愈方法,但为从蛋白质积累到脑细胞损伤描绘了一条更为细致的分子路径,使研究者更接近于开发减缓或预防阿尔茨海默病的新策略。
引用: Leung, S.K., Walker, E.M., Policicchio, S. et al. Methylomic signatures of tau and amyloid-beta in transgenic mouse models of Alzheimer’s disease neuropathology. npj Dement. 2, 23 (2026). https://doi.org/10.1038/s44400-026-00074-y
关键词: 阿尔茨海默病, 表观遗传学, DNA 甲基化, tau 与淀粉样β, 小鼠模型