Clear Sky Science · fr
Signatures méthylomiques de la protéine tau et de l’amyloïde-bêta dans des modèles murins transgéniques de la neuropathologie de la maladie d’Alzheimer
Pourquoi cette recherche compte pour comprendre la perte de mémoire
La maladie d’Alzheimer prive progressivement les personnes de leur mémoire et de leur autonomie, mais nous ne comprenons pas encore complètement ce qui provoque les dommages dans le cerveau. Cette étude examine de petites marques chimiques sur l’ADN, appelées marques de méthylation, dans des modèles murins qui reproduisent des traits centraux de la maladie d’Alzheimer. En suivant l’évolution de ces marques à mesure que s’accumulent les enchevêtrements toxiques de tau et les plaques d’amyloïde-bêta, les chercheurs cherchent à mettre au jour des signaux d’alerte précoces et des cibles potentielles pour des traitements bien avant la mort des cellules cérébrales. 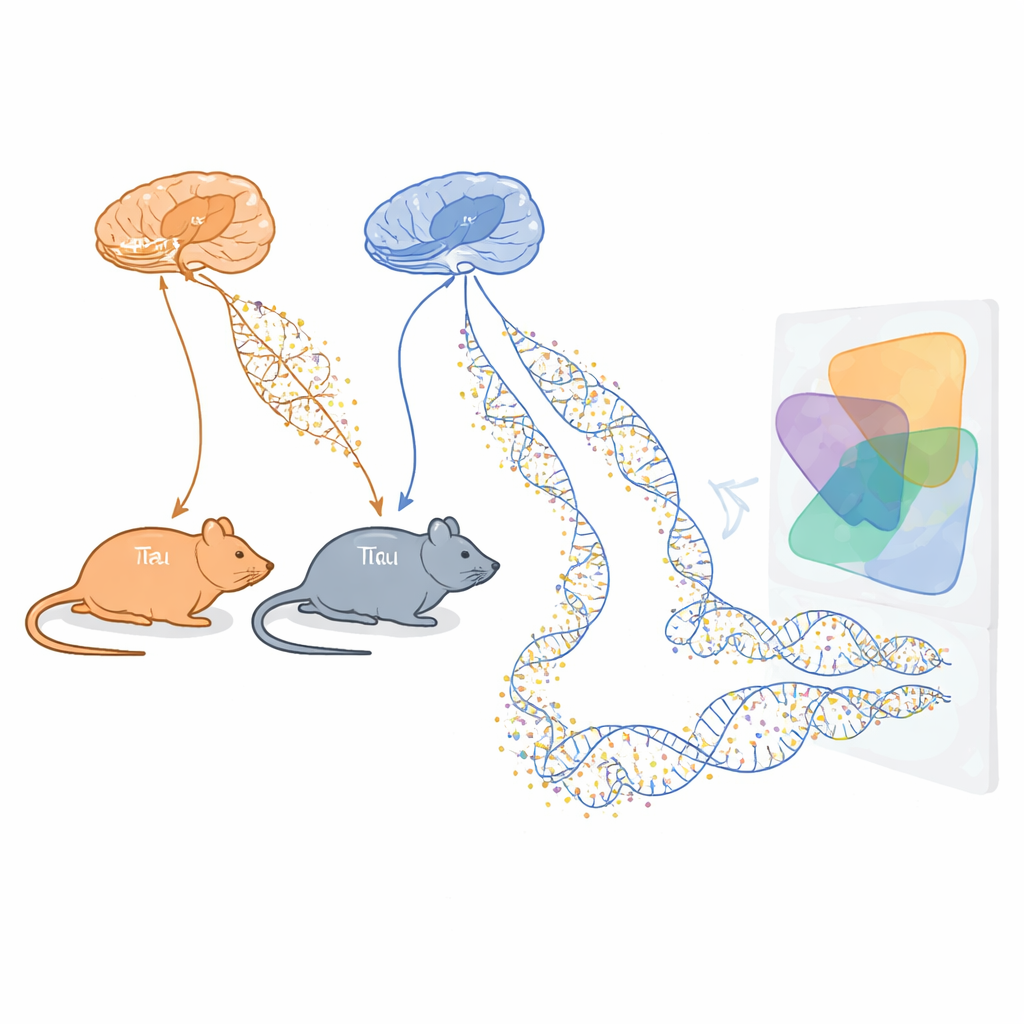
Deux modèles murins pour représenter l’Alzheimer humaine
L’équipe a utilisé deux lignées murines bien établies qui modélisent chacune un aspect majeur de la maladie d’Alzheimer. L’une, appelée rTg4510, produit une protéine tau humaine anormale qui forme des enchevêtrements à l’intérieur des neurones. L’autre, appelée J20, porte des mutations qui entraînent un excès d’amyloïde-bêta, une protéine qui s’agglomère en plaques entre les cellules. Pour les deux modèles, les scientifiques ont prélevé des échantillons de deux régions cérébrales essentielles à la mémoire, le cortex entorhinal et l’hippocampe, à plusieurs âges couvrant des stades précoces à plus avancés simulant la maladie. Ils ont ensuite mesuré la méthylation de l’ADN sur plus d’un million de sites du génome, en utilisant à la fois un séquençage profond et une puce personnalisée afin d’obtenir une vue large et fiable des changements épigénétiques au fil du temps.
Ce qui change avec les enchevêtrements de tau dans le cerveau
Chez le modèle tau, la méthylation de l’ADN a évolué de façon étendue, en particulier dans des gènes liés à la communication neuronale, à la mort cellulaire et à la signalisation lipidique dans le cerveau. De nombreux sites ont gagné en méthylation à mesure que la pathologie liée à la tau s’aggravait, y compris dans des gènes qui contribuent à contrôler la survie ou l’autodestruction des neurones. Certains de ces gènes, comme ceux impliqués dans les systèmes d’élimination des protéines et le maintien de synapses saines, ont aussi montré des modifications de leur activité, ce qui suggère que l’altération de la méthylation pourrait contribuer à activer ou désactiver des voies pathologiques. L’hippocampe, un centre clé pour la formation des souvenirs, a présenté des changements de méthylation encore plus prononcés que le cortex entorhinal, et son « âge épigénétique » semblait plus avancé que prévu, laissant penser que la tau peut accélérer le vieillissement moléculaire de cette région vulnérable.
Comment les plaques d’amyloïde‑bêta laissent une empreinte différente
En revanche, le modèle amyloïde‑bêta a montré moins de changements de méthylation et des changements généralement moins marqués, davantage liés aux réponses immunitaires et aux « centrales énergétiques » des cellules. Les sites proches de gènes impliqués dans l’inflammation, la santé mitochondriale et la structure des synapses ont été particulièrement affectés à mesure que les plaques s’accumulaient. Les schémas différaient fortement entre cortex entorhinal et hippocampe, ce qui implique que les effets épigénétiques de l’amyloïde‑bêta sont plus spécifiques à la région et peut‑être plus dépendants des types cellulaires locaux ou du timing que ceux de la tau. Ensemble, les deux modèles suggèrent que le cerveau répond aux enchevêtrements de tau et aux plaques d’amyloïde‑bêta par des voies moléculaires qui se recoupent mais restent distinctes, la tau laissant une empreinte génomique plus large.
Empreintes épigénétiques partagées chez la souris et l’humain
Pour vérifier si les observations murines reflètent réellement la maladie humaine, les chercheurs ont comparé leurs résultats à de larges études de méthylation de l’ADN sur des cerveaux humains atteints d’Alzheimer. Ils ont trouvé des recouvrements frappants. Des gènes clés tels qu’ANK1 et PRDM16 ont montré des décalages de méthylation similaires chez les modèles murins et dans les tissus cérébraux de personnes atteintes d’Alzheimer. De nombreux changements partagés se sont produits dans des cellules de soutien non neuronales, en accord avec les données humaines qui soulignent le rôle des cellules gliales dans la progression de la maladie. Ces échos inter‑espèces suggèrent que les motifs de méthylation observés chez la souris ne sont pas de simples sous‑produits de modifications génétiques, mais reflètent des mécanismes fondamentaux qui opèrent également dans le cerveau humain. 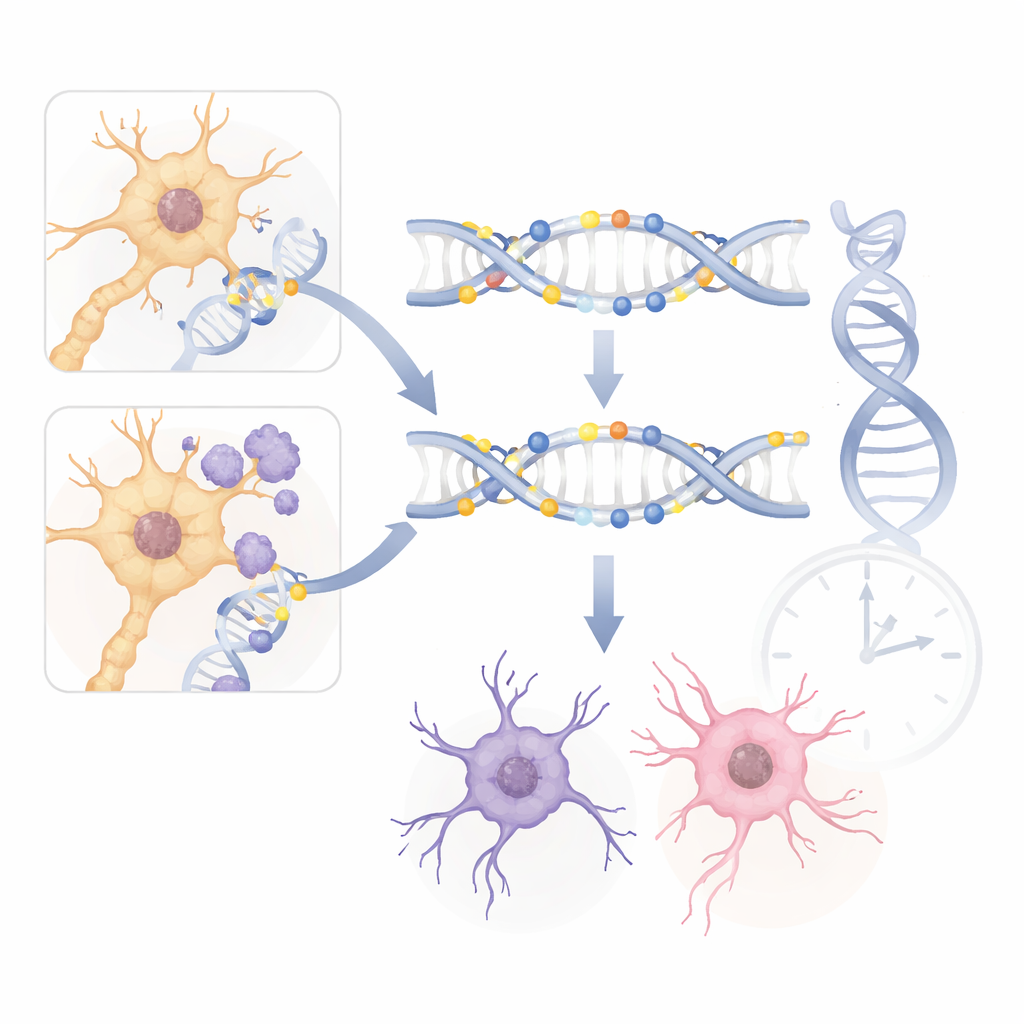
Ce que tout cela signifie pour les traitements futurs
Pour un non‑spécialiste, le message principal est que les changements cérébraux liés à l’Alzheimer laissent une empreinte chimique détectable sur l’ADN bien avant l’apparition des symptômes. Les enchevêtrements de tau, en particulier, s’associent à des modifications étendues de la méthylation qui suivent la sévérité de la maladie et un vieillissement moléculaire accéléré. Les plaques d’amyloïde‑bêta déclenchent leur propre jeu de changements, notamment dans les voies immunitaires et énergétiques. Parce que beaucoup de ces signatures épigénétiques reflètent celles observées dans les cerveaux humains, elles pourraient aider les chercheurs à identifier des biomarqueurs précoces ou à concevoir des médicaments qui réorientent des programmes génétiques nuisibles vers un état plus sain. Ce travail n’apporte pas encore de cure, mais il cartographie de façon plus détaillée le trajet moléculaire depuis l’accumulation de protéines jusqu’aux dommages neuronaux, rapprochant les chercheurs d’approches nouvelles pour ralentir ou prévenir la maladie d’Alzheimer.
Citation: Leung, S.K., Walker, E.M., Policicchio, S. et al. Methylomic signatures of tau and amyloid-beta in transgenic mouse models of Alzheimer’s disease neuropathology. npj Dement. 2, 23 (2026). https://doi.org/10.1038/s44400-026-00074-y
Mots-clés: maladie d’Alzheimer, épigénétique, méthylation de l’ADN, tau et amyloïde-bêta, modèles murins