Clear Sky Science · ru
Метиломные сигнатуры тау и амилоид-бета в трансгенных мышиных моделях нейропатологии болезни Альцгеймера
Почему это исследование важно для понимания потери памяти
Болезнь Альцгеймера постепенно лишает людей памяти и независимости, но механизмы поражения мозга остаются не до конца изученными. В этом исследовании изучаются крошечные химические метки на ДНК — метилляционные отметки — в мышиных моделях, воспроизводящих ключевые черты Альцгеймера. Отслеживая, как эти метки меняются по мере накопления вредоносных клубков тау и амилоид-бета бляшек, исследователи стремятся выявить ранние сигналы тревоги и возможные новые мишени для лечения задолго до гибели нейронов. 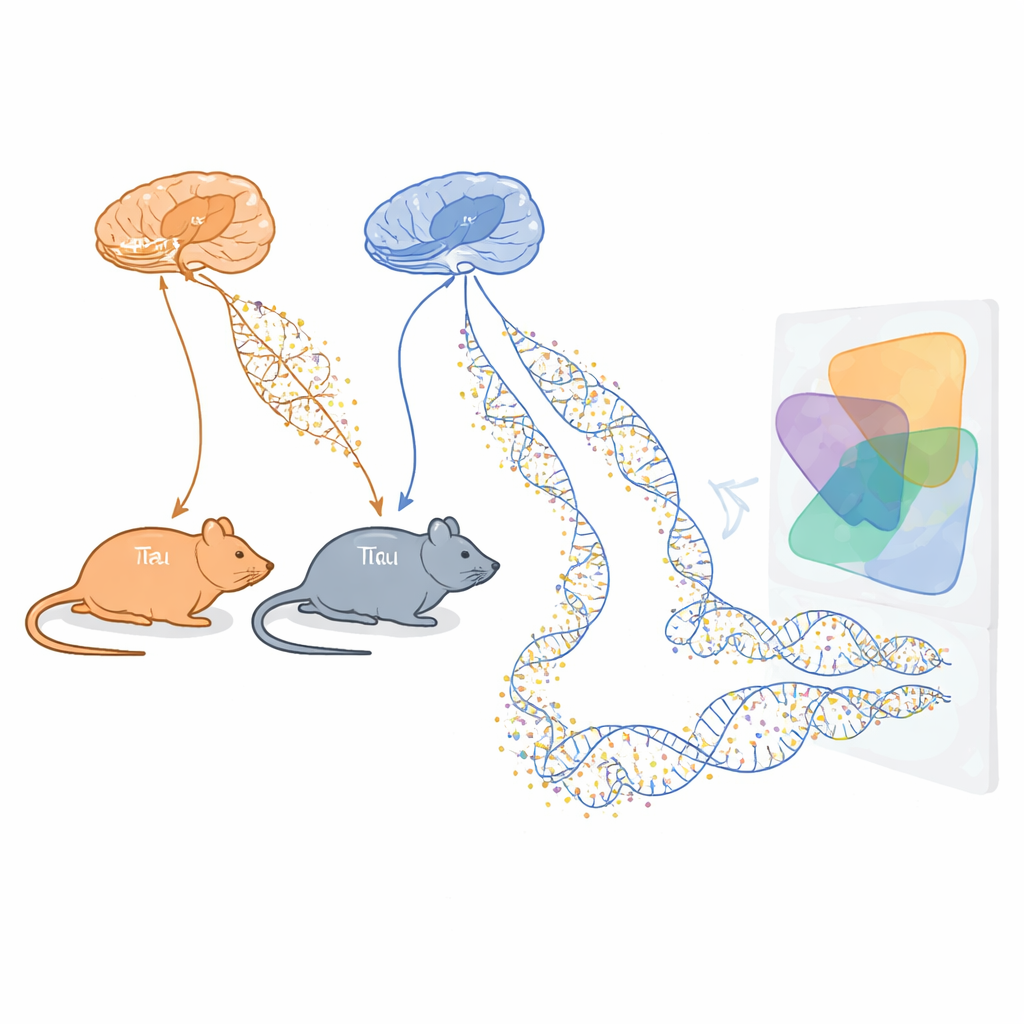
Две мыши, заменяющие человека с Альцгеймером
Команда использовала две хорошо зарекомендовавшие себя линии мышей, каждая из которых моделирует один из ключевых аспектов болезни Альцгеймера. Одна, rTg4510, экспрессирует аномальный человеческий белок тау, образующий клубки внутри нейронов. Другая, J20, несет мутации, приводящие к избытку амилоид-бета — белка, который скапливается в бляшки между клетками. Для обеих моделей ученые собирали образцы из двух критически важных для памяти областей мозга — энторинальной коры и гиппокампа — в разные возрасты, охватывающие стадии от ранних до более продвинутых, похожих на болезнь. Затем они измеряли метилирование ДНК более чем в миллионе сайтов в геноме, используя как глубокое секвенирование, так и специализированный чип, чтобы получить широкую и надежную картину эпигенетических изменений с течением времени.
Что меняется при клубках тау в мозге
У мышей с тау наблюдались обширные изменения метилирования ДНК, особенно в генах, связанных с передачей сигналов между нейронами, программируемой гибелью клеток и липидной сигнализацией в мозге. Многие сайты приобретали метилирование по мере усугубления тау-патологии, в том числе в генах, участвующих в контроле выживания нейронов или запуске их самоуничтожения. Некоторые из этих генов, например вовлеченные в системы утилизации белков и поддержание здоровых синапсов, также демонстрировали изменения экспрессии, что указывает на то, что измененное метилирование может переключать патологические пути в активное или неактивное состояние. Гиппокамп, ключевой центр формирования памяти, показал еще более выраженные метиломные сдвиги, чем энторинальная кора, а его «эпигенетический возраст» выглядел старше ожидаемого, намекая на то, что тау может ускорять молекулярное старение этой уязвимой области.
Как амилоид-бета бляшки оставляют иной след
В отличие от этого, у мышей с амилоид-бета наблюдалось меньше и в целом более слабое изменение метилирования, причём эти изменения были теснее связаны с иммунными ответами и работой энергетических «фабрик» в клетках — митохондрий. Сайты рядом с генами, участвующими во воспалении, здоровье митохондрий и структуре синапсов, были особенно затронуты по мере накопления бляшек. Шаблоны отличались между энторинальной корой и гиппокампом, что указывает на то, что эпигенетические эффекты амилоид-бета более регионально специфичны и, возможно, сильнее зависят от локальных типов клеток или времени, чем эффекты тау. В совокупности обе модели показывают, что мозг реагирует на клубки тау и бляшки амилоид-бета перекрывающимися, но различающимися молекулярными путями, при этом тау оказывает более широкое влияние на геном.
Общие эпигенетические отпечатки у мышей и людей
Чтобы проверить, отражают ли мышиные результаты человеческое заболевание, исследователи сопоставили свои данные с крупными исследованиями метилирования ДНК в мозге людей с Альцгеймером. Они обнаружили поразительные совпадения. Ключевые гены, такие как ANK1 и PRDM16, показывали схожие сдвиги метилирования в мышиных моделях и в тканях мозга людей с Альцгеймером. Многие общие изменения происходили в не-нейронных поддерживающих клетках, что соответствует человеческим данным, подчеркивающим роль глиальных клеток в прогрессии болезни. Эти межвидовые отклики предполагают, что паттерны метилирования у мышей — это не просто побочный продукт генетической модификации, а отражение ключевых механизмов, действующих и в человеческом мозге. 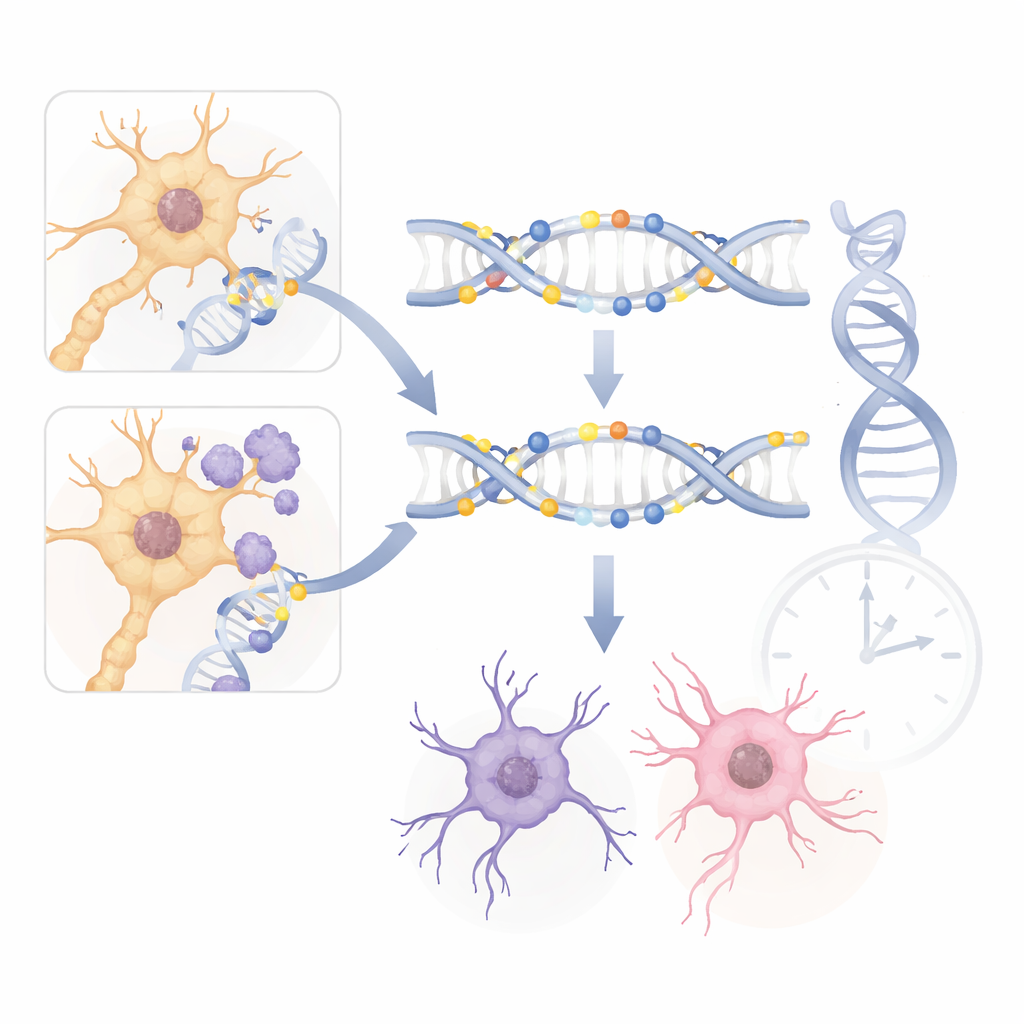
Что это значит для будущих методов лечения
Для неспециалиста главный вывод таков: изменения в мозге, связанные с Альцгеймером, оставляют обнаруживаемый химический след на ДНК задолго до появления симптомов. Особо клубки тау ассоциируются с широкими сдвигами метилирования, которые коррелируют с тяжестью болезни и ускоренным молекулярным старением. Бляшки амилоид-бета вызывают собственный набор изменений, особенно в иммунных и энергетических путях. Поскольку многие из этих эпигенетических сигнатур повторяются и в человеческом мозге, они могут помочь ученым найти ранние биомаркеры или разработать препараты, которые смещают вредные генетические программы в сторону более здорового состояния. Это исследование пока не дает лекарства, но прокладывает более детальную молекулярную дорожную карту от накопления белков до повреждения нейронов, приближая исследователей к новым способам замедлить или предотвратить болезнь Альцгеймера.
Цитирование: Leung, S.K., Walker, E.M., Policicchio, S. et al. Methylomic signatures of tau and amyloid-beta in transgenic mouse models of Alzheimer’s disease neuropathology. npj Dement. 2, 23 (2026). https://doi.org/10.1038/s44400-026-00074-y
Ключевые слова: Болезнь Альцгеймера, эпигенетика, метилирование ДНК, тау и амилоид-бета, мышиные модели