Clear Sky Science · sv
Metylografiska signaturer för tau och amyloid‑beta i transgena musmodeller av Alzheimers sjukdoms neuropatologi
Varför denna forskning är viktig för förståelsen av minnesförlust
Alzheimers sjukdom berövar människor gradvis minnet och självständigheten, men vi förstår fortfarande inte fullt ut vad som driver skadorna inne i hjärnan. Denna studie undersöker små kemiska markörer på DNA, kallade metyleringsmarkörer, i musmodeller som efterliknar centrala drag hos Alzheimers. Genom att följa hur dessa markörer förändras i takt med att skadliga tau‑trassel och amyloid‑beta‑plack byggs upp vill forskarna identifiera tidiga varningssignaler och potentiella nya mål för behandling långt innan nervceller dör. 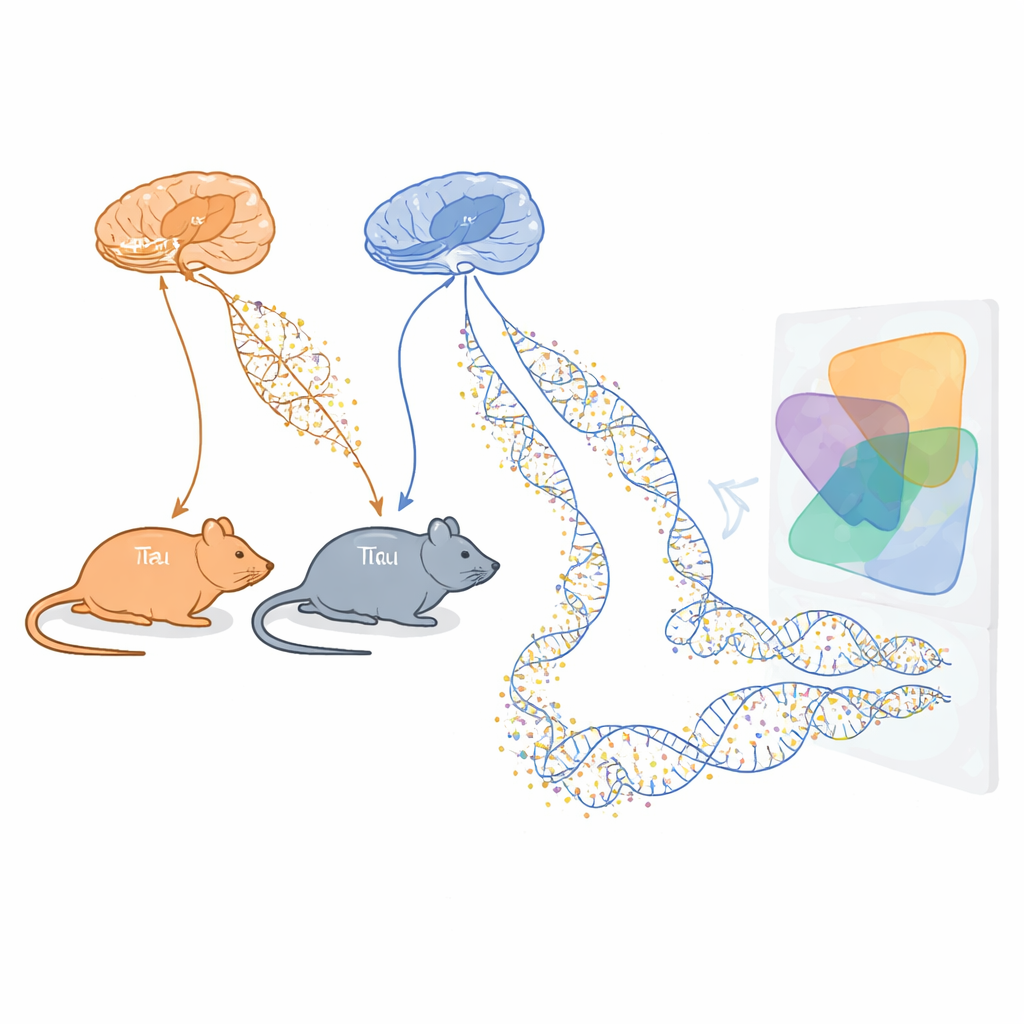
Två musers motsvarighet till människans Alzheimer
Forskargruppen använde två väletablerade muslinjer som vardera modellerar en huvudaspekt av Alzheimers sjukdom. Den ena, kallad rTg4510, producerar ett onormalt humant tau‑protein som bildar trassel inne i nervceller. Den andra, kallad J20, bär mutationer som leder till överskott av amyloid‑beta, ett protein som klumpar ihop sig till plack mellan celler. För båda modellerna samlade forskarna prover från två minneskritiska hjärnregioner, entorhinal cortex och hippocampus, vid flera åldrar som spänner över tidiga till mer avancerade sjukdomsliknande stadier. De mätte sedan DNA‑metylering över mer än en miljon platser i genomet, med både djup sekvensering och en specialanpassad array för att få en bred och tillförlitlig bild av epigenetiska förändringar över tid.
Vad som förändras med tau‑trassel i hjärnan
I tau‑musen förändrades DNA‑metyleringen omfattande, särskilt i gener kopplade till nervcellskommunikation, celldöd och lipidrelaterad signalering i hjärnan. Många platser fick ökad metylering i takt med att tau‑patologin förvärrades, inklusive i gener som hjälper avgöra om neuroner överlever eller genomgår självdöd. Några av dessa gener, såsom de som är involverade i proteinsopningssystem och i att bevara friska synapser, visade också förändringar i aktivitetsnivåer, vilket tyder på att altererad metylering kan bidra till att slå på eller av sjukdomsbanor. Hippocampus, en central nod för minnesbildning, visade ännu mer uttalade metyleringsförändringar än entorhinal cortex, och dess "epigenetiska ålder" verkade äldre än väntat, vilket antyder att tau kan påskynda molekylär åldrande i denna sårbara region.
Hur amyloid‑beta‑plack lämnar ett annat avtryck
Tvärtom visade amyloid‑beta‑musen färre och generellt mindre metyleringsförändringar, och dessa var mer tydligt kopplade till immunreaktioner och cellernas energiproduktion. Platser i närheten av gener involverade i inflammation, mitokondriell hälsa och synapsstruktur påverkades särskilt när placken ackumulerades. Mönstren skilde sig kraftigt mellan entorhinal cortex och hippocampus, vilket antyder att amyloid‑betas epigenetiska effekter är mer regionsspecifika och kanske mer beroende av lokala celltyper eller tidpunkt än taus effekter. Tillsammans tyder de två modellerna på att hjärnan svarar på tau‑trassel och amyloid‑beta‑plack genom överlappande men distinkta molekylära vägar, där tau har ett bredare avtryck på genomet.
Delade epigenetiska fingeravtryck mellan möss och människor
För att testa om fynden i möss verkligen speglar mänsklig sjukdom jämförde forskarna sina resultat med stora studier av DNA‑metylering i mänskliga Alzheimers‑hjärnor. De fann slående överlappningar. Nyckelgener såsom ANK1 och PRDM16 visade liknande metyleringsförskjutningar i musmodellerna och i hjärnvävnad från personer med Alzheimer. Många delade förändringar förekom i icke‑neuronala stödjeceller, vilket överensstämmer med mänskliga data som framhäver gliacellers roll i sjukdomsprogressionen. Dessa ekon över arter tyder på att musens metyleringsmönster inte bara är biprodukter av genetisk manipulation, utan fångar kärnmekanismer som också är verksamma i människohjärnor. 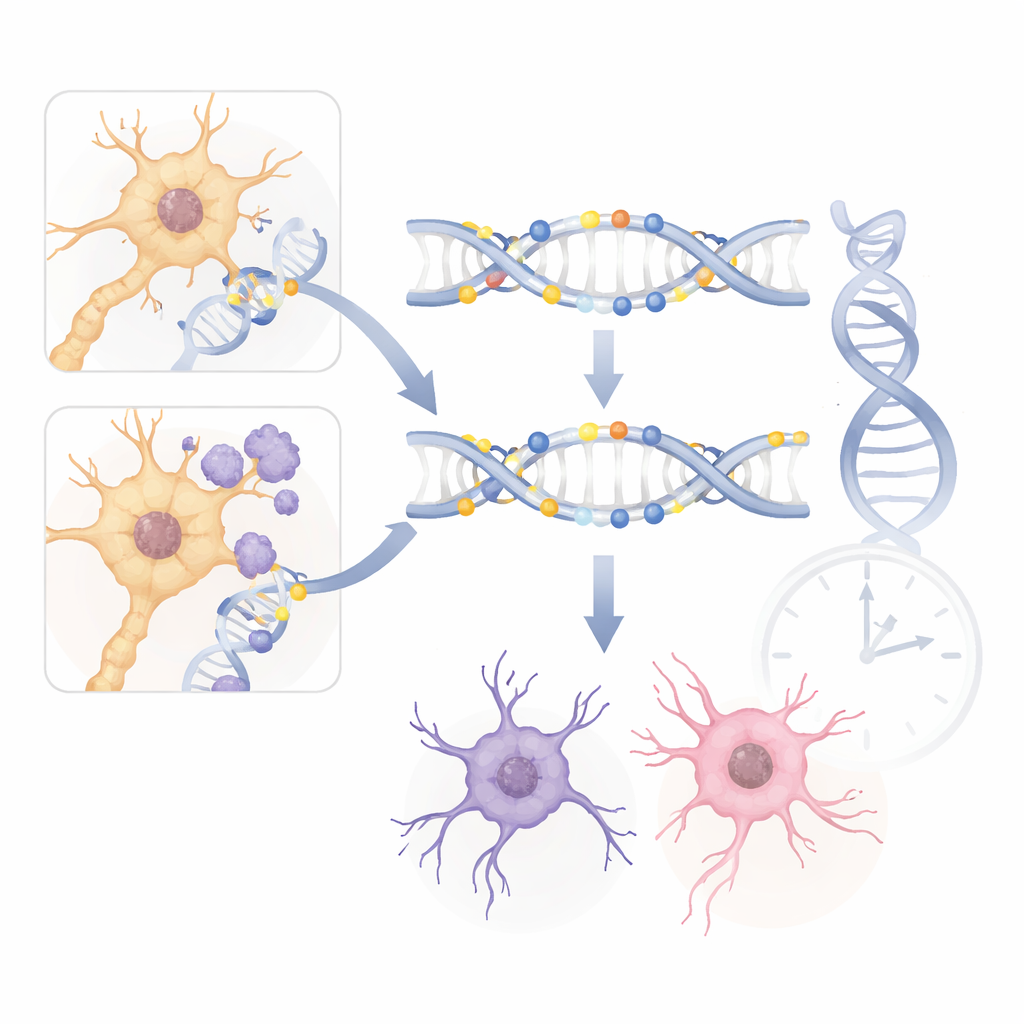
Vad allt detta betyder för framtida behandlingar
För en lekmannaläsare är huvudbudskapet att Alzheimers‑relaterade hjärnförändringar lämnar ett detekterbart kemiskt avtryck på DNA långt innan symtom uppträder. Tau‑trassel är särskilt förknippade med omfattande skiften i metylering som följer sjukdomens svårighetsgrad och accelererat molekylärt åldrande. Amyloid‑beta‑plack utlöser sitt eget mönster av förändringar, särskilt i immun‑ och energirelaterade vägar. Eftersom många av dessa epigenetiska signaturer speglar dem som ses i mänskliga hjärnor, kan de hjälpa forskare att identifiera tidiga biomarkörer eller att utforma läkemedel som knuffar skadliga genprogram tillbaka mot ett friskare tillstånd. Detta arbete erbjuder ännu inget botemedel, men det kartlägger en mer detaljerad molekylär stig från proteinansamling till nervcellsskada, vilket för forskarna ett steg närmare nya sätt att bromsa eller förebygga Alzheimers sjukdom.
Citering: Leung, S.K., Walker, E.M., Policicchio, S. et al. Methylomic signatures of tau and amyloid-beta in transgenic mouse models of Alzheimer’s disease neuropathology. npj Dement. 2, 23 (2026). https://doi.org/10.1038/s44400-026-00074-y
Nyckelord: Alzheimers sjukdom, epigenetik, DNA‑metylering, tau och amyloid‑beta, musmodeller