Clear Sky Science · es
Firmas metilómicas de la tau y la beta-amiloide en modelos de ratón transgénicos de la neuropatología de la enfermedad de Alzheimer
Por qué esta investigación importa para entender la pérdida de memoria
La enfermedad de Alzheimer va robando lentamente la memoria y la independencia de las personas, pero aún no comprendemos por completo qué impulsa el daño dentro del cerebro. Este estudio examina pequeñas etiquetas químicas en el ADN, llamadas marcas de metilación, en modelos de ratón que replican características centrales del Alzheimer. Al seguir cómo cambian estas marcas a medida que se acumulan ovillos dañinos de tau y placas de beta-amiloide, los investigadores pretenden descubrir señales de alerta tempranas y posibles nuevos objetivos terapéuticos mucho antes de que las células cerebrales mueran. 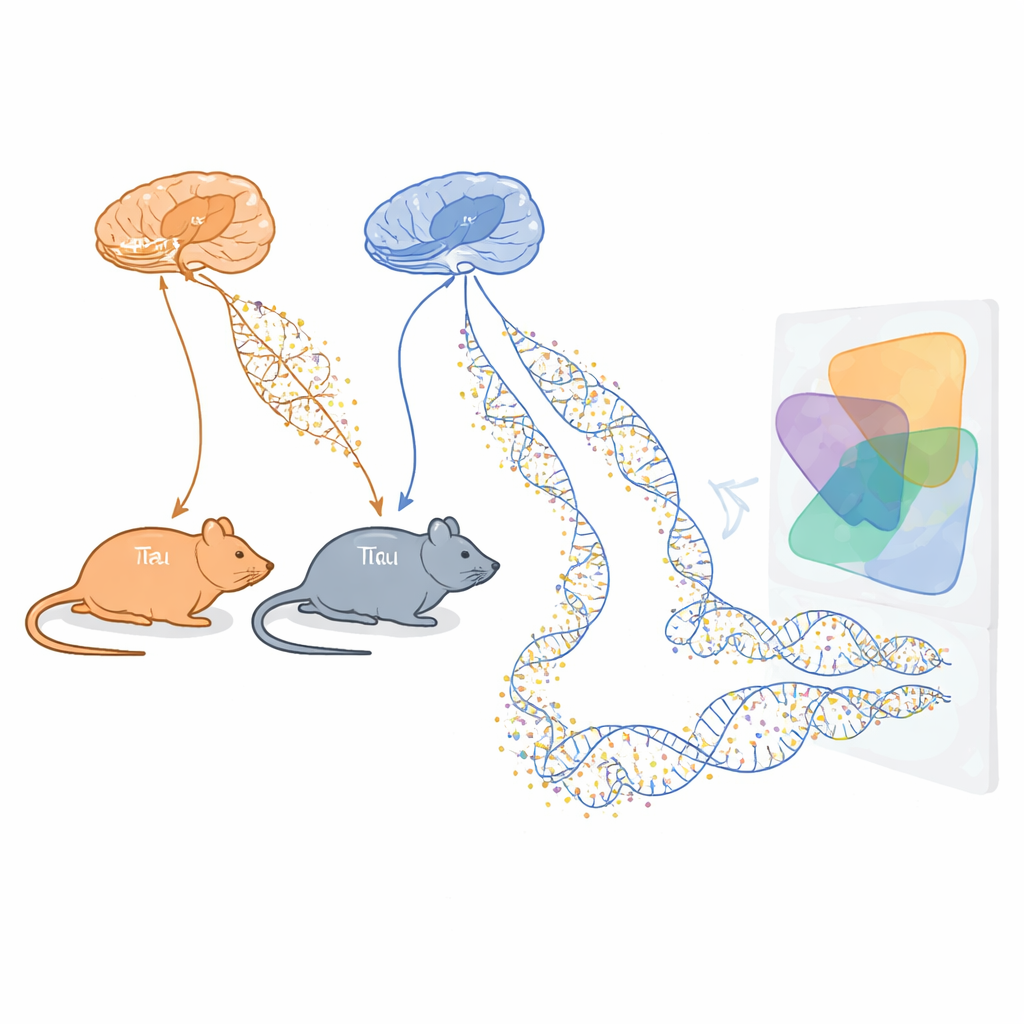
Dos sustitutos de ratón para el Alzheimer humano
El equipo utilizó dos líneas de ratón bien establecidas que cada una modela un aspecto principal de la enfermedad de Alzheimer. Una, llamada rTg4510, produce una proteína humana tau anormal que forma ovillos dentro de las neuronas. La otra, llamada J20, porta mutaciones que provocan un exceso de beta-amiloide, una proteína que se agrupa en placas entre las células. Para ambos modelos, los científicos recogieron muestras de dos regiones cerebrales críticas para la memoria, la corteza entorrinal y el hipocampo, a varias edades que abarcan desde etapas tempranas hasta fases más avanzadas similares a la enfermedad. Luego midieron la metilación del ADN en más de un millón de sitios del genoma, usando tanto secuenciación profunda como una matriz personalizada para obtener una visión amplia y fiable de los cambios epigenéticos a lo largo del tiempo.
Qué cambia con los ovillos de tau en el cerebro
En el ratón con tau, la metilación del ADN cambió de forma extensa, especialmente en genes relacionados con la comunicación neuronal, la muerte celular y las señales lipídicas en el cerebro. Muchos sitios ganaron metilación a medida que la patología de tau empeoraba, incluyendo genes que ayudan a controlar si las neuronas sobreviven o se autodestruyen. Algunos de estos genes, como los implicados en los sistemas de eliminación de proteínas y en el mantenimiento de sinapsis saludables, también mostraron cambios en sus niveles de actividad, lo que sugiere que la metilación alterada puede contribuir a activar o desactivar vías relacionadas con la enfermedad. El hipocampo, un eje clave para la formación de recuerdos, presentó cambios de metilación aún más pronunciados que la corteza entorrinal, y su «edad epigenética» pareció mayor de lo esperado, lo que insinúa que la tau puede acelerar el envejecimiento molecular de esta región vulnerable.
Cómo las placas de beta-amiloide dejan una huella distinta
En contraste, el ratón con beta-amiloide mostró cambios de metilación menos numerosos y, en general, de menor magnitud, y estos estuvieron más relacionados con respuestas inmunitarias y con las «centrales energéticas» dentro de las células. Se vieron afectados de forma particular los sitios cercanos a genes implicados en la inflamación, la salud mitocondrial y la estructura sináptica a medida que se acumulaban las placas. Los patrones diferían claramente entre la corteza entorrinal y el hipocampo, lo que implica que los efectos epigenéticos de la beta-amiloide son más específicos por región y quizá más dependientes del tipo celular local o del momento que los de la tau. En conjunto, los dos modelos sugieren que el cerebro responde a los ovillos de tau y a las placas de beta-amiloide mediante rutas moleculares solapadas pero distintas, con la tau dejando una huella más amplia en el genoma.
Huellas epigenéticas compartidas entre ratones y humanos
Para comprobar si los hallazgos en ratón reflejan realmente la enfermedad humana, los investigadores compararon sus resultados con grandes estudios de metilación del ADN en cerebros humanos con Alzheimer. Encontraron solapamientos llamativos. Genes clave como ANK1 y PRDM16 mostraron cambios de metilación similares en los modelos de ratón y en tejido cerebral de personas con Alzheimer. Muchos de los cambios compartidos se produjeron en células de soporte no neuronales, coincidiendo con datos humanos que destacan el papel de las células gliales en la progresión de la enfermedad. Estos ecos entre especies sugieren que los patrones de metilación en ratón no son solo subproductos de la ingeniería genética, sino que capturan mecanismos centrales que también operan en cerebros humanos. 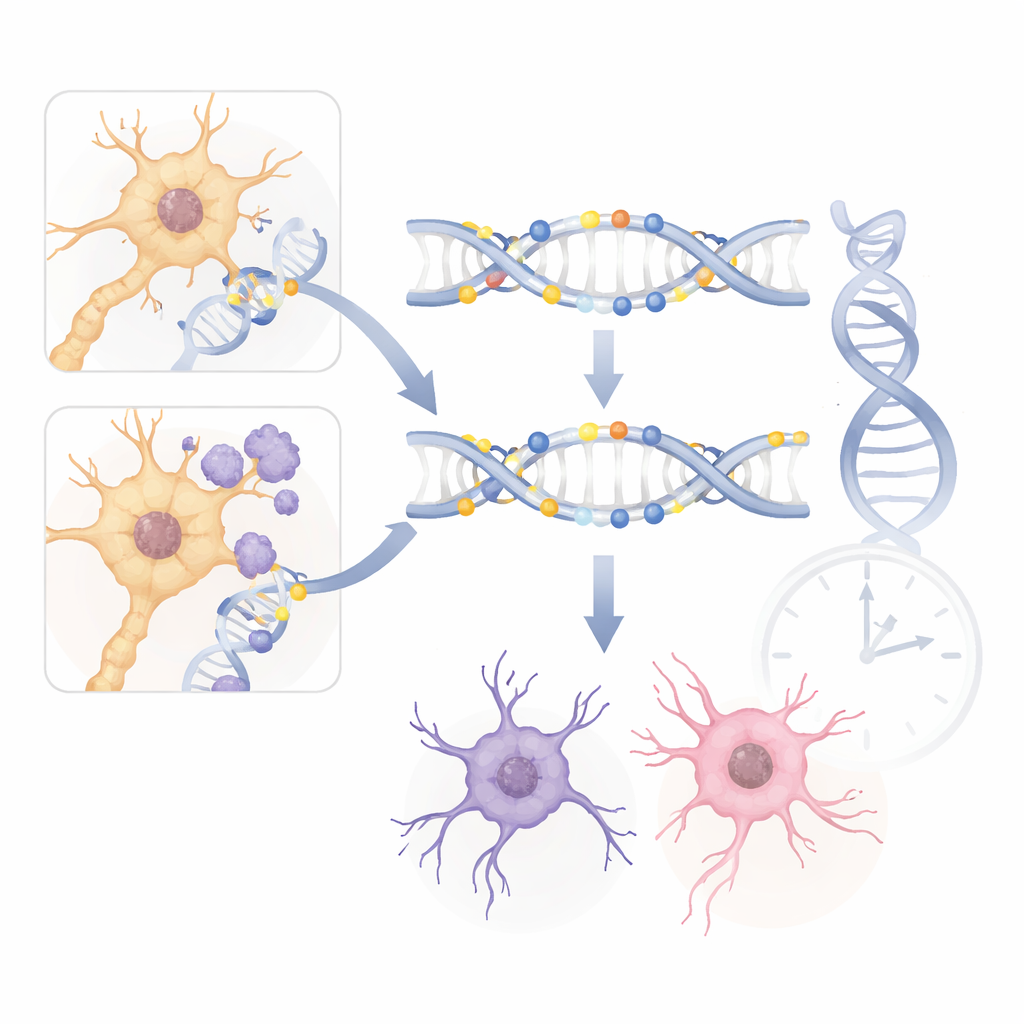
Qué significa todo esto para tratamientos futuros
Para un lector no experto, el mensaje principal es que los cambios cerebrales relacionados con el Alzheimer dejan una huella química detectable en el ADN mucho antes de que aparezcan los síntomas. Los ovillos de tau, en particular, se asocian con cambios generalizados en la metilación que se correlacionan con la gravedad de la enfermedad y con un envejecimiento molecular acelerado. Las placas de beta-amiloide desencadenan su propio conjunto de cambios, especialmente en vías inmunitarias y energéticas. Dado que muchas de estas firmas epigenéticas reflejan las observadas en cerebros humanos, podrían ayudar a los científicos a identificar biomarcadores tempranos o diseñar fármacos que empujen programas génicos dañinos hacia un estado más saludable. Este trabajo aún no ofrece una cura, pero traza una ruta molecular más detallada desde la acumulación proteica hasta el daño celular cerebral, acercando a los investigadores un paso más hacia nuevas formas de ralentizar o prevenir la enfermedad de Alzheimer.
Cita: Leung, S.K., Walker, E.M., Policicchio, S. et al. Methylomic signatures of tau and amyloid-beta in transgenic mouse models of Alzheimer’s disease neuropathology. npj Dement. 2, 23 (2026). https://doi.org/10.1038/s44400-026-00074-y
Palabras clave: Enfermedad de Alzheimer, epigenética, metilación del ADN, tau y beta-amiloide, modelos de ratón