Clear Sky Science · pt
Assinaturas metilômicas de tau e beta-amilóide em modelos transgênicos de camundongo da neuropatologia da doença de Alzheimer
Por que esta pesquisa importa para entender a perda de memória
A doença de Alzheimer rouba gradualmente a memória e a independência das pessoas, mas ainda não compreendemos totalmente o que causa o dano dentro do cérebro. Este estudo examina pequenas marcas químicas no DNA, chamadas marcas de metilação, em modelos de camundongo que reproduzem características centrais do Alzheimer. Ao acompanhar como essas marcas mudam à medida que emaranhados prejudiciais de tau e placas de beta-amilóide se acumulam, os pesquisadores buscam identificar sinais de alerta precoces e potenciais novos alvos terapêuticos muito antes da morte das células cerebrais. 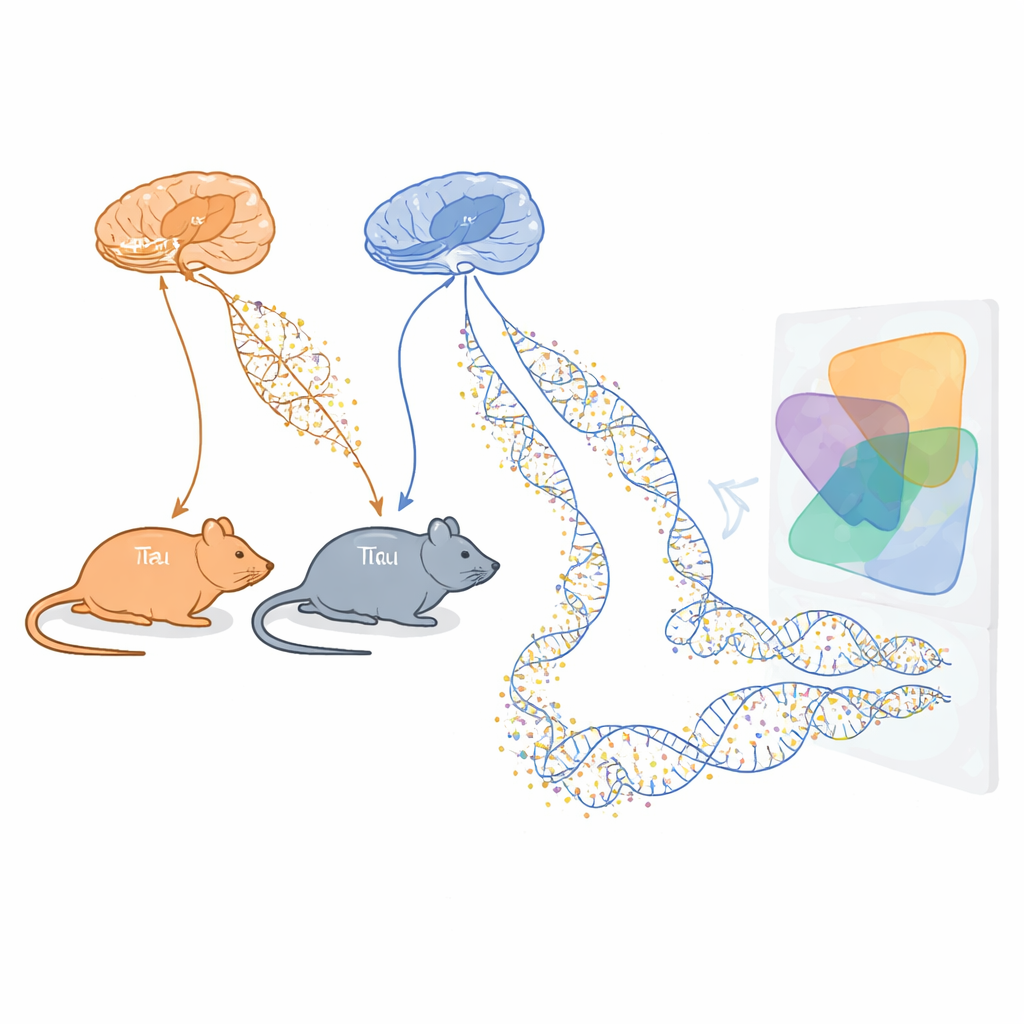
Dois substitutos murinos para o Alzheimer humano
A equipe usou duas linhagens bem estabelecidas de camundongos que modelam cada uma um aspecto importante da doença de Alzheimer. Uma, chamada rTg4510, produz uma forma humana anormal da proteína tau que forma emaranhados dentro dos neurônios. A outra, chamada J20, carrega mutações que causam excesso de beta-amilóide, uma proteína que se aglomera em placas entre as células. Para ambos os modelos, os cientistas coletaram amostras de duas regiões cerebrais críticas para a memória, o córtex entorrinal e o hipocampo, em várias idades cobrindo estágios iniciais e mais avançados semelhantes à doença. Em seguida, mediram a metilação do DNA em mais de um milhão de sítios no genoma, usando tanto sequenciamento profundo quanto um array personalizado para obter uma visão ampla e confiável das mudanças epigenéticas ao longo do tempo.
O que muda com os emaranhados de tau no cérebro
No camundongo com tau, a metilação do DNA mudou extensivamente, especialmente em genes ligados à comunicação entre neurônios, morte celular e sinais relacionados a lipídios no cérebro. Muitos sítios ganharam metilação à medida que a patologia de tau piorava, inclusive em genes que ajudam a controlar se os neurônios sobrevivem ou se autodestroem. Alguns desses genes, como os envolvidos em sistemas de eliminação de proteínas e na manutenção de sinapses saudáveis, também apresentaram alterações nos níveis de atividade, sugerindo que a metilação alterada pode ajudar a ligar ou desligar vias relacionadas à doença. O hipocampo, um centro-chave para a formação de memórias, mostrou mudanças de metilação ainda mais pronunciadas do que o córtex entorrinal, e sua "idade epigenética" aparentou ser mais velha do que o esperado, insinuando que a tau pode acelerar o envelhecimento molecular dessa região vulnerável.
Como as placas de beta-amilóide deixam uma marca diferente
Em contraste, o camundongo com beta-amilóide apresentou mudanças de metilação menos numerosas e, em geral, menores, e estas estiveram mais fortemente associadas a respostas imunes e às usinas de energia dentro das células. Sítios próximos a genes envolvidos em inflamação, saúde mitocondrial e estrutura sináptica foram particularmente afetados à medida que as placas se acumulavam. Os padrões diferiram fortemente entre córtex entorrinal e hipocampo, o que implica que os efeitos epigenéticos da beta-amilóide são mais específicos por região e talvez mais dependentes do tipo celular local ou do tempo do que os efeitos da tau. Juntos, os dois modelos sugerem que o cérebro responde aos emaranhados de tau e às placas de beta-amilóide por meio de rotas moleculares sobrepostas, porém distintas, com a tau deixando uma pegada mais ampla no genoma.
Impressões epigenéticas compartilhadas entre camundongos e humanos
Para testar se as descobertas em camundongos realmente refletem a doença humana, os pesquisadores compararam seus resultados com grandes estudos de metilação do DNA em cérebros humanos com Alzheimer. Eles encontraram sobreposições marcantes. Genes-chave, como ANK1 e PRDM16, mostraram mudanças de metilação semelhantes em modelos murinos e em tecido cerebral de pessoas com Alzheimer. Muitas mudanças compartilhadas ocorreram em células de suporte não neuronais, em consonância com dados humanos que destacam o papel das células gliais na progressão da doença. Esses ecos entre espécies sugerem que os padrões de metilação observados nos camundongos não são apenas subprodutos da engenharia genética, mas capturam mecanismos centrais que também operam em cérebros humanos. 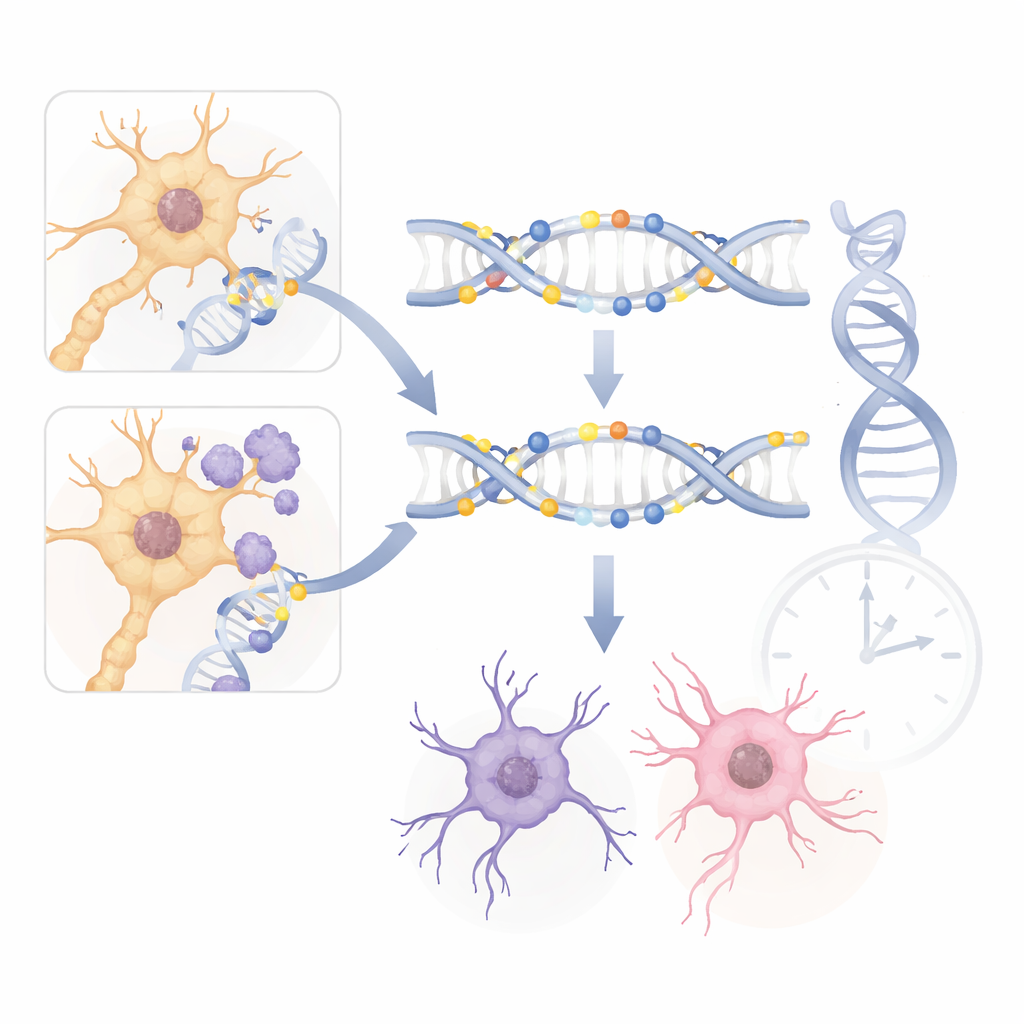
O que tudo isso significa para tratamentos futuros
Para um leitor leigo, a mensagem principal é que as alterações cerebrais relacionadas ao Alzheimer deixam uma impressão química detectável no DNA muito antes do aparecimento dos sintomas. Emaranhados de tau, em particular, estão associados a mudanças generalizadas na metilação que acompanham a gravidade da doença e o envelhecimento molecular acelerado. Placas de beta-amilóide desencadeiam seu próprio conjunto de alterações, sobretudo em vias imunes e de energia. Como muitas dessas assinaturas epigenéticas espelham as encontradas em cérebros humanos, elas podem ajudar os cientistas a identificar biomarcadores precoces ou a projetar fármacos que empurrem programas gênicos nocivos de volta a um estado mais saudável. Este trabalho ainda não oferece uma cura, mas mapeia uma trilha molecular mais detalhada do acúmulo de proteínas ao dano nas células cerebrais, aproximando os pesquisadores de novas formas de retardar ou prevenir a doença de Alzheimer.
Citação: Leung, S.K., Walker, E.M., Policicchio, S. et al. Methylomic signatures of tau and amyloid-beta in transgenic mouse models of Alzheimer’s disease neuropathology. npj Dement. 2, 23 (2026). https://doi.org/10.1038/s44400-026-00074-y
Palavras-chave: Doença de Alzheimer, epigenética, metilação do DNA, tau e beta-amilóide, modelos murinos