Clear Sky Science · zh
用刺激响应型生物材料递送生物药物
能辨别药物去向的智能材料
许多现代强效药物从未发挥全部潜力,因为它们在体内四处扩散、作用消失过快或引起严重副作用。本文探讨了一类新型“智能”材料,旨在将药物、蛋白质、基因疗法、疫苗甚至活细胞直接运送到所需位置,并仅在出现合适信号时释放它们。这些响应性递送系统可能使治疗更有效、更温和,并提高患者的可耐受性。
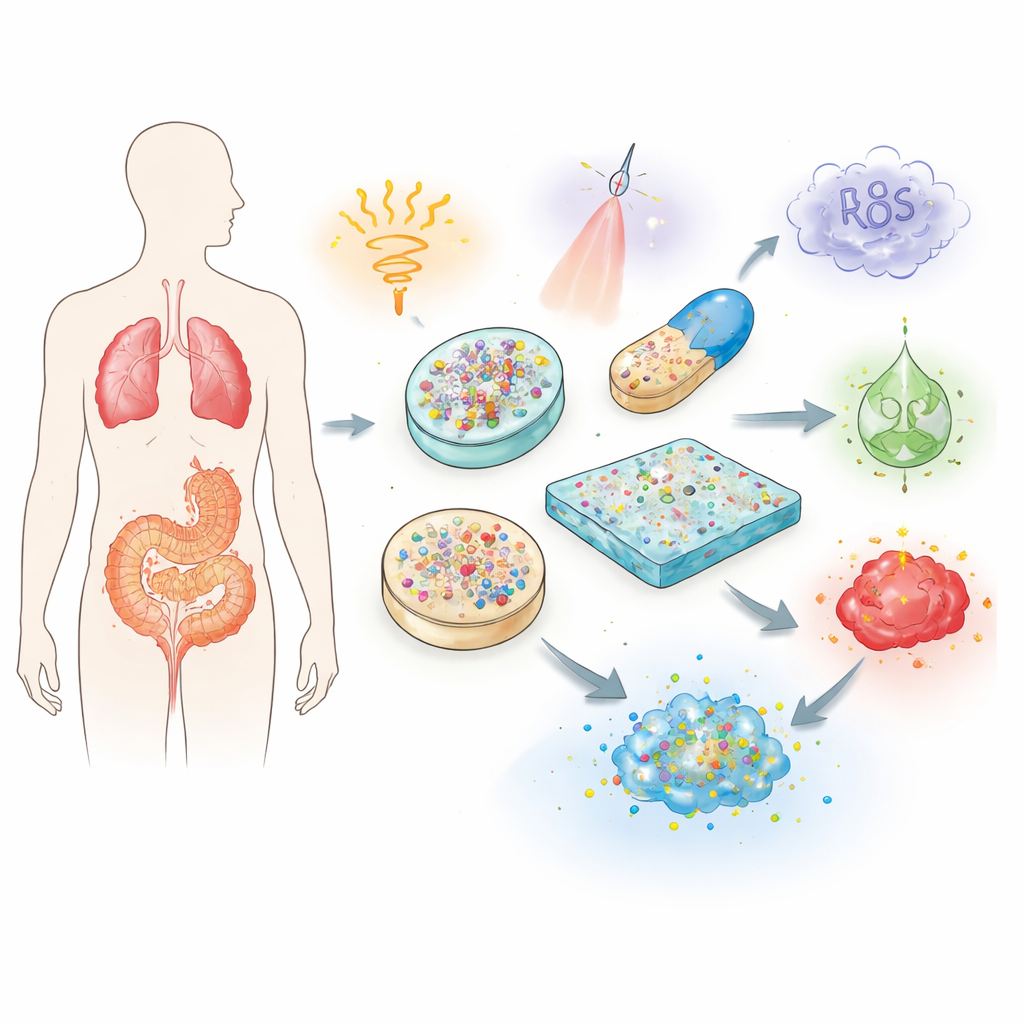
为什么传统治疗需要升级
传统的口服药物和注射剂在体内进行的是大体上无法控制的旅程。大量药物可能在到达肿瘤、发炎关节或受损心脏之前就被分解、排出或被健康器官吸收。为补偿这一点,医生常常开更高剂量或反复给药,从而增加了器官损伤或免疫反应等副作用的风险。综述解释了刺激响应型生物材料如何通过充当保护性运输载体来解决这些问题。由生物相容性聚合物、凝胶和纳米粒子构成,它们可以保护脆弱的载荷,延长在体内的寿命,并精确调控药物何时何地释放。
能“聆听”周围环境的材料
核心思想是赋予材料“感知”周围环境并据此改变行为的能力。作者描述了三大类触发机制。物理信号如热、光、磁场和超声可从体外施加,在选定时刻开启或关闭释放。化学信号如酸度、氧化还原平衡和盐度在健康组织与病变组织间存在差异,使载体只在例如肿瘤的酸性微环境中打开。生物信号包括在特定疾病中升高的酶、葡萄糖和活性氧,它们可以切断材料中的特殊键、软化凝胶或改变溶解性,从而仅在病灶处释放药物。一些先进系统甚至结合多种触发器以获得更精确的控制。
智能载体如何导航并释放治疗物
除了感知外,这些材料还被设计用于在体内导航并与细胞相互作用。它们的表面可以修饰短肽、抗体或其他结合剂,以识别癌细胞、发炎组织或特定器官表面的标志,从而将载体引导至目标。被细胞摄取后,巧妙的化学设计帮助它们逃脱细胞内的“垃圾仓”,并将mRNA或CRISPR等基因载荷递送至正确的细胞隔间。通过调节孔隙率、电荷和可降解性,设计者可以实现数周的缓慢稳定释放、由光脉冲或温度变化触发的瞬时释放,或随愈合阶段变化的多步释放模式。在组织层面,特殊涂层帮助颗粒穿过黏液、粘附于创面或避免被免疫系统过快清除。
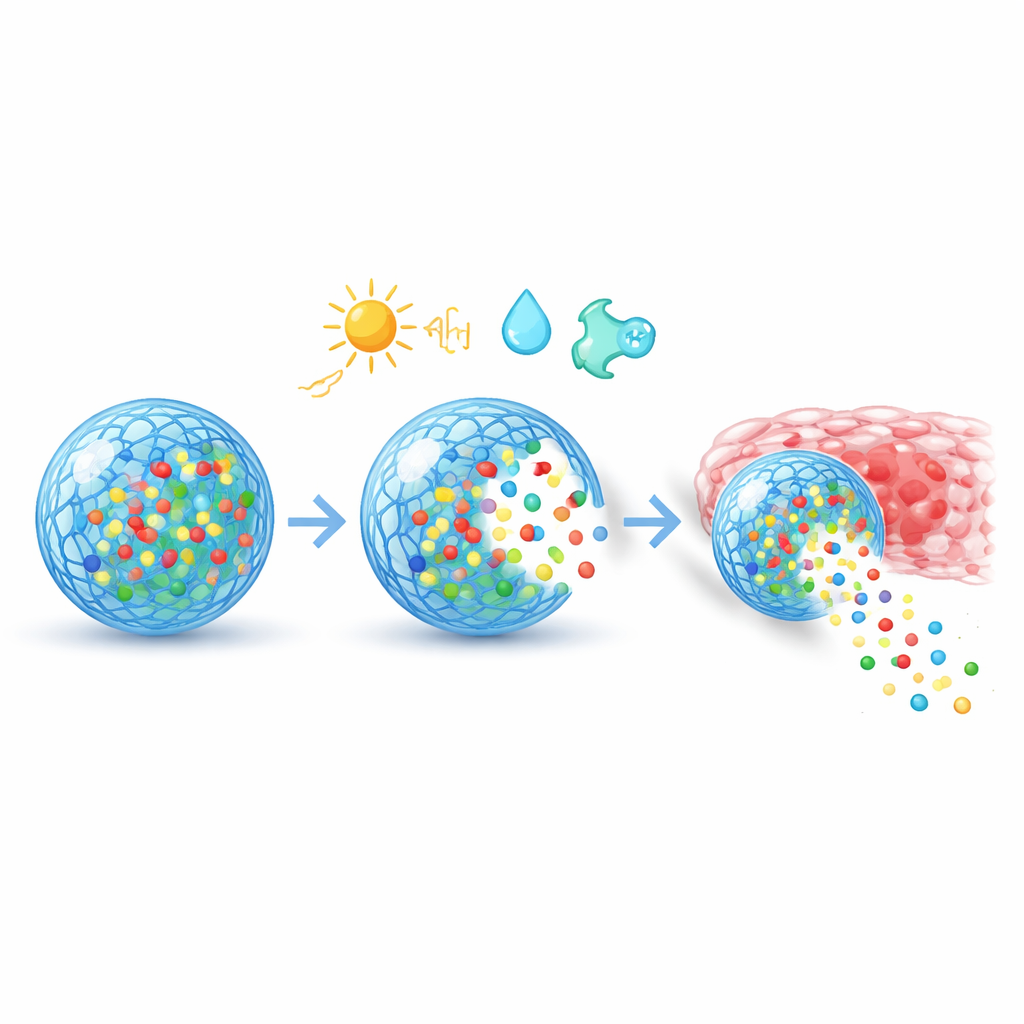
从胰岛素到癌症疫苗的现实应用
综述概述了一系列迅速扩展的实际应用。对于蛋白药物和肽类,热或光响应的植入物和水凝胶可以实现按需给药,减少频繁注射。对pH敏感的颗粒能够暂时打开肠道紧密连接,为口服通常需注射的大分子生物药物提供途径。基因疗法受益于能保护脆弱DNA和RNA并仅在目标细胞内释放的响应性纳米粒子和凝胶。小分子药物,如化疗药物,可装载于对肿瘤中存在的酶或氧化应激有响应的载体中,将治疗浓缩于癌变部位。在细胞与基因治疗中,工程支架和保护性涂层改善了移植细胞定位受损器官并在其中存活的能力。对于疫苗与免疫疗法,pH触发的微针贴片和3D打印的免疫细胞支架可控制抗原与免疫信号的出现时机,从而增强且延长保护效果。
前景、障碍与未来道路
对非专业读者而言,结论是这些智能材料像可编程的药物运输车,仅在合适条件下打开货舱门。早期动物研究和一些临床例证表明,这能在癌症护理、糖尿病、伤口愈合和再生医学等领域提高疗效并降低副作用。然而,作者强调关于长期安全性、大规模制造以及这些复杂材料在真实患者多样且不断变化的体内环境中的行为仍有重要问题需解。随着机器学习、先进的3D与4D打印技术以及微型嵌入式传感器融入材料设计,他们预计将出现快速进展。如果这些挑战得到解决,刺激响应型生物材料可能成为未来疗法的基础,使治疗适应每个人的生物学,并在确切的时间与地点递送药物。
引用: Singh, H., Darban, Z., Ebrahimi, A. et al. Delivering biomedicines with stimuli‑responsive biomaterials. Commun Mater 7, 122 (2026). https://doi.org/10.1038/s43246-026-01163-4
关键词: 智能药物递送, 刺激响应型生物材料, 靶向治疗, 纳米医学, 再生医学