Clear Sky Science · tr
Uyarana duyarlı biyomateryallerle biyomedikasyon teslimatı
İlaçların Gitmesi Gereken Yeri Bilen Akıllı Materyaller
Birçok güçlü modern ilaç, vücutta yayılması, çok çabuk etkisini kaybetmesi veya şiddetli yan etkilere yol açması nedeniyle potansiyelini tam olarak kullanamıyor. Bu makale, ilaçları, proteinleri, gen tedavilerini, aşıları ve hatta canlı hücreleri ihtiyaç duyulan yere doğrudan taşıyıp yalnızca doğru sinyal ortaya çıktığında salacak şekilde tasarlanmış yeni bir “akıllı” materyal sınıfını inceliyor. Bu tepkiye duyarlı teslimat sistemleri, tedavileri daha etkili, daha nazik ve hastaların yaşamını kolaylaştıracak biçimde sunabilir.
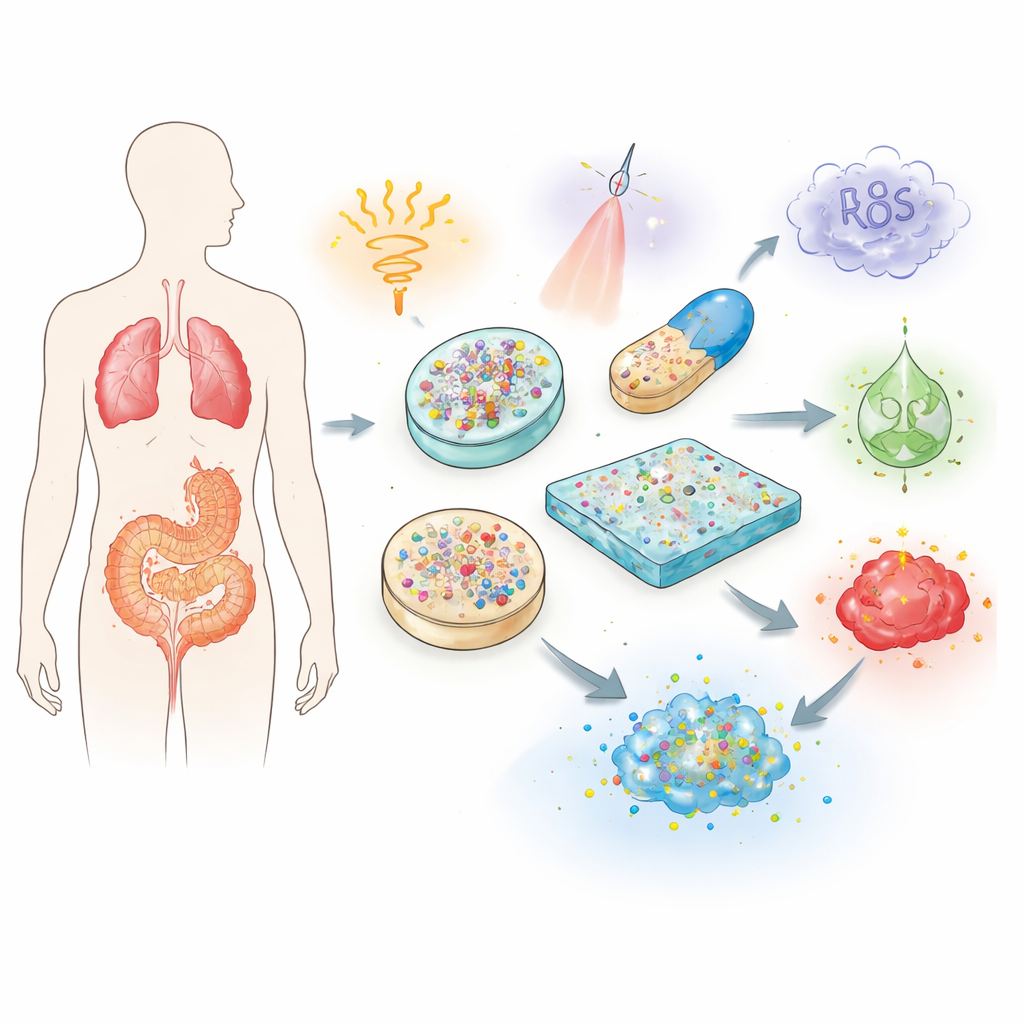
Geleneksel Tedavilerin Neden Geliştirilmesi Gerekiyor
Geleneksel haplar ve enjeksiyonlar, ilacı vücutta büyük ölçüde kontrolsüz bir yolculuğa gönderir. İlacın çoğu, bir tümöre, iltihaplı bir ekleme veya hasarlı bir kalbe ulaşmadan çok önce parçalanabilir, atılabilir veya sağlıklı organlar tarafından tutulabilir. Telafi amacıyla doktorlar genellikle daha yüksek veya tekrarlı dozlar reçete eder; bu da organ hasarı veya bağışıklık reaksiyonları gibi yan etki riskini artırır. Derleme, uyaran-duyarlı biyomateryallerin bu sorunları koruyucu taşıyıcılar olarak nasıl çözdüğünü açıklar. Biyouyumlu polimerler, jeller ve nanopartiküllerden inşa edilen bu sistemler kırılgan yükleri koruyabilir, vücuttaki ömürlerini uzatabilir ve ilacın ne zaman ve nerede salınacağını ince ayarlayabilir.
Çevresini Dinleyen Materyaller
Temel fikir, bir materyale çevresini “hissetme” ve buna göre davranışını değiştirme yeteneği kazandırmaktır. Yazarlar üç geniş tetikleyici ailesini tanımlar. Isı, ışık, manyetik alanlar ve ultrason gibi fiziksel uyaranlar, vücut dışından uygulanarak salımı seçilen anlarda açıp kapatabilir. Asitlik, redoks dengesi ve tuz seviyeleri gibi kimyasal ipuçları sağlıklı doku ile hastalıklı doku arasında farklılık gösterir; bu, taşıyıcıların örneğin tümörlerin asidik mikroçevresinde açılmasına olanak tanır. Enzimler, glukoz ve reaktif oksijen türleri gibi biyolojik ipuçları belirli hastalıklarda yükselir; bunlar bir materyaldeki özel bağları kesebilir, jeli yumuşatabilir veya çözünürlüğünü değiştirerek ilacı yalnızca sorunlu bölgede serbest bırakır. Bazı gelişmiş sistemler daha hassas kontrol sağlamak için birden fazla tetikleyiciyi bile birleştirir.
Akıllı Taşıyıcılar Tedavileri Nasıl Yönlendirir ve Serbest Bırakır
Algılamanın ötesinde, bu materyaller vücutta gezinmek ve hücrelerle etkileşim kurmak üzere tasarlanır. Yüzeyleri, kanser hücreleri, iltihaplı dokular veya belirli organlardaki belirteçleri tanıyan kısa peptitler, antikorlar ya da diğer bağlayıcı ajanlarla donatılabilir ve taşıyıcıları hedeflerine yönlendirir. Hücre tarafından alındıktan sonra, hücre içindeki “çöp kutularından” kaçmalarına ve mRNA veya CRISPR bileşenleri gibi genetik yükleri doğru bölmeye teslim etmelerine yardımcı olan zekice kimyalar kullanılır. Gözeneklilik, yük ve parçalanabilirlik ayarlanarak haftalar boyunca yavaş ve sabit salım, bir ışık darbesi veya sıcaklık değişimiyle tetiklenen ani salım ya da iyileşme evrelerini izleyen çok aşamalı desenler oluşturulabilir. Doku düzeyinde, özel kaplamalar parçacıkların mukustan geçmesini, yaralara yapışmasını veya bağışıklık sistemi tarafından çok çabuk temizlenmeden korunmasını sağlar.
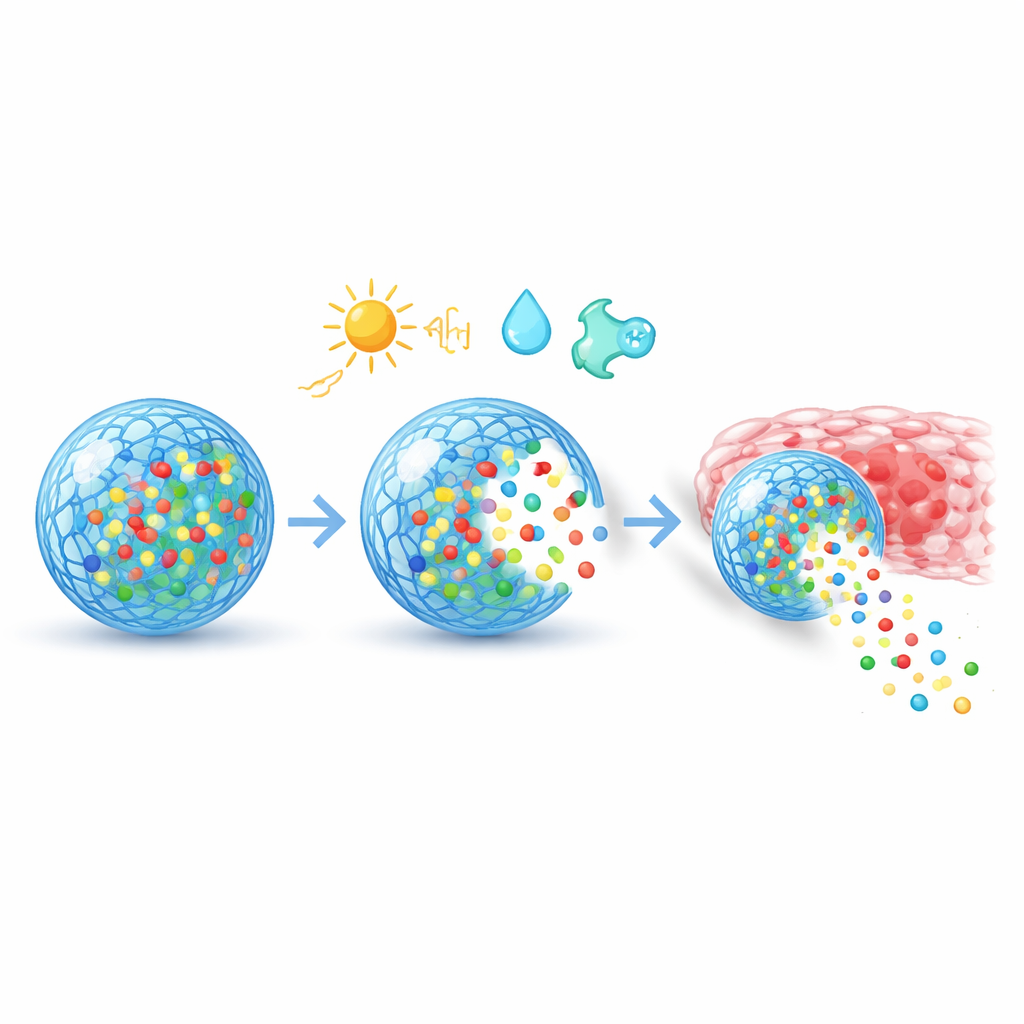
İnsülinden Kanser Aşılarına Gerçek Dünya Kullanımları
Derleme, hızla genişleyen pratik uygulamalar listesini gözden geçirir. Protein ilaçlar ve peptidler için ısıya veya ışığa duyarlı implantlar ve hidrojel sistemleri sık enjeksiyonlara gerek kalmadan isteğe bağlı dozlama sağlayabilir. Bağırsaktaki sıkı bağlantıları geçici olarak açan pH-duyarlı partiküller normalde enjeksiyonla verilen büyük biyolojik ilaçların ağızdan alınmasına bir yol sunar. Gen tedavileri, hassas DNA ve RNA’yı koruyan ve yalnızca hedef hücrelerin içinde serbest bırakan duyarlı nanopartiküller ve jellerden yararlanır. Kemoterapi ajanları gibi küçük moleküllü ilaçlar, tümörlerde bulunan enzimlere veya oksidatif strese yanıt veren taşıyıcılara yüklenir; böylece tedavi kanser bölgesinde yoğunlaşır. Hücre ve gen tedavisinde mühendislik iskeletleri ve koruyucu kaplamalar, nakledilen hücrelerin hasarlı organlara yönelmesini ve orada hayatta kalmasını geliştirir. Aşılar ve immünoterapiler için pH ile tetiklenen mikroiğne yamaları ve 3D yazdırılmış bağışıklık hücresi iskeletleri, antijenlerin ve immün sinyallerin ortaya çıkışını zamanlayarak daha güçlü ve daha uzun süreli koruma sağlayabilir.
Umut, Engeller ve İleriye Dönük Yol
Bir uzman olmayan için çıkarım şu: bu akıllı materyaller, ilaç için programlanabilir teslimat kamyonları gibi davranır; kargo kapaklarını yalnızca doğru koşullar altında açarlar. Erken hayvan çalışmaları ve bazı klinik örnekler bunun kanser bakımı, diyabet, yara iyileşmesi ve rejeneratif tıp alanlarında etkililiği artırıp yan etkileri azaltabileceğini gösteriyor. Ancak yazarlar, uzun vadeli güvenlik, büyük ölçekli üretim ve bu karmaşık materyallerin gerçek hastaların çeşitli ve sürekli değişen ortamlarında nasıl davrandığı konusunda önemli soruların sürdüğünü vurguluyor. Makine öğrenmesi, gelişmiş 3D ve 4D baskı ile küçük gömülü sensörlerin materyal tasarımına entegre edilmesiyle hızlı ilerleme öngörüyorlar. Bu zorluklar aşılırsa, uyaran-duyarlı biyomateryaller her kişinin biyolojisine uyum sağlayan ve tedaviyi tam olarak gerektiği yer ve zamanda teslim eden geleceğin terapilerinin temelini oluşturabilir.
Atıf: Singh, H., Darban, Z., Ebrahimi, A. et al. Delivering biomedicines with stimuli‑responsive biomaterials. Commun Mater 7, 122 (2026). https://doi.org/10.1038/s43246-026-01163-4
Anahtar kelimeler: akıllı ilaç taşıma, uyarana-duyarlı biyomateryaller, hedefe yönelik tedavi, nanotıp, rejeneratif tıp