Clear Sky Science · sv
Leverera biomediciner med stimuli‑responsiva biomaterial
Smarta material som vet vart mediciner ska
Många av dagens kraftfulla läkemedel når aldrig sin fulla potential eftersom de sprids i hela kroppen, verkningslängden blir för kort eller de ger svåra biverkningar. Denna artikel utforskar en ny kategori av "smarta" material som är konstruerade för att bära läkemedel, proteiner, gentekniska behandlingar, vacciner och till och med levande celler direkt till där de behövs, och att bara frige dem när rätt signal uppträder. Dessa responsiva leveranssystem skulle kunna göra behandlingar mer effektiva, mildare och lättare för patienter att leva med.
Varför konventionella behandlingar behöver uppgraderas
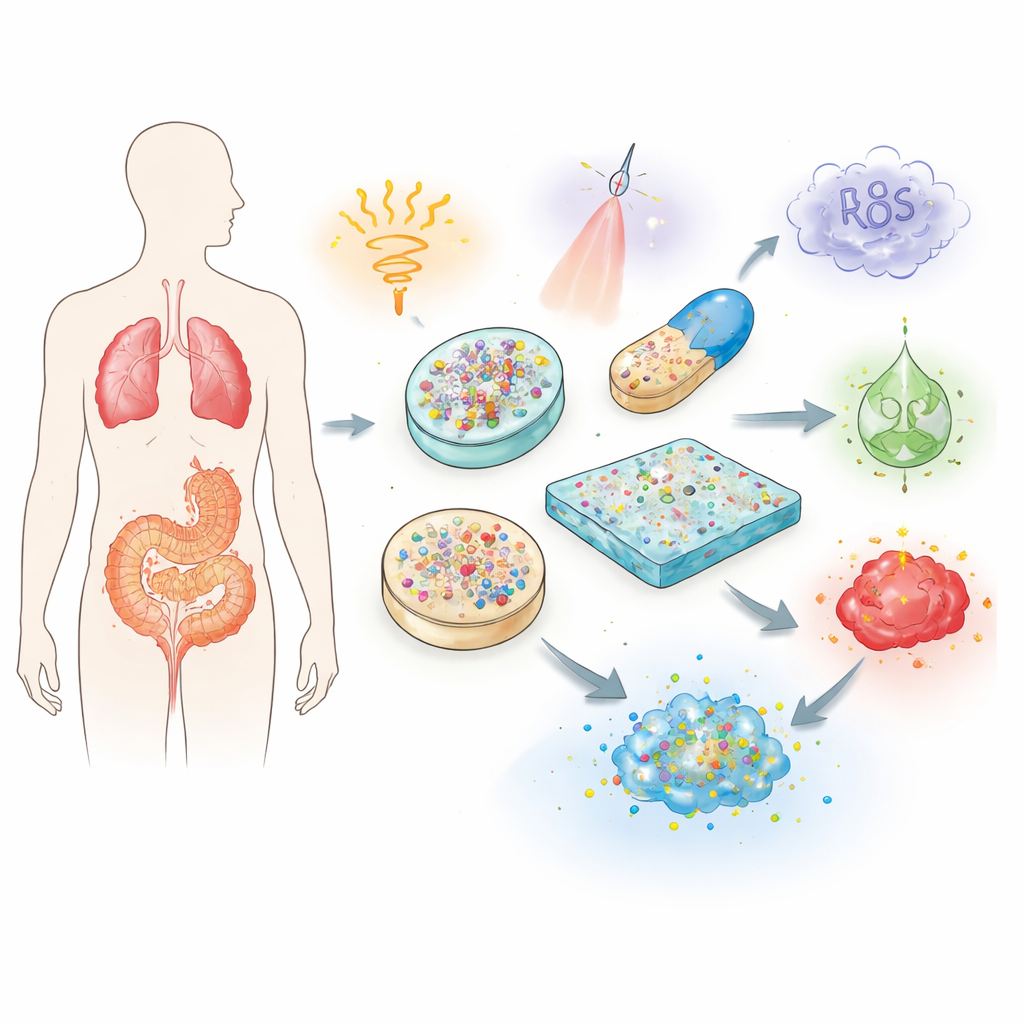
Traditionella tabletter och injektioner skickar läkemedel på en i stort sett okontrollerad resa genom kroppen. Mycket av ett läkemedel kan brytas ner, spolas ut eller tas upp av friska organ långt innan det når en tumör, ett inflammerat led eller ett skadat hjärta. För att kompensera ordinerar läkare ofta högre eller upprepade doser, vilket ökar risken för biverkningar som organskador eller immunreaktioner. Översikten förklarar hur stimuli‑responsiva biomaterial tar sig an dessa problem genom att fungera som skyddande transporter. Byggda av biokompatibla polymerer, geler och nanopartiklar kan de skydda känsliga laster, förlänga deras livslängd i kroppen och finjustera när och var läkemedlet släpps.
Material som lyssnar på sin omgivning
Det centrala är att ge ett material förmågan att "känna" sin omgivning och förändra sitt beteende därefter. Författarna beskriver tre breda familjer av triggerfaktorer. Fysiska signaler som värme, ljus, magnetfält och ultraljud kan appliceras utanför kroppen för att slå på eller av frisättning vid valda tidpunkter. Kemiska signaler som surhetsgrad, redox‑balans och saltnivåer skiljer sig mellan frisk och sjuk vävnad, vilket gör att bärare kan öppna endast i exempelvis den sura mikro‑miljön i tumörer. Biologiska signaler inkluderar enzymer, glukos och reaktiva syrgasarter som är förhöjda vid specifika sjukdomar; dessa kan bryta särskilda bindningar i ett material, mjuka upp en gel eller förändra dess löslighet och därigenom frigöra läkemedlet endast i det drabbade området. Vissa avancerade system kombinerar flera triggers för att uppnå mer precis kontroll.
Hur smarta bärare styr och frigör behandlingar
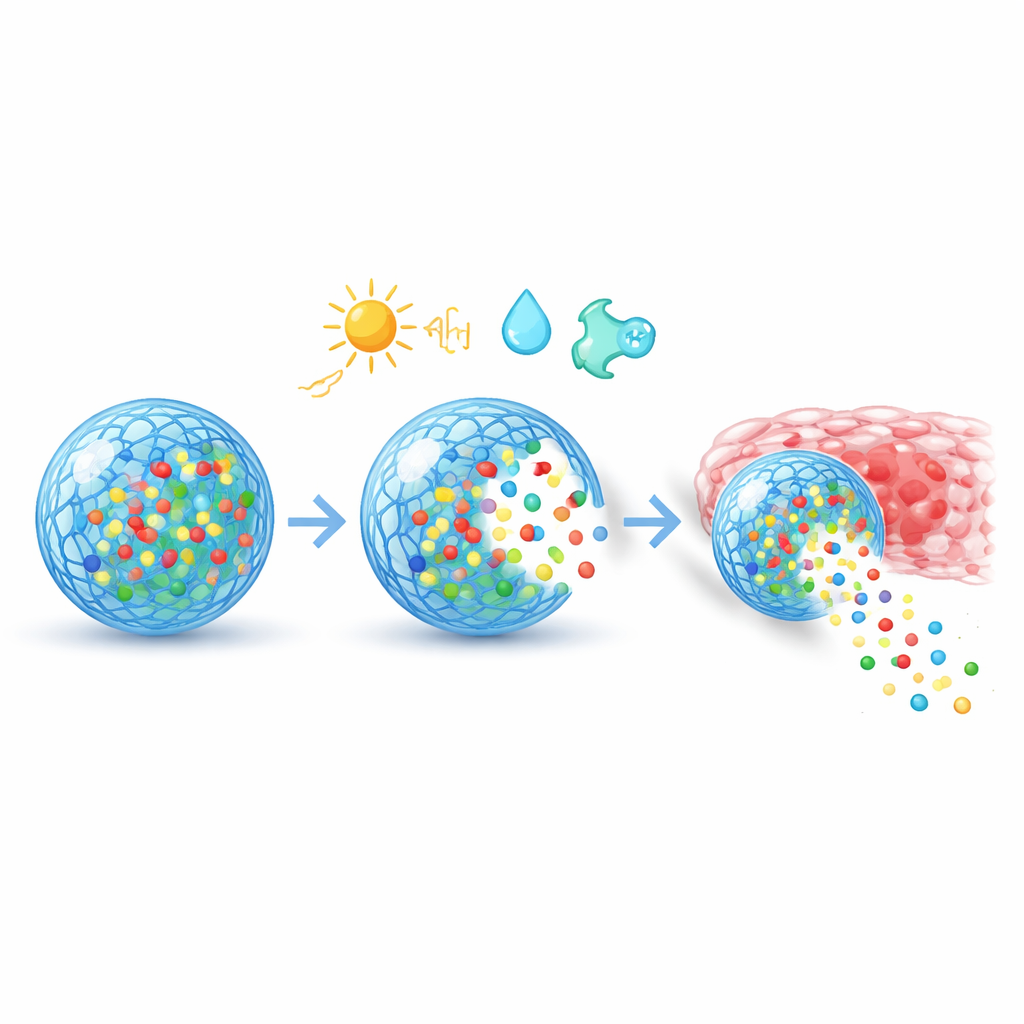
Bortom att känna av omgivningen är dessa material konstruerade för att navigera i kroppen och samverka med celler. Deras ytor kan dekoreras med korta peptider, antikroppar eller andra bindande ämnen som känner igen markörer på cancerceller, inflammerad vävnad eller specifika organ och guidar bärarna till sina mål. När de tas upp av celler hjälper smart kemi dem att undkomma interna "soptunnor" och leverera genetiskt material som mRNA eller CRISPR‑komponenter till rätt fack. Genom att justera porositet, laddning och nedbrytbarhet kan formgivare skapa långsam, jämn frisättning över veckor, skarpa utsläpp utlösta av en ljuspuls eller temperaturförändring, eller flerstegs‑mönster som följer läkningsfaserna. På vävnadsnivå hjälper särskilda beläggningar partiklar att glida genom slem, fästa vid sår eller undvika att snabbt rensas bort av immunsystemet.
Verkliga användningsområden från insulin till cancervacciner
Översikten går igenom en snabbt växande lista av praktiska tillämpningar. För proteintyper och peptider kan värme‑ eller ljus‑responsiva implantat och hydrogeler ge dosering vid behov utan frekventa injektioner. pH‑känsliga partiklar som tillfälligt öppnar tarmens tight junctions erbjuder en väg att svälja stora biologiska läkemedel som normalt måste injiceras. Genterapier gagnas av responsiva nanopartiklar och geler som skyddar känsligt DNA och RNA och sedan släpper dem först inne i mål‑celler. Småmolekylära läkemedel, såsom cytostatika, lastas i bärare som svarar på enzymer eller oxidativ stress i tumörer och koncentrerar behandlingen till cancerstället. Inom cell‑ och genterapi förbättrar konstruerade ställningar och skyddande beläggningar hur transplanterade celler söker sig till skadade organ och överlever där. För vacciner och immunterapier kan pH‑utlösta mikronålspatchar och 3D‑printade immuncell‑stommar tidsstyra framträdandet av antigener och immunsignaler för starkare och mer långvarigt skydd.
löften, hinder och vägen framåt
För en icke‑specialist är slutsatsen att dessa smarta material fungerar som programmerbara leveransfordon för medicin, som öppnar sina lastrum endast under rätt förhållanden. Tidiga djurstudier och några kliniska exempel visar att detta kan öka effektiviteten och minska biverkningar inom cancerbehandling, diabetes, sårhelande och regenerativ medicin. Författarna understryker dock att viktiga frågor återstår kring långtidssäkerhet, storskalig tillverkning och hur dessa komplexa material beter sig i den mångfacetterade, ständigt föränderliga miljön hos verkliga patienter. De förutser snabb utveckling i takt med att maskininlärning, avancerad 3D‑ och 4D‑printning samt små inbyggda sensorer vävs in i materialdesignen. Om dessa utmaningar löses kan stimuli‑responsiva biomaterial bli en grund för framtida terapier som anpassar sig till varje persons biologi och levererar behandling exakt där och när den behövs.
Citering: Singh, H., Darban, Z., Ebrahimi, A. et al. Delivering biomedicines with stimuli‑responsive biomaterials. Commun Mater 7, 122 (2026). https://doi.org/10.1038/s43246-026-01163-4
Nyckelord: smart läkemedelsleverans, stimuli‑responsiva biomaterial, målinriktad terapi, nanomedicin, regenerativ medicin