Clear Sky Science · ru
Доставка биопрепаратов с помощью материалов, реагирующих на стимулы
Умные материалы, которые знают, куда надо доставить лекарство
Многие современные эффективные препараты не раскрывают весь свой потенциал, потому что распространяются по всему организму, слишком быстро теряют активность или вызывают серьёзные побочные эффекты. В этой статье рассматривается новый класс «умных» материалов, предназначенных для переноса лекарств, белков, генетических терапий, вакцин и даже живых клеток прямо в нужное место и для высвобождения их только при появлении соответствующего сигнала. Такие адаптивные системы доставки могут сделать лечение более эффективным, мягким и удобным для пациентов.
Почему традиционным методам нужна модернизация
Обычные таблетки и уколы отправляют лекарство в по сути неконтролируемое путешествие по организму. Значительная часть препарата может разрушиться, вывестись или оказаться в здоровых органах задолго до достижения опухоли, воспалённого сустава или повреждённого сердца. Чтобы компенсировать это, врачи часто назначают более высокие или повторные дозы, что повышает риск побочных эффектов — от повреждения органов до иммунных реакций. Обзор объясняет, как стимул‑чувствительные биоматериалы решают эти проблемы, действуя как защитные транспортёры. Созданные из биосовместимых полимеров, гелей и наночастиц, они могут защищать хрупкое содержимое, продлевать его жизнь в организме и тонко настраивать, когда и где лекарство высвобождается.
Материалы, которые «слушают» окружение
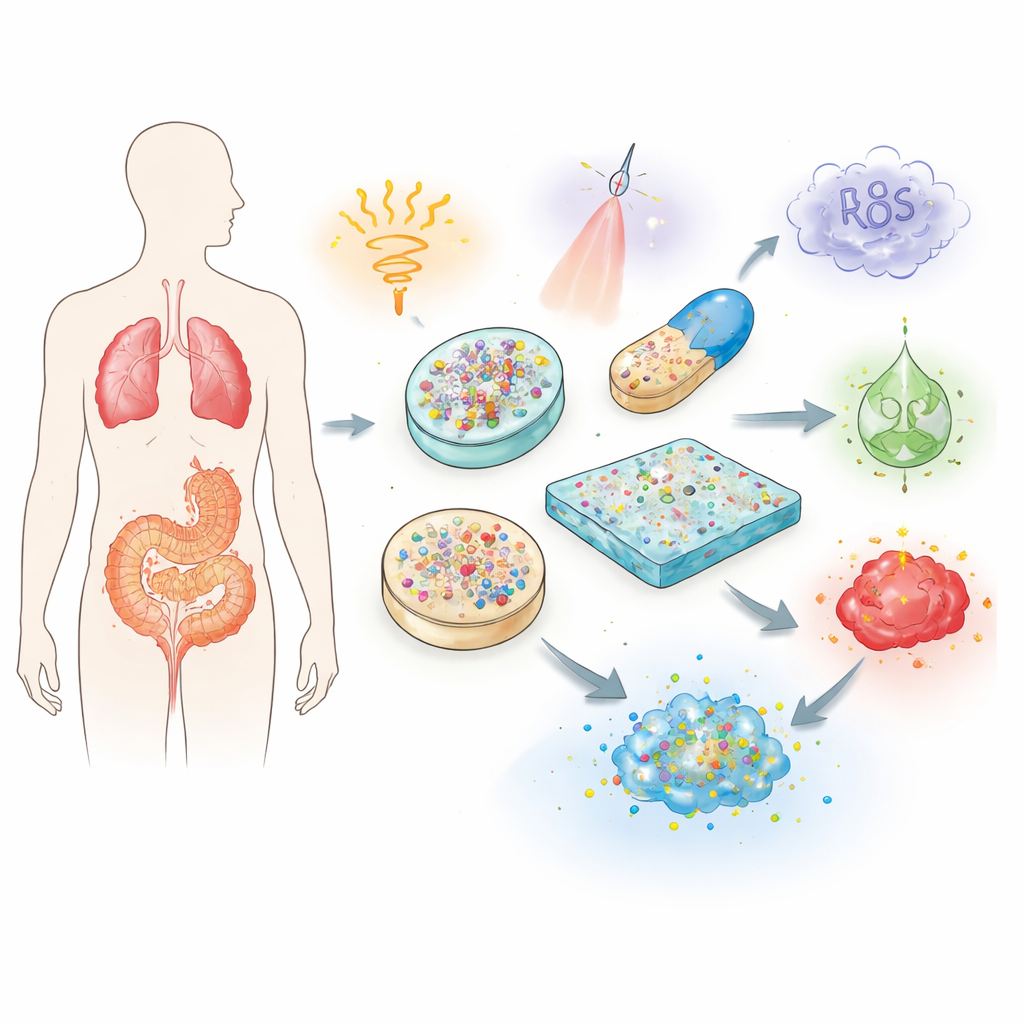
Ключевая идея — наделить материал способностью «чувствовать» окружение и изменять своё поведение соответственно. Авторы описывают три большие группы триггеров. Физические сигналы — тепло, свет, магнитные поля и ультразвук — могут подаваться извне, включая или выключая высвобождение в выбранные моменты. Химические сигналы — кислотность, состояние редокс‑баланса и уровень солей — отличаются в здоровых и поражённых тканях, что позволяет носителям открываться, например, в более кислой микросреде опухолей. Биологические сигналы включают ферменты, глюкозу и реактивные формы кислорода, повышенные при конкретных заболеваниях; они могут разрывать специальные связи в материале, размягчать гель или менять растворимость, освобождая препарат только в проблемной области. Некоторые продвинутые системы комбинируют несколько триггеров для более точного контроля.
Как умные носители направляют и высвобождают препараты
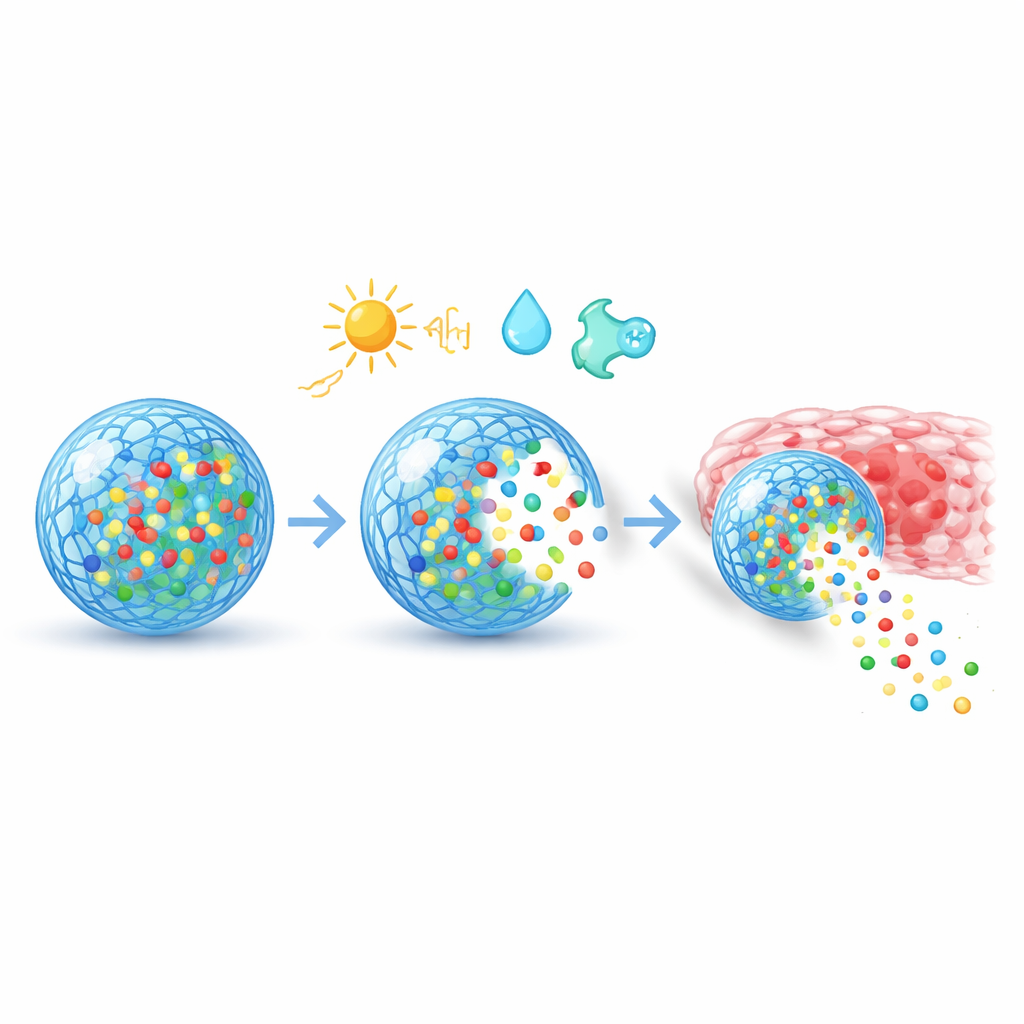
Кроме сенсоров, эти материалы проектируют так, чтобы они могли перемещаться по организму и взаимодействовать с клетками. Их поверхности можно украшать короткими пептидами, антителами или другими связывающими агентами, которые распознают маркеры на раковых клетках, воспалённых тканях или в конкретных органах, направляя носители к месту назначения. После захвата клетками хитрая химия помогает им избежать внутриклеточных «мусорных контейнеров» и доставить генетические грузы, такие как мРНК или компоненты CRISPR, в нужный компартмент. За счёт регулировки пористости, заряда и скорости деградации разработчики создают медленное равномерное высвобождение в течение недель, резкие выбросы, вызванные импульсом света или изменением температуры, или многоступенчатые схемы, соответствующие фазам заживления. На уровне тканей специальные покрытия помогают частицам проходить через слизь, прилипать к ранам или не выводиться слишком быстро иммунной системой.
Реальные применения: от инсулина до противораковых вакцин
Обзор охватывает быстро растущий список практических применений. Для белковых препаратов и пептидов импланты и гидрогели, реагирующие на тепло или свет, могут обеспечивать дозирование по требованию без частых инъекций. Частицы, чувствительные к pH, которые на короткое время открывают плотные контакты кишечного эпителия, предлагают путь для приёма больших биологических молекул перорально, которые обычно требуют инъекций. Генотерапии выигрывают от ответных наночастиц и гелей, защищающих хрупкую ДНК и РНК и высвобождающих их только внутри целевых клеток. Малые молекулы, например химиопрепараты, загружают в носители, реагирующие на ферменты или оксидативный стресс в опухолях, концентрируя лечение в раковой ткани. В клеточной и генной терапии инженерные каркасы и защитные покрытия улучшают приживаемость пересаженных клеток и их нацеливание на повреждённые органы. Для вакцин и иммунотерапии пластыри с микророжками, триггеруемые pH, и 3D‑печатные каркасы для иммунных клеток могут синхронизировать появление антигенов и иммунных сигналов для более мощной и долговременной защиты.
Перспективы, препятствия и дальнейший путь
Главный вывод для неспециалиста в том, что эти умные материалы действуют как программируемые грузовики для лекарств, открывающие грузовые отсеки только при подходящих условиях. Ранние исследования на животных и некоторые клинические примеры показывают, что это может повысить эффективность и снизить побочные эффекты в онкологии, лечении диабета, заживлении ран и регенеративной медицине. Однако авторы подчёркивают, что остаются важные вопросы о долгосрочной безопасности, производстве в крупном масштабе и поведении этих сложных материалов в разнообразной, постоянно меняющейся среде реальных пациентов. Они прогнозируют быстрый прогресс по мере внедрения машинного обучения, продвинутой 3D‑ и 4D‑печати и миниатюрных встроенных сенсоров в дизайн материалов. Если эти задачи будут решены, стимул‑чувствительные биоматериалы могут стать основой будущих терапий, которые адаптируются к биологии каждого человека и доставляют лечение точно туда и в то время, когда это требуется.
Цитирование: Singh, H., Darban, Z., Ebrahimi, A. et al. Delivering biomedicines with stimuli‑responsive biomaterials. Commun Mater 7, 122 (2026). https://doi.org/10.1038/s43246-026-01163-4
Ключевые слова: умная доставка лекарств, стимул‑чувствительные биоматериалы, таргетная терапия, наномедицина, регенеративная медицина