Clear Sky Science · fr
Administration de biomédicaments avec des biomatériaux réactifs aux stimuli
Matériaux intelligents qui savent où les médicaments doivent aller
Beaucoup de médicaments puissants d’aujourd’hui n’exploitent jamais pleinement leur potentiel parce qu’ils se répartissent dans tout le corps, s’estompent trop rapidement ou provoquent des effets secondaires sévères. Cet article explore une nouvelle classe de matériaux « intelligents » conçus pour transporter des médicaments, des protéines, des traitements génétiques, des vaccins et même des cellules vivantes directement là où ils sont nécessaires, et pour les libérer seulement lorsqu’un signal approprié apparaît. Ces systèmes de délivrance réactifs pourraient rendre les traitements plus efficaces, plus doux et plus faciles à vivre pour les patients.
Pourquoi les traitements conventionnels méritent une mise à niveau
Les comprimés et les injections traditionnels envoient le médicament dans un parcours largement incontrôlé à travers le corps. Une grande partie d’un médicament peut être dégradée, éliminée ou absorbée par des organes sains bien avant d’atteindre une tumeur, une articulation enflammée ou un cœur endommagé. Pour compenser, les médecins prescrivent souvent des doses plus élevées ou répétées, augmentant le risque d’effets indésirables tels que des lésions d’organes ou des réactions immunitaires. La revue explique comment les biomatériaux réactifs aux stimuli s’attaquent à ces problèmes en jouant le rôle de navettes protectrices. Fabriqués à partir de polymères biocompatibles, de gels et de nanoparticules, ils peuvent protéger des charges fragiles, prolonger leur durée de vie dans l’organisme et affiner le moment et le lieu de la libération du médicament.
Des matériaux qui écoutent leur environnement
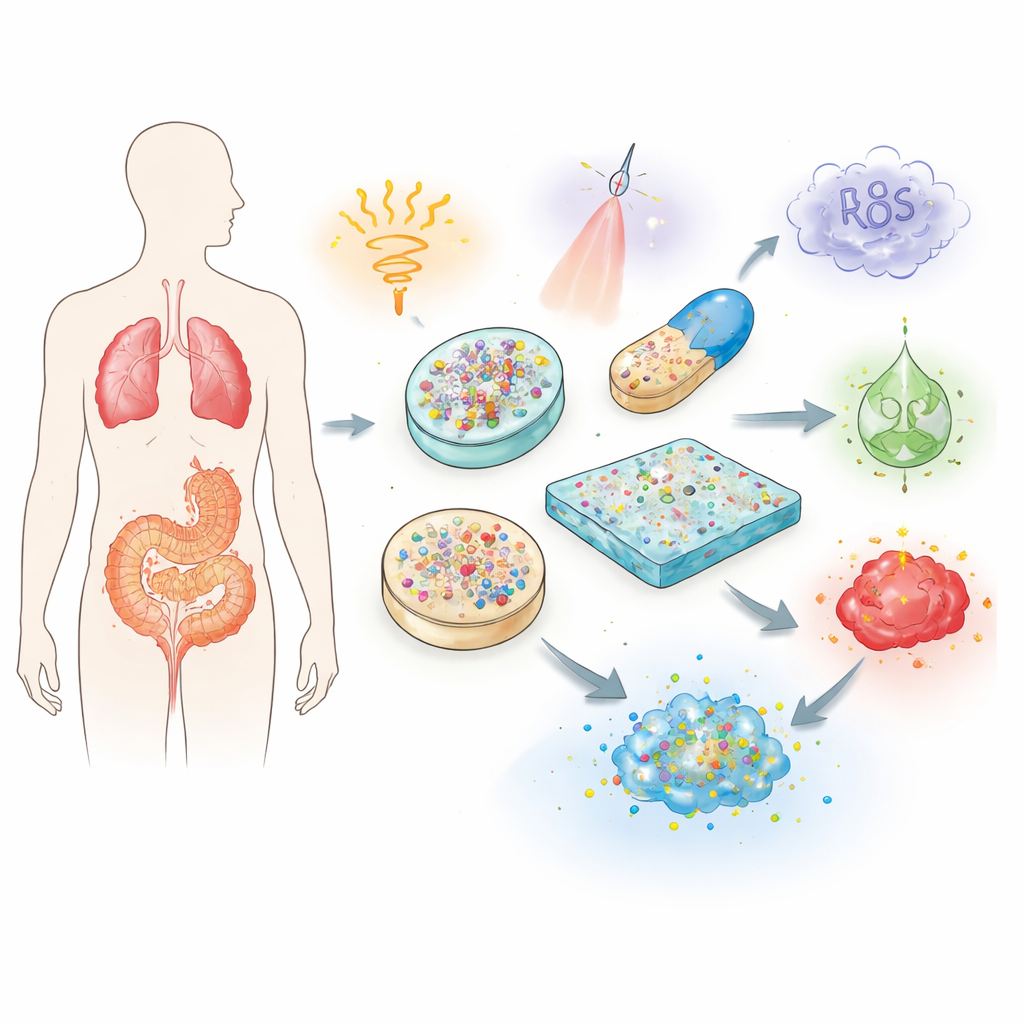
L’idée centrale est de doter un matériau de la capacité à « sentir » son environnement et à modifier son comportement en conséquence. Les auteurs décrivent trois grandes familles de déclencheurs. Les signaux physiques tels que la chaleur, la lumière, les champs magnétiques et les ultrasons peuvent être appliqués de l’extérieur du corps pour activer ou désactiver la libération à des moments choisis. Les signaux chimiques, comme l’acidité, l’équilibre redox et la concentration en sels, diffèrent entre tissus sains et tissus malades, permettant aux vecteurs de s’ouvrir uniquement, par exemple, dans le microenvironnement acide des tumeurs. Les indices biologiques incluent des enzymes, le glucose et les espèces réactives de l’oxygène qui sont élevées dans certaines maladies ; ils peuvent rompre des liaisons spécifiques dans un matériau, ramollir un gel ou modifier sa solubilité, libérant le médicament uniquement dans la zone problématique. Certains systèmes avancés combinent même plusieurs déclencheurs pour obtenir un contrôle plus précis.
Comment les transporteurs intelligents dirigent et libèrent les traitements
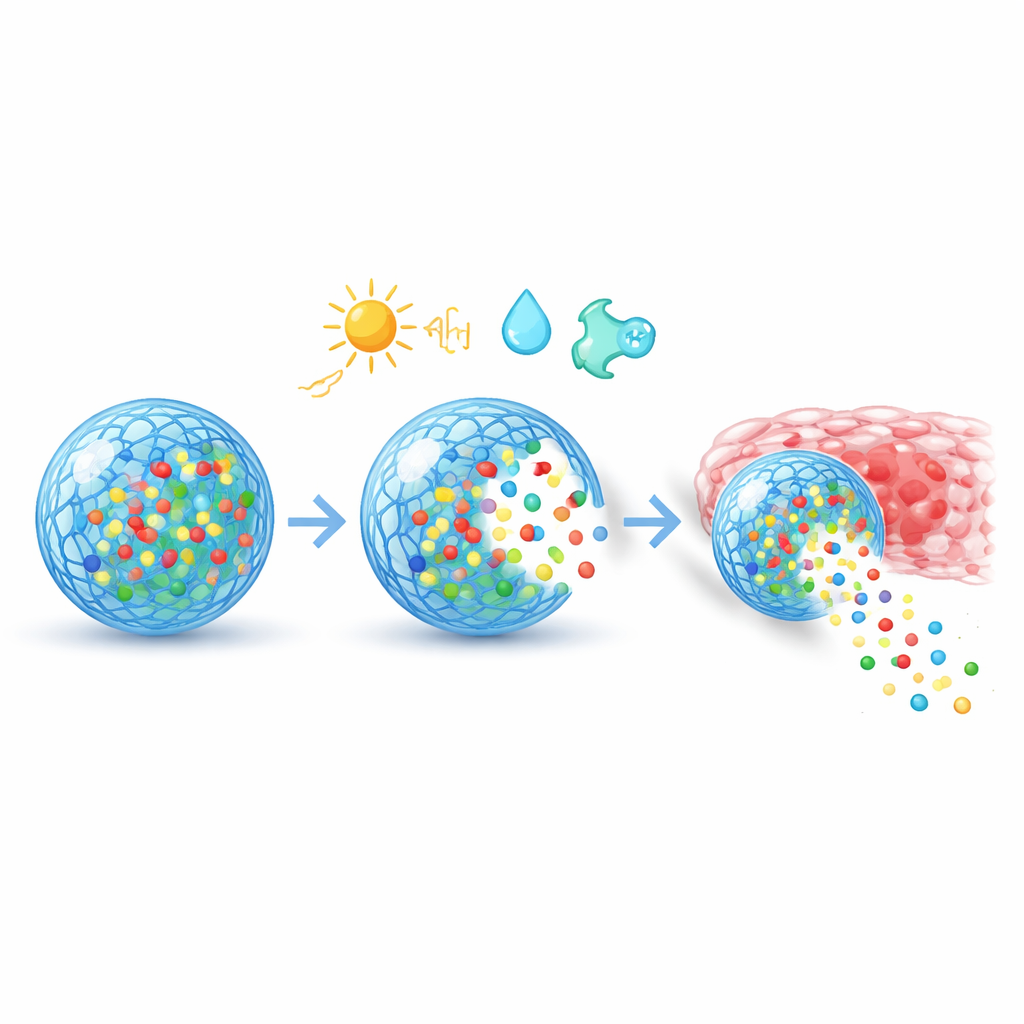
Au-delà de la détection, ces matériaux sont conçus pour naviguer dans l’organisme et interagir avec les cellules. Leurs surfaces peuvent être parées de peptides courts, d’anticorps ou d’autres agents de liaison qui reconnaissent des marqueurs de cellules cancéreuses, de tissus enflammés ou d’organes spécifiques, guidant ainsi les transporteurs vers leurs cibles. Une fois internalisés par les cellules, une chimie ingénieuse les aide à échapper aux « poubelles » internes et à délivrer des cargaisons génétiques comme l’ARNm ou des composants CRISPR vers le compartiment adéquat. En ajustant la porosité, la charge et la dégradabilité, les concepteurs peuvent créer une libération lente et régulière sur des semaines, des poussées nettes déclenchées par une impulsion lumineuse ou un changement de température, ou des schémas à étapes multiples qui suivent les phases de la guérison. Au niveau tissulaire, des revêtements spéciaux aident les particules à traverser le mucus, à adhérer aux plaies ou à éviter d’être éliminées trop rapidement par le système immunitaire.
Applications concrètes, de l’insuline aux vaccins anticancéreux
La revue passe en revue une liste en rapide expansion d’applications pratiques. Pour les médicaments protéiques et les peptides, des implants et hydrogels réactifs à la chaleur ou à la lumière peuvent fournir des doses à la demande sans injections fréquentes. Des particules sensibles au pH qui ouvrent temporairement les jonctions serrées de l’intestin offrent une voie pour avaler de grands médicaments biologiques qui doivent normalement être injectés. Les thérapies géniques tirent parti de nanoparticules et de gels réactifs qui protègent l’ADN et l’ARN fragiles, puis les libèrent uniquement à l’intérieur des cellules cibles. Les petits médicaments, tels que les agents chimiothérapeutiques, sont chargés dans des véhicules répondant aux enzymes ou au stress oxydatif trouvés dans les tumeurs, concentrant le traitement sur le site cancéreux. En thérapie cellulaire et génique, des échafaudages conçus et des revêtements protecteurs améliorent la capacité des cellules transplantées à se diriger vers les organes lésés et à y survivre. Pour les vaccins et les immunothérapies, des patchs à micro-aiguilles déclenchés par le pH et des échafaudages cellulaires imprimés en 3D peuvent programmer l’apparition d’antigènes et de signaux immunitaires pour une protection plus forte et plus durable.
Promesses, obstacles et perspectives
Pour un non-spécialiste, la conclusion est que ces matériaux intelligents agissent comme des camions de livraison programmables pour la médecine, n’ouvrant leurs portes de cargaison que dans les bonnes conditions. Des études animales préliminaires et quelques exemples cliniques montrent que cela peut augmenter l’efficacité et réduire les effets secondaires dans les domaines du cancer, du diabète, de la cicatrisation des plaies et de la médecine régénérative. Toutefois, les auteurs soulignent que des questions importantes subsistent concernant la sécurité à long terme, la production à grande échelle et le comportement de ces matériaux complexes dans l’environnement divers et changeant des patients réels. Ils prévoient des progrès rapides à mesure que l’apprentissage automatique, l’impression avancée 3D et 4D et de minuscules capteurs intégrés seront intégrés à la conception des matériaux. Si ces défis sont relevés, les biomatériaux réactifs aux stimuli pourraient devenir une base pour des thérapies futures qui s’adaptent à la biologie de chaque personne et délivrent le traitement exactement où et quand il est nécessaire.
Citation: Singh, H., Darban, Z., Ebrahimi, A. et al. Delivering biomedicines with stimuli‑responsive biomaterials. Commun Mater 7, 122 (2026). https://doi.org/10.1038/s43246-026-01163-4
Mots-clés: libération intelligente de médicaments, biomatériaux réactifs aux stimuli, thérapie ciblée, nanomédecine, médecine régénérative