Clear Sky Science · de
Biomedikamente liefern mit stimuli‑responsiven Biomaterialien
Intelligente Materialien, die wissen, wohin Medikamente sollen
Viele leistungsfähige moderne Medikamente erreichen nie ihr volles Potenzial, weil sie sich im Körper verteilen, zu schnell abgebaut werden oder starke Nebenwirkungen verursachen. Dieser Artikel untersucht eine neue Klasse „intelligenter“ Materialien, die so konzipiert sind, dass sie Medikamente, Proteine, gentherapeutische Wirkstoffe, Impfstoffe und sogar lebende Zellen direkt dorthin transportieren, wo sie gebraucht werden, und sie nur dann freisetzen, wenn das richtige Signal eintrifft. Diese responsiven Abgabesysteme könnten Behandlungen wirkungsvoller, schonender und für Patienten leichter handhabbar machen.
Warum herkömmliche Behandlungen ein Upgrade brauchen
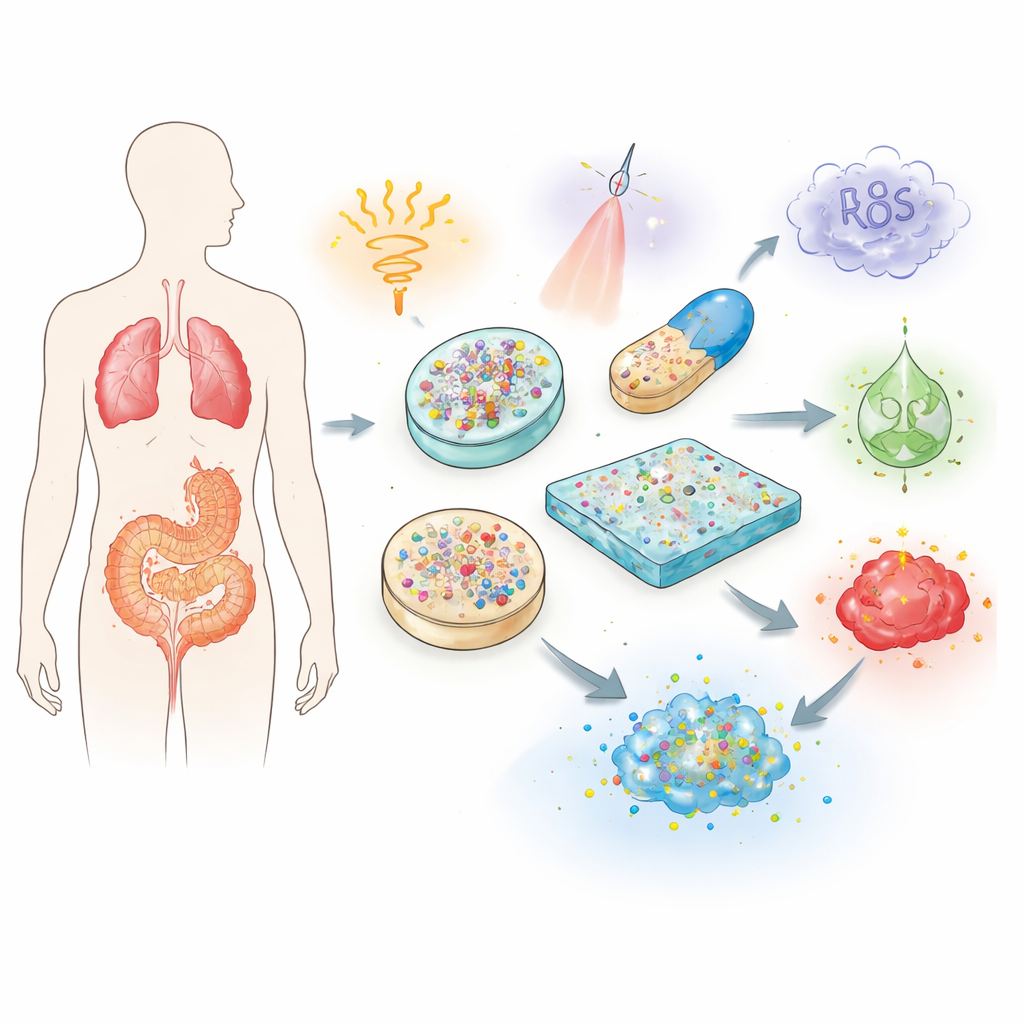
Traditionelle Pillen und Injektionen schicken Medikamente auf eine weitgehend unkontrollierte Reise durch den Körper. Ein Großteil eines Wirkstoffs kann abgebaut, ausgeschieden oder von gesunden Organen aufgenommen werden, lange bevor er ein Tumor, ein entzündetes Gelenk oder ein geschädigtes Herz erreicht. Um das auszugleichen, verschreiben Ärztinnen und Ärzte oft höhere oder wiederholte Dosen, was das Risiko für Nebenwirkungen wie Organschäden oder Immunreaktionen erhöht. Der Review erklärt, wie stimuli-responsive Biomaterialien diese Probleme angehen, indem sie als schützende Transporter fungieren. Aus biokompatiblen Polymeren, Gelen und Nanopartikeln aufgebaut, können sie empfindliche Ladungen schützen, deren Lebensdauer im Körper verlängern und genau steuern, wann und wo das Medikament freigesetzt wird.
Materialien, die auf ihre Umgebung hören
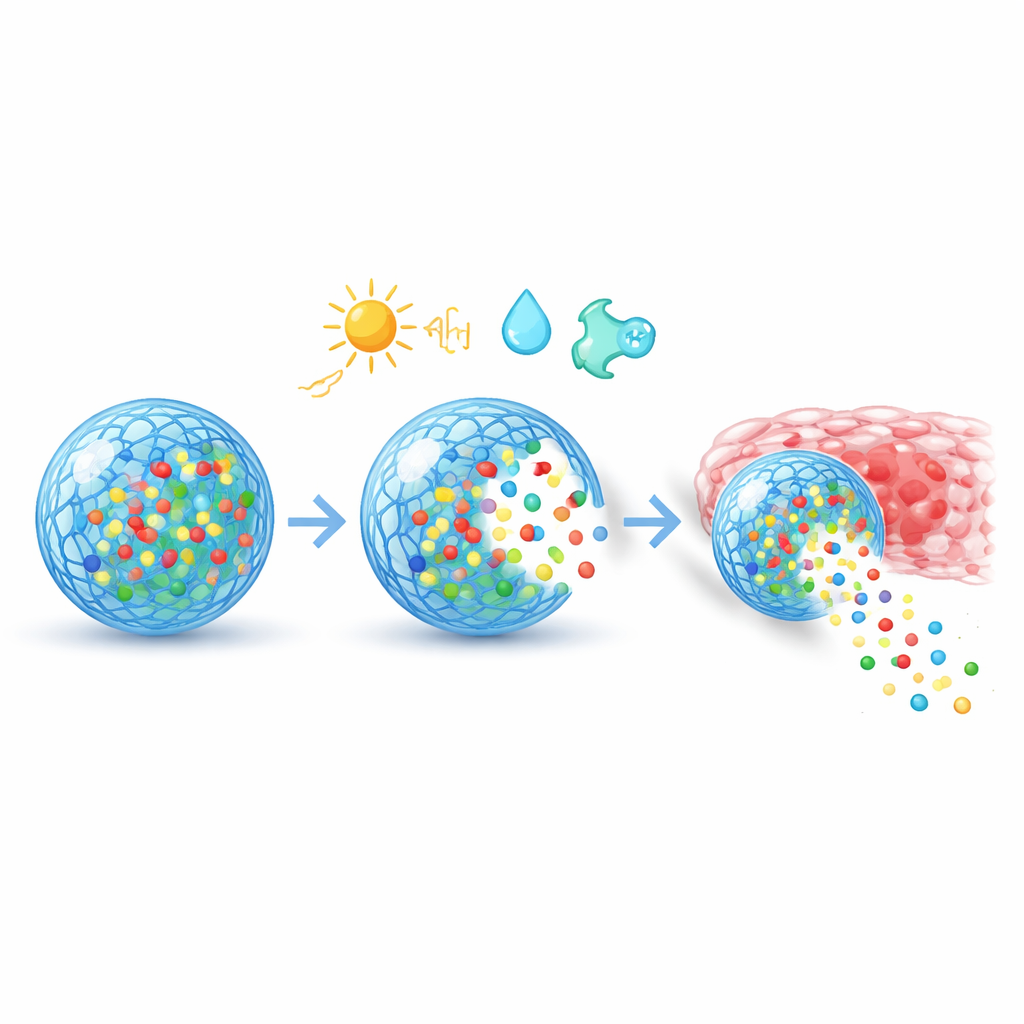
Die Grundidee ist, einem Material die Fähigkeit zu geben, seine Umgebung zu „erkennen“ und sein Verhalten entsprechend zu ändern. Die Autoren beschreiben drei große Familien von Auslösern. Physikalische Signale wie Wärme, Licht, Magnetfelder und Ultraschall können von außen auf den Körper angewandt werden, um die Freisetzung zu ausgewählten Zeitpunkten ein- oder auszuschalten. Chemische Signale wie Säuregrad, Redox-Balance und Salzgehalt unterscheiden sich zwischen gesundem und erkranktem Gewebe, sodass Träger sich nur in beispielsweise saurer Tumorumgebung öffnen. Biologische Signale umfassen Enzyme, Glukose und reaktive Sauerstoffspezies, die in bestimmten Krankheiten erhöht sind; diese können spezielle Bindungen in einem Material kappen, ein Gel erweichen oder die Löslichkeit verändern und so das Medikament nur im Problemgebiet freisetzen. Einige fortgeschrittene Systeme kombinieren sogar mehrere Auslöser, um eine präzisere Kontrolle zu erreichen.
Wie intelligente Träger Behandlung steuern und freisetzen
Über das Erkennen hinaus werden diese Materialien so gestaltet, dass sie sich im Körper navigieren und mit Zellen interagieren. Ihre Oberflächen können mit kurzen Peptiden, Antikörpern oder anderen Bindemitteln versehen werden, die Marker auf Krebszellen, entzündetem Gewebe oder bestimmten Organen erkennen und die Träger zu ihren Zielen leiten. Nach der Aufnahme in Zellen hilft clevere Chemie, aus internen „Mülltonnen“ zu entkommen und genetische Fracht wie mRNA oder CRISPR-Komponenten in das richtige Zellkompartiment zu liefern. Durch Anpassung von Porosität, Ladung und Abbaubarkeit können Entwickler langsame, gleichmäßige Freisetzungen über Wochen, scharfe Impulse ausgelöst durch Licht oder Temperaturänderung oder mehrstufige Muster schaffen, die den Phasen der Heilung folgen. Auf Gewebeebene helfen spezielle Beschichtungen Partikeln, durch Schleim zu gleiten, an Wunden haften zu bleiben oder nicht zu schnell vom Immunsystem entfernt zu werden.
Anwendungen von Insulin bis zu Krebsimpfstoffen
Der Review gibt einen Überblick über eine schnell wachsende Liste praktischer Anwendungen. Für Proteinwirkstoffe und Peptide können wärme- oder lichtreaktive Implantate und Hydrogele bedarfsgerechte Dosierungen ohne häufige Injektionen ermöglichen. pH-sensitive Partikel, die vorübergehend die engen Verbindungen im Darm öffnen, bieten einen Weg, große biologische Wirkstoffe zu schlucken, die normalerweise injiziert werden müssen. Gentherapien profitieren von responsiven Nanopartikeln und Gelen, die empfindliche DNA und RNA schützen und sie dann nur in Zielzellen freisetzen. Kleinmolekulare Medikamente, wie Chemotherapeutika, werden in Träger geladen, die auf in Tumoren vorhandene Enzyme oder oxidativen Stress reagieren und so die Behandlung am Krebsort konzentrieren. In Zell- und Gentherapie verbessern gefertigte Gerüste und schützende Beschichtungen, wie transplantierte Zellen in verletzte Organe finden und dort überleben. Für Impfstoffe und Immuntherapien können pH‑ausgelöste Mikronadelpflaster und 3D‑gedruckte Immunzellgerüste das Auftreten von Antigenen und Immun‑Signalen zeitlich steuern, um einen stärkeren, länger anhaltenden Schutz zu erzielen.
Versprechen, Hürden und der Weg nach vorn
Für Nichtfachleute ist die Quintessenz, dass diese intelligenten Materialien wie programmierbare Lieferwagen für Medikamente wirken, die ihre Ladetüren nur unter den richtigen Bedingungen öffnen. Erste Tierstudien und einige klinische Beispiele zeigen, dass dies die Wirksamkeit steigern und Nebenwirkungen in der Krebsbehandlung, bei Diabetes, Wundheilung und regenerativer Medizin reduzieren kann. Die Autoren betonen jedoch, dass wichtige Fragen zur Langzeitsicherheit, zur Großserienfertigung und zum Verhalten dieser komplexen Materialien in der vielfältigen, sich ständig verändernden Umgebung realer Patientinnen und Patienten offenbleiben. Sie sehen schnellen Fortschritt, wenn maschinelles Lernen, fortschrittlicher 3D‑ und 4D‑Druck sowie winzige eingebettete Sensoren in das Materialdesign einfließen. Werden diese Herausforderungen gemeistert, könnten stimuli-responsive Biomaterialien zur Grundlage zukünftiger Therapien werden, die sich an die Biologie jedes Einzelnen anpassen und Behandlung genau dort und dann liefern, wo und wann sie gebraucht wird.
Zitation: Singh, H., Darban, Z., Ebrahimi, A. et al. Delivering biomedicines with stimuli‑responsive biomaterials. Commun Mater 7, 122 (2026). https://doi.org/10.1038/s43246-026-01163-4
Schlüsselwörter: intelligente Wirkstofffreisetzung, stimuli-responsive Biomaterialien, zielgerichtete Therapie, Nanomedizin, Regenerative Medizin