Clear Sky Science · zh
通过有机化学推进蛋白质工程
重写自然的构件
蛋白质是驱动细胞运作的小型机器,从抵抗感染到传递信息和药物。然而,自然仅用有限的工具箱构建它们:20种标准氨基酸和少数天然修饰。本文解释了现代有机化学如何使科学家突破自然规则:如今可以逐原子地构建、重塑和改良蛋白质,以制造更耐用的药物、更智能的诊断工具,以及用于精准研究疾病的工具。
化学家如何改造天然蛋白质
综述首先描述了天然蛋白质如何被小型化学标签——称为翻译后修饰——高度调控,这些标签可以开启或关闭蛋白活性。受此启发,化学家现在有意改造蛋白侧链、序列,甚至骨架,以微调构象和稳定性。强有力的方法如固相肽合成和具选择性的“点击样”连接术,让研究者能够逐段缝合长蛋白链,然后在选定位置加入精确改动。这些策略将蛋白质变成可编程的定制平台,其行为可以被设计而非仅被观察。
将蛋白质锁定为更坚固、更智能的构象
一个重要主题是使用化学“订书钉”和交联将蛋白质锁定为在严苛环境中更稳定的构象,例如在肿瘤内或工业反应器中。例如,研究者通过在关键螺旋间安装烃类订书钉和芳香交联桥,增强了脆弱的转录因子——那些与DNA结合并控制基因开启的蛋白质。这些稳定的模拟体可以进入细胞、结合与癌症相关的DNA位点,并阻断难以药物化的靶点如Myc致癌基因的作用。类似的交联策略也使酶更耐热且更活跃,并强化了免疫信使白细胞介素-2(IL-2),使其在体内存留更久而不丧失有益作用。
用新序列与镜像设计蛋白质
作者还强调了如何构建全新的蛋白序列以暴露隐藏的结合口袋或逆转常见的反应选择性。自动流动合成允许快速生产具有锁定构象的宏环蛋白,这些构象有利于与特定类药分子结合。化学家可替换非天然氨基酸来探测催化或识别中哪些相互作用最为关键。更进一步,他们构建由D-氨基酸组成的“镜像”蛋白——化学上与自然相反的构件。这些镜像蛋白能抗拒通常会降解药物的天然酶,并可通过镜像显示技术进行进化,成为针对生长因子和炎症信号的高效、低免疫原性的抑制剂。
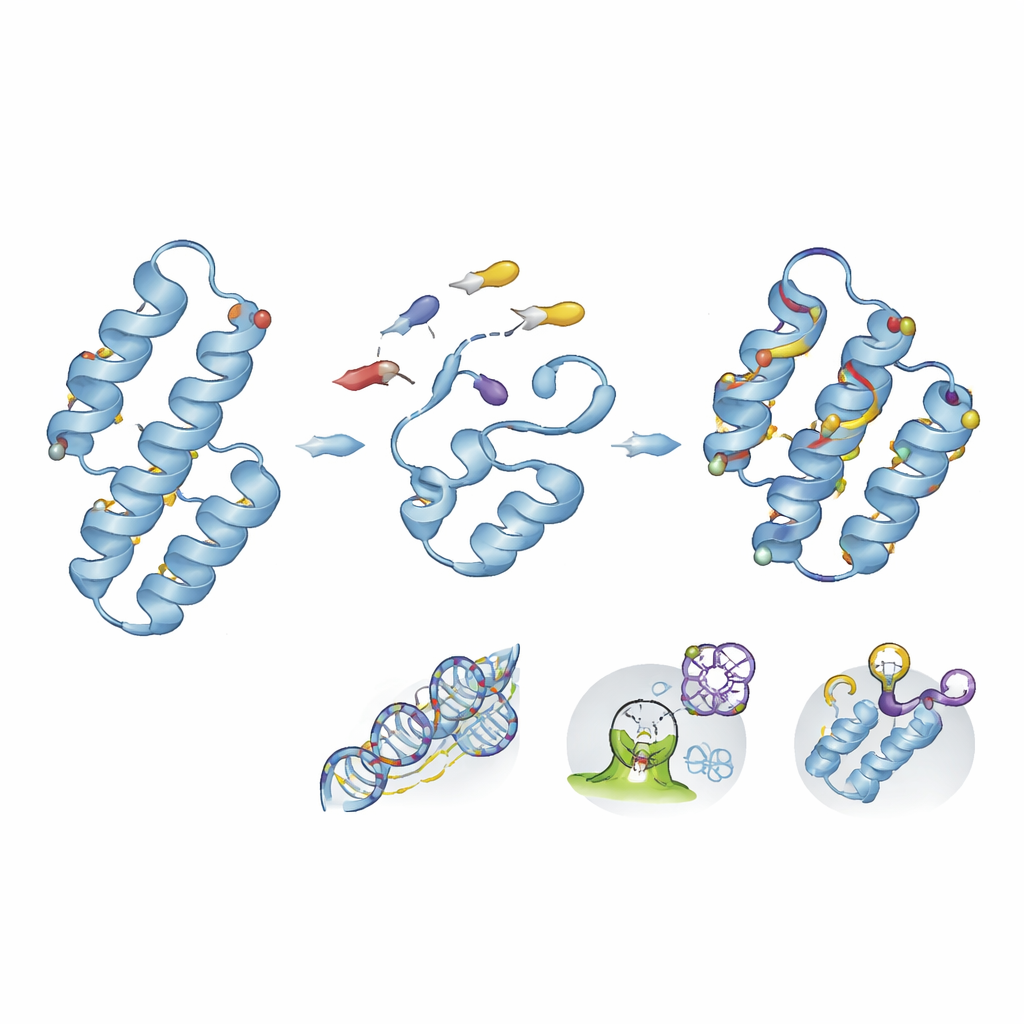
从零开始构建蛋白以捕获药物和毒素
除了改造天然产物之外,从头蛋白质设计使科学家能够创造在生物学中从未存在过的新折叠。借助计算蓝图和高通量筛选,团队已构建小型螺旋束,能将如抗凝药阿哌沙班等有毒药物安置在特化口袋内,从而在动物模型中将其从循环中清除。同样的设计原则可与骨架环化或镜像化学结合,产生高度稳定、持久的结合体。其他定制迷你蛋白已被调控以纳米摩尔亲和力识别与癌症或炎症相关的靶点,同时在血液和组织中能抵抗降解。
从化学把戏到未来药物
结论指出,有机化学、结构生物学与计算的结合正将蛋白质转变为完全可工程化的材料。通过以受控方式改变侧链、序列与骨架,研究者现在能打造比许多天然同类更稳定、更具选择性且更易进入细胞的蛋白质。仍需克服的挑战包括放大复杂合成的规模、扩展可用于连接片段的化学键类型,以及可靠折叠大型高度修饰蛋白。尽管如此,发展方向清晰:化学工程蛋白有望成为一种新型药物与分子工具,能够攻克先前“难以成药”的靶点,并实现更高精度与更少副作用的治疗方案。
引用: Nithun, R.V., Singh, M., Baransi, A. et al. Advancing protein engineering via organic chemistry. Commun Chem 9, 161 (2026). https://doi.org/10.1038/s42004-026-02033-3
关键词: 化学蛋白质工程, 合成蛋白质, 蛋白质治疗, 从头蛋白质设计, 镜像蛋白质