Clear Sky Science · de
Fortschritte in der Proteintechnik durch organische Chemie
Die Bausteine der Natur neu schreiben
Proteine sind die winzigen Maschinen, die unsere Zellen steuern – vom Abwehren von Infektionen bis zum Transport von Signalen und Medikamenten. Die Natur baut sie allerdings nur aus einem begrenzten Werkzeugkasten von 20 standardmäßigen Aminosäuren und einigen wenigen natürlichen Modifikationen. Dieser Artikel erklärt, wie die moderne organische Chemie es Wissenschaftlern erlaubt, über die Regeln der Natur hinauszugehen: Sie können Proteine jetzt atomgenau aufbauen, umformen und verbessern, um robustere Medikamente, intelligentere Diagnostika und präzise Werkzeuge zur Erforschung von Krankheiten zu entwickeln.
Wie Chemiker natürliche Proteine aufrüsten
Der Überblick beginnt mit der Beschreibung, wie natürliche Proteine bereits stark durch kleine chemische Markierungen – sogenannte posttranslationale Modifikationen – reguliert werden, die ihre Aktivität ein- oder ausschalten können. Davon inspiriert verändern Chemiker heute gezielt Seitenketten, Sequenzen und sogar das Rückgrat von Proteinen, um Form und Stabilität fein abzustimmen. Leistungsfähige Methoden wie die Festphasen-Peptidsynthese und chemoselektive „Click-ähnliche“ Ligationen erlauben es Forschern, lange Proteinketten Stück für Stück zusammenzunähen und gezielte Änderungen an definierten Positionen vorzunehmen. Diese Strategien verwandeln Proteine in anpassbare Plattformen, deren Verhalten programmiert statt bloß beobachtet werden kann.
Proteine in robustere, intelligentere Formen verriegeln
Ein zentrales Thema ist der Einsatz chemischer „Klammern“ und Quervernetzungen, um Proteine in Formen zu fixieren, die unter rauen Bedingungen besser funktionieren, etwa in Tumoren oder in industriellen Reaktoren. Beispielsweise verstärkten Forscher fragile Transkriptionsfaktoren – Proteine, die an DNA binden und steuern, welche Gene aktiviert werden – durch Einbau von Kohlenwasserstoff‑Staples und aromatischen Querbrücken zwischen wichtigen Helices. Diese stabilisierten Nachahmer können in Zellen eindringen, an krebsassoziierte DNA‑Stellen binden und die Wirkung schwer zu behandelnder Ziele wie des Onkogens Myc blockieren. Ähnliche Quervernetzungsstrategien haben Enzyme hitzeresistenter und aktiver gemacht sowie den Immunbotenstoff Interleukin‑2 so gestärkt, dass er länger im Körper wirkt, ohne seine nützlichen Effekte zu verlieren.
Proteine mit neuen Sequenzen und Spiegelbildern entwerfen
Die Autorinnen und Autoren heben auch hervor, wie völlig neue Proteinsequenzen entworfen werden können, um verborgene Bindungstaschen freizulegen oder die übliche Selektivität von Reaktionen umzukehren. Automatisierte Fluss‑Synthese ermöglicht die schnelle Herstellung makrocyclischer Proteine mit fixierten Konformationen, die die Bindung an bestimmte, medikamentenähnliche Moleküle begünstigen. Chemiker können nicht‑natürliche Aminosäuren einbauen, um herauszufinden, welche Wechselwirkungen für Katalyse oder Erkennung am wichtigsten sind. Noch einen Schritt weiter gehen Spiegelbildproteine aus D‑Aminosäuren – der chemischen Umkehrung der in der Natur üblichen L‑Aminosäuren. Diese Spiegelproteine sind resistent gegen natürliche Enzyme, die Medikamente normalerweise abbauen, und lassen sich mithilfe von Spiegelbild‑Display‑Technologien zu potenten, nicht immunogenen Blockern von Wachstumsfaktoren und Entzündungssignalen entwickeln.
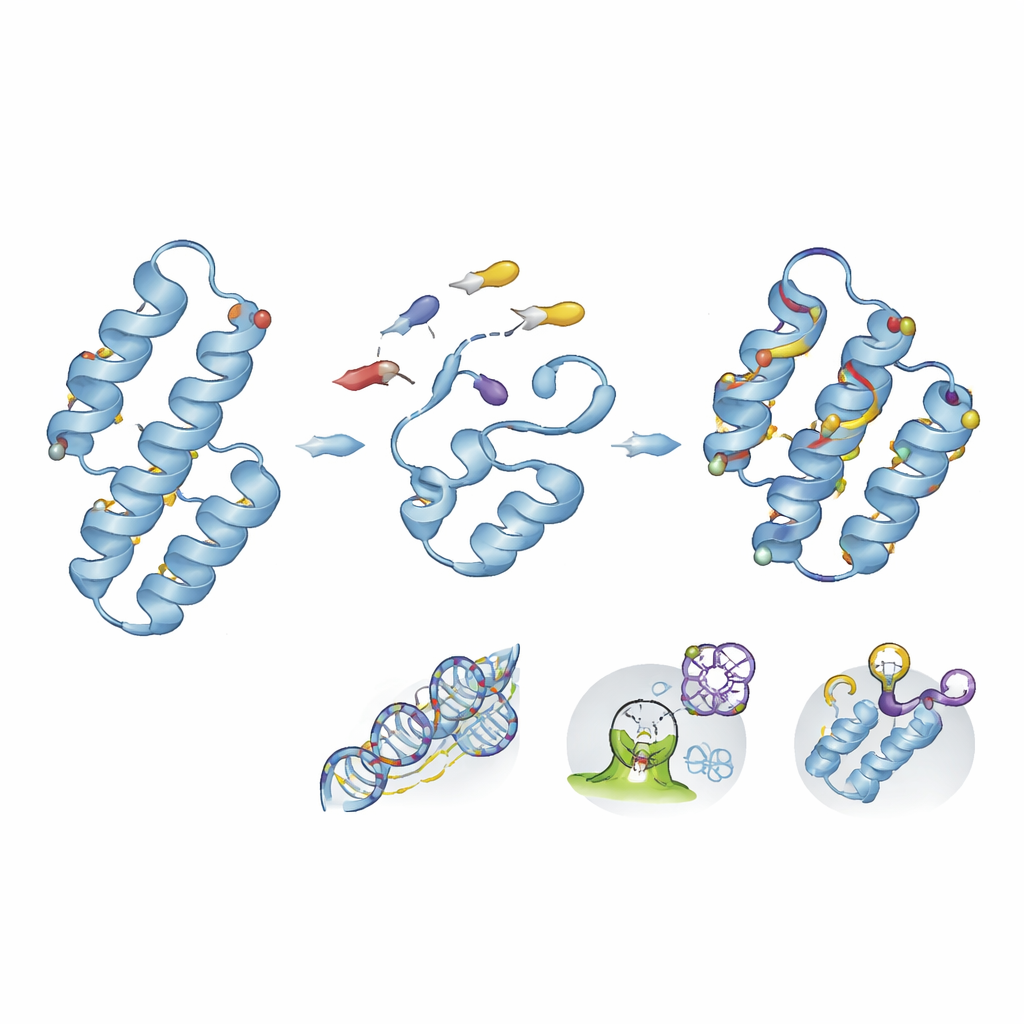
Proteine von Grund auf bauen, um Arzneien und Toxine einzufangen
Über die Modifikation natürlicher Vorlagen hinaus ermöglicht das De‑novo‑Protein‑Design die Schaffung völlig neuer Faltungen, die in der Biologie nie vorkamen. Mithilfe computergestützter Blaupausen und Hochdurchsatz‑Screenings haben Teams kleine helikale Bündel konstruiert, die sich giftige Wirkstoffe wie den Blutverdünner Apixaban in spezialisierten Taschen einverleiben und so aus der Zirkulation in Tiermodellen entfernen können. Dieselben Designprinzipien lassen sich mit Rückgratcyclisierung oder Spiegelbildchemie kombinieren, um hochstabile, langlebige Binder zu erzeugen. Andere maßgeschneiderte Miniproteine wurden so gestaltet, dass sie Krebs‑ oder Entzündungsziele mit Nanomol‑Affinität erkennen und gleichzeitig Abbau in Blut und Gewebe widerstehen.
Von chemischen Tricks zu künftigen Arzneimitteln
Abschließend argumentiert der Artikel, dass die Verbindung von organischer Chemie, Strukturbiologie und Computation Proteine zu vollständig engineerbaren Materialien macht. Durch kontrollierte Veränderungen an Seitenketten, Sequenzen und Rückgraten können Forschende nun Proteine entwerfen, die stabiler, selektiver und zellgängiger sind als viele natürliche Entsprechungen. Verbleibende Herausforderungen sind das Hochskalieren komplexer Synthesen, die Erweiterung der nutzbaren chemischen Verknüpfungstypen zum Zusammenfügen von Fragmenten und das zuverlässige Falten großer, stark modifizierter Proteine. Dennoch ist der Trend klar: chemisch entwickelte Proteine stehen kurz davor, eine neue Klasse von Arzneimitteln und molekularen Werkzeugen zu werden, die zuvor „nicht behandelbare“ Ziele angehen und Therapien mit höherer Präzision und geringeren Nebenwirkungen ermöglichen.
Zitation: Nithun, R.V., Singh, M., Baransi, A. et al. Advancing protein engineering via organic chemistry. Commun Chem 9, 161 (2026). https://doi.org/10.1038/s42004-026-02033-3
Schlüsselwörter: chemische Proteintechnik, synthetische Proteine, Proteintherapeutika, De-novo-Proteindesign, Spiegelbildproteine