Clear Sky Science · pl
Postępy inżynierii białek dzięki chemii organicznej
Przepisywanie budulca natury
Białka to mikroskopijne maszyny napędzające nasze komórki — od walki z infekcjami po przekazywanie sygnałów i przenoszenie leków. Natura jednak buduje je z ograniczonego zestawu 20 standardowych aminokwasów i kilku naturalnych modyfikacji. W tym artykule wyjaśniono, jak współczesna chemia organiczna pozwala naukowcom wyjść poza reguły natury: dziś można budować, przekształcać i ulepszać białka atom po atomie, tworząc trwalsze leki, inteligentniejsze testy diagnostyczne i precyzyjne narzędzia do badania chorób.
Jak chemicy ulepszają naturalne białka
Przegląd zaczyna się od opisu, jak naturalne białka są już silnie regulowane przez małe chemiczne etykiety, zwane modyfikacjami potranslacyjnymi, które mogą włączać lub wyłączać ich aktywność. Zainspirowani tym, chemicy celowo zmieniają łańcuchy boczne, sekwencje, a nawet kręgosłup białka, aby dopracować jego kształt i stabilność. Potężne metody, takie jak synteza peptydów na stałej fazie i chemoselektywne ligacje „podobne do click”, pozwalają badaczom zszywać długie łańcuchy białkowe kawałek po kawałku, a następnie wprowadzać precyzyjne zmiany w wybranych pozycjach. Strategie te przekształcają białka w konfigurowalne platformy, których zachowanie można programować, zamiast tylko obserwować.
Usztywnianie białek w trwalsze, sprytniejsze kształty
Głównym motywem jest wykorzystanie chemicznych „zacisków” i mostków krzyżowych do utrwalania białek w konformacjach działających lepiej w trudnych warunkach, na przykład wewnątrz guzów czy w reaktorach przemysłowych. Na przykład badacze wzmocnili kruche czynniki transkrypcyjne — białka wiążące DNA i kontrolujące, które geny są aktywne — poprzez instalację hydrokarbonowych zszywek i aromatycznych mostków między kluczowymi helisami. Takie ustabilizowane mimetyki mogą przenikać do komórek, przyłączać się do miejsc na DNA związanych z rakiem i blokować działanie trudno farmakologicznie celowanych celów, takich jak onkogen Myc. Podobne strategie krzyżowania zwiększyły odporność enzymów na temperaturę i ich aktywność oraz wzmocniły czynnik immunologiczny interleukinę‑2, dzięki czemu dłużej pozostaje aktywny w organizmie bez utraty korzystnych efektów.
Projektowanie białek z nowymi sekwencjami i lustrzanymi obrazami
Autorzy podkreślają także, jak można tworzyć całkowicie nowe sekwencje białkowe, aby odsłonić ukryte kieszenie wiążące lub odwrócić zwykłą selektywność reakcji. Zautomatyzowana synteza przepływowa umożliwia szybkie wytwarzanie makrocyklicznych białek z utrwalonymi konformacjami sprzyjającymi wiązaniu określonych cząsteczek przypominających leki. Chemicy mogą wprowadzać nienaturalne aminokwasy, aby badać, które interakcje są najważniejsze dla katalizy lub rozpoznawania. Idąc dalej, budują „białka lustrzane” z aminokwasów D — chemicznego przeciwieństwa tych występujących w naturze. Białka lustrzane są odporne na naturalne enzymy, które zwykle rozkładają leki, i mogą być ewoluowane przy użyciu metod wyświetlania obrazu lustrzanego, aby stać się silnymi, nieimmunogennymi blokerami czynników wzrostu i sygnałów zapalnych.
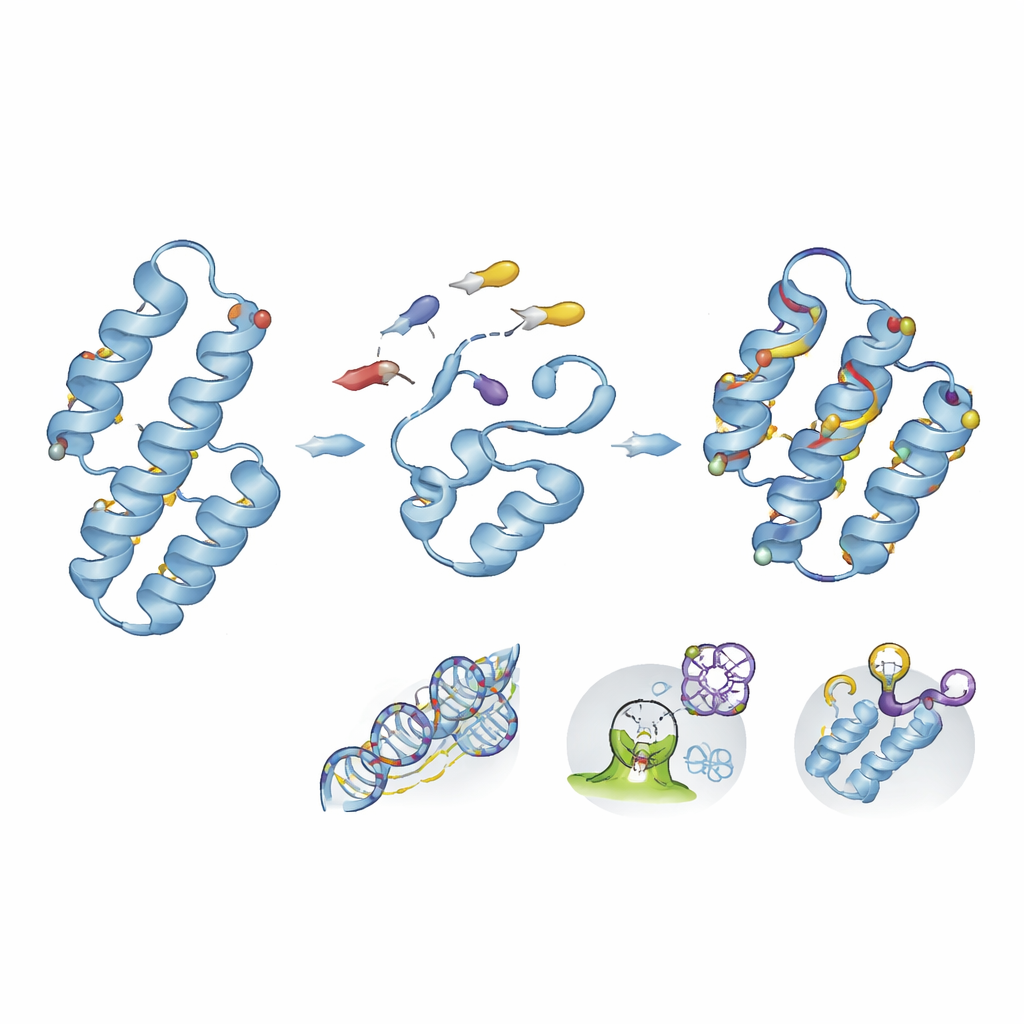
Budowanie białek od podstaw, aby wychwytywać leki i toksyny
Ponad modyfikowaniem tego, co daje natura, projektowanie białek de novo pozwala naukowcom tworzyć zupełnie nowe fałdowania, które nigdy nie występowały w biologii. Korzystając z obliczeniowych planów i przesiewów wysokoprzepustowych, zespoły zbudowały małe pęczki helikalne, które mieszczą toksyczne leki, takie jak antykoagulant apiksaban, w wyspecjalizowanych kieszeniach, usuwając je z krążenia w modelach zwierzęcych. Te same zasady projektowe można łączyć z cyklizacją kręgosłupa lub chemią lustrzaną, aby uzyskać wysoce stabilne, długo działające wiążące białka. Inne spersonalizowane minibiałka zostały zaprojektowane tak, by rozpoznawać cele związane z rakiem lub zapaleniem z powinowactwem w skali nanomoli, jednocześnie opierając się degradacji we krwi i tkankach.
Od chemicznych sztuczek do przyszłych leków
Na zakończenie artykuł stwierdza, że połączenie chemii organicznej, biologii strukturalnej i obliczeń przekształca białka w w pełni inżynieryjne materiały. Poprzez kontrolowane modyfikacje łańcuchów bocznych, sekwencji i kręgosłupa badacze potrafią tworzyć białka bardziej stabilne, bardziej selektywne i lepiej penetrujące komórki niż wiele naturalnych odpowiedników. Wyzwania, które pozostają, obejmują skalowanie złożonych syntez, rozszerzanie rodzajów połączeń chemicznych używanych do łączenia fragmentów oraz niezawodne fałdowanie dużych, silnie zmodyfikowanych białek. Niemniej jednak kierunek jest jasny: chemicznie inżynieryjne białka mają szansę stać się nową klasą leków i narzędzi molekularnych, zdolnych do zaatakowania wcześniej „niedruggowalnych” celów i umożliwienia terapii o większej precyzji i mniejszej liczbie efektów ubocznych.
Cytowanie: Nithun, R.V., Singh, M., Baransi, A. et al. Advancing protein engineering via organic chemistry. Commun Chem 9, 161 (2026). https://doi.org/10.1038/s42004-026-02033-3
Słowa kluczowe: chemiczna inżynieria białek, syntetyczne białka, terapeutyki białkowe, projektowanie białek de novo, białka lustrzane