Clear Sky Science · nl
Vooruitgang in proteïne-engineering via organische chemie
De bouwstenen van de natuur herschrijven
Eiwitten zijn de kleine machientjes die onze cellen laten draaien, van het bestrijden van infecties tot het vervoeren van boodschappen en geneesmiddelen. Toch bouwt de natuur ze alleen uit een beperkt gereedschapssysteem van 20 standaardaminozuren en een paar natuurlijke aanpassingen. Dit artikel legt uit hoe moderne organische chemie wetenschappers in staat stelt de regels van de natuur te overstijgen: zij kunnen nu eiwitten atoom voor atoom bouwen, hervormen en verbeteren om stevigere geneesmiddelen, slimmere diagnostiek en nauwkeurige instrumenten voor ziekteonderzoek te maken.
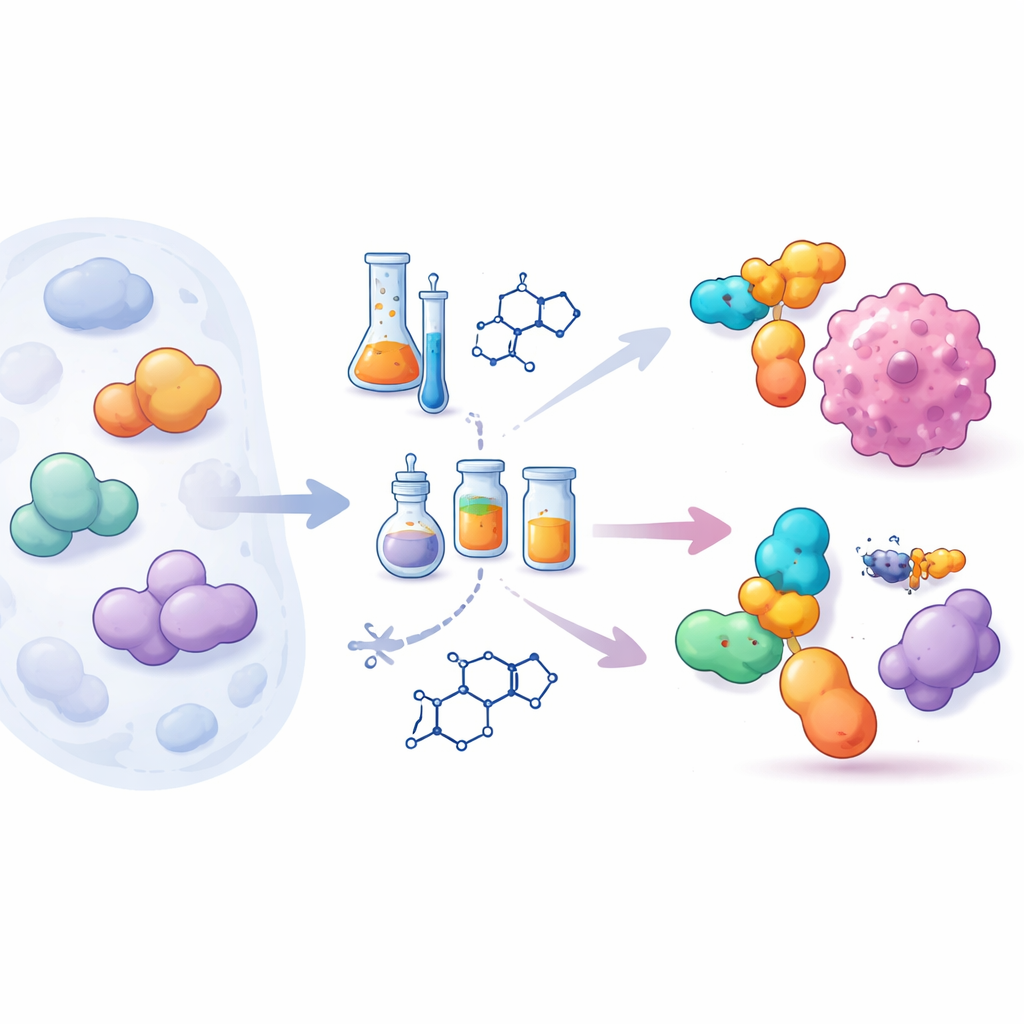
Hoe chemici natuurlijke eiwitten upgraden
De review begint met te beschrijven hoe natuurlijke eiwitten al sterk gereguleerd worden door kleine chemische labels, zogenaamde posttranslationele modificaties, die hun activiteit aan- of uit kunnen schakelen. Geïnspireerd door dit mechanisme veranderen chemici nu bewust zijgroepen, sequenties en zelfs de ruggegraat van eiwitten om vorm en stabiliteit fijn af te stemmen. Krachtige methoden zoals solid-phase peptidesynthese en chemoselectieve, "click-achtige" ligatie stellen onderzoekers in staat lange eiwitketens stukje bij beetje aan elkaar te naaien en vervolgens precieze veranderingen op gekozen posities aan te brengen. Deze strategieën veranderen eiwitten in aanpasbare platforms waarvan het gedrag geprogrammeerd kan worden in plaats van alleen geobserveerd.
Eiwitten vergrendelen in stevigere, slimere vormen
Een hoofdthema is het gebruik van chemische “nietjes” en crosslinks om eiwitten vast te zetten in vormen die beter werken onder zware omstandigheden, zoals in tumoren of industriële reactoren. Zo versterkten onderzoekers kwetsbare transcriptiefactoren—eiwitten die aan DNA binden en bepalen welke genen aan gaan—door hydrocarbonen nietjes en aromatische cross-bridges tussen sleutelhelixen aan te brengen. Deze gestabiliseerde mimics kunnen cellen binnendringen, zich vastklampen aan DNA-locaties die met kanker samenhangen, en de werking van moeilijk geneesbare doelen zoals het Myc-oncogen blokkeren. Vergelijkbare crosslinkingstrategieën maakten enzymen hittebestendiger en actiever en versterkten de immuunboodschapper interleukine-2 zodat deze langer in het lichaam blijft zonder zijn gunstige effecten te verliezen.
Eiwitten ontwerpen met nieuwe sequenties en spiegelbeelden
De auteurs belichten ook hoe volledig nieuwe eiwitsequenties kunnen worden ontworpen om verborgen bindingspockets bloot te leggen of de gebruikelijke selectiviteit van reacties om te keren. Geautomatiseerde flow-synthese maakt snelle productie mogelijk van macrocyclische eiwitten met vergrendelde conformaties die de binding aan specifieke geneesmiddelachtige moleculen bevorderen. Chemici kunnen niet-natuurlijke aminozuren inwisselen om te onderzoeken welke interacties het meest van belang zijn voor katalyse of herkenning. Verdergaand bouwen ze “spiegelbeeldige” eiwitten uit D-aminozuren—de chemische tegenpool van die in de natuur. Deze spiegelproteïnen zijn bestand tegen natuurlijke enzymen die normaal gesproken geneesmiddelen afbreken en kunnen, met behulp van spiegelbeeldige display-technologieën, geëvolueerd worden tot krachtige, niet-immunogene remmers van groeifactoren en ontstekingssignalen.
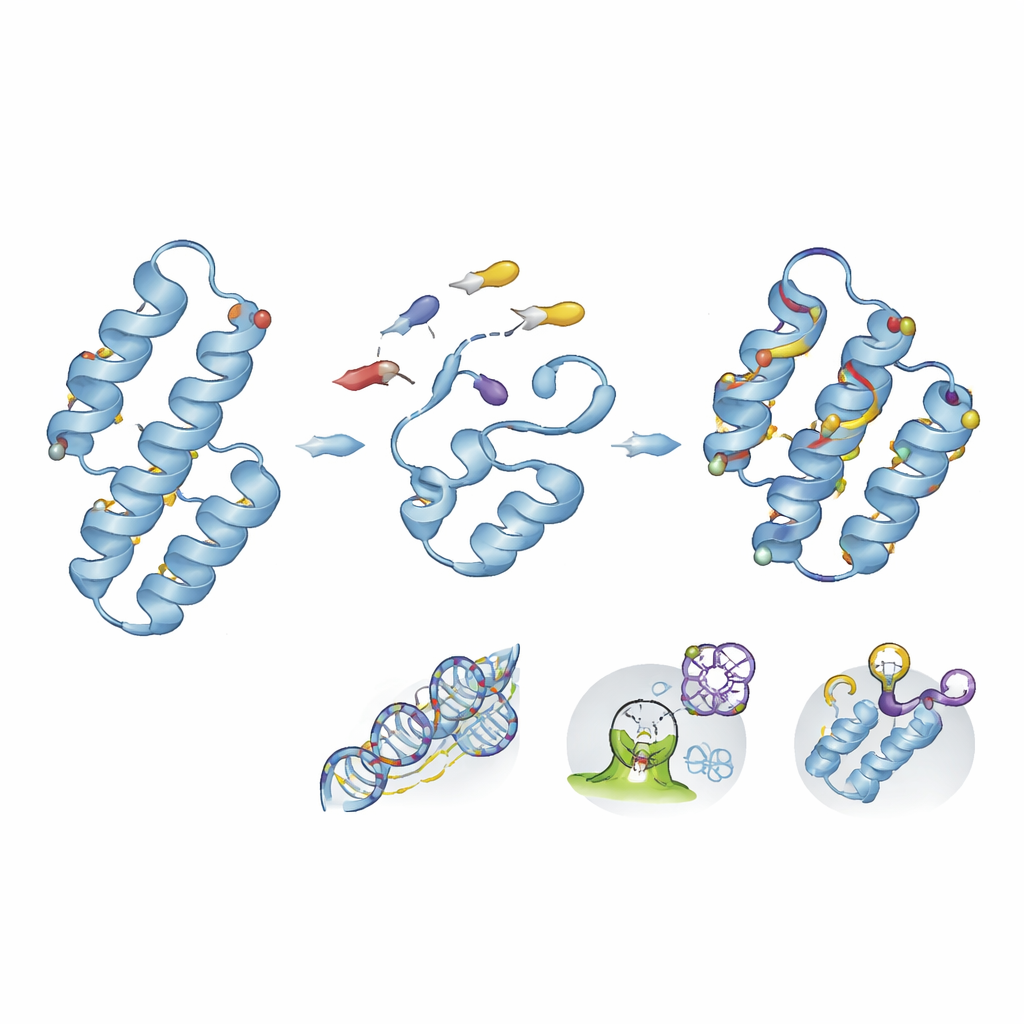
Eiwitten vanaf nul bouwen om geneesmiddelen en toxines op te vangen
Naast het aanpassen van wat de natuur levert, maakt de novo eiwitontwerp het mogelijk geheel nieuwe vouwen te creëren die niet in de biologie voorkwamen. Met computationele blauwdrukken en hoogdoorloopscreening hebben teams kleine helixbundels gebouwd die toxische geneesmiddelen zoals de bloedverdunner apixaban in gespecialiseerde pockets omsluiten en uit de circulatie halen in diermodellen. Dezelfde ontwerpprincipes kunnen worden gecombineerd met ruggegraatcyclisatie of spiegelbeeldige chemie om zeer stabiele, langwerkende binders te verkrijgen. Andere op maat gemaakte miniproteïnen zijn afgestemd om kankergenen of ontstekingsgerelateerde doelen met nanomolaire affiniteit te herkennen, terwijl ze degradatie in bloed en weefsels weerstaan.
Van chemische trucs naar toekomstige geneesmiddelen
Ter afsluiting betoogt het artikel dat het huwelijk van organische chemie, structurele biologie en computation eiwitten verandert in volledig engineerbare materialen. Door zijgroepen, sequenties en ruggraten gecontroleerd te wijzigen, kunnen onderzoekers nu eiwitten ontwerpen die stabieler, selectiever en beter in staat zijn cellen binnen te dringen dan veel natuurlijke tegenhangers. Blijvende uitdagingen zijn het opschalen van complexe syntheses, het uitbreiden van de types chemische verbindingen die gebruikt kunnen worden om fragmenten samen te voegen, en het betrouwbaar laten vouwen van grote, sterk gewijzigde eiwitten. Niettemin is de koers duidelijk: chemisch gemodificeerde eiwitten staan op het punt een nieuwe klasse geneesmiddelen en moleculaire hulpmiddelen te worden, in staat moeilijk te behandelen doelen aan te pakken en therapieën met grotere precisie en minder bijwerkingen mogelijk te maken.
Bronvermelding: Nithun, R.V., Singh, M., Baransi, A. et al. Advancing protein engineering via organic chemistry. Commun Chem 9, 161 (2026). https://doi.org/10.1038/s42004-026-02033-3
Trefwoorden: chemische proteïne-engineering, synthetische eiwitten, proteïnetherapieën, de novo eiwitontwerp, spiegelbeeldige eiwitten