Clear Sky Science · es
Avanzando la ingeniería de proteínas mediante la química orgánica
Reescribiendo los bloques constructores de la naturaleza
Las proteínas son las pequeñas máquinas que hacen funcionar nuestras células, desde combatir infecciones hasta transportar señales y fármacos. Sin embargo, la naturaleza solo las construye a partir de un conjunto limitado de 20 aminoácidos estándar y unas pocas modificaciones naturales. Este artículo explica cómo la química orgánica moderna permite a los científicos ir más allá de las reglas de la naturaleza: ahora pueden construir, remodelar y mejorar proteínas átomo por átomo para crear medicamentos más resistentes, diagnósticos más inteligentes y herramientas de precisión para estudiar la enfermedad.
Cómo los químicos mejoran las proteínas naturales
La revisión comienza describiendo cómo las proteínas naturales ya están fuertemente reguladas por pequeñas etiquetas químicas, llamadas modificaciones posraduccionales, que pueden activar o desactivar su actividad. Inspirados por ello, los químicos ahora alteran deliberadamente las cadenas laterales, las secuencias e incluso la columna vertebral de las proteínas para ajustar su forma y estabilidad. Métodos poderosos como la síntesis de péptidos en fase sólida y las ligaciones quimioselectivas tipo “click” permiten a los investigadores ensamblar largas cadenas proteicas pieza por pieza y después añadir cambios precisos en posiciones elegidas. Estas estrategias convierten a las proteínas en plataformas personalizables cuyo comportamiento puede programarse en lugar de limitarse a observarse.
Bloquear proteínas en conformaciones más resistentes e inteligentes
Un tema central es el uso de “grapas” químicas y entrecruzamientos para fijar las proteínas en conformaciones que funcionan mejor en condiciones adversas, como dentro de tumores o reactores industriales. Por ejemplo, los investigadores reforzaron factores de transcripción frágiles —proteínas que se unen al ADN y controlan qué genes se activan— instalando grapas hidrocarbonadas y puentes aromáticos entre hélices clave. Estos análogos estabilizados pueden penetrar en las células, unirse a sitios de ADN vinculados al cáncer y bloquear la acción de dianas difíciles de abordar, como el oncogén Myc. Estrategias de entrecruzamiento similares han hecho que enzimas sean más resistentes al calor y más activas, y han reforzado el mensajero inmunitario interleucina-2 para que dure más tiempo en el organismo sin perder sus efectos beneficiosos.
Diseñar proteínas con nuevas secuencias e imágenes en espejo
Los autores también resaltan cómo se pueden crear secuencias de proteínas totalmente nuevas para exponer bolsillos de unión ocultos o invertir la selectividad habitual de reacciones. La síntesis automatizada en flujo permite la producción rápida de proteínas macrocíclicas con conformaciones bloqueadas que favorecen la unión a moléculas con carácter farmacológico específico. Los químicos pueden introducir aminoácidos no naturales para sondear qué interacciones son las más importantes para la catálisis o el reconocimiento. Y yendo más allá, construyen proteínas en “imagen especular” compuestas por aminoácidos D —el opuesto químico de los presentes en la naturaleza. Estas proteínas espejo resisten las enzimas naturales que normalmente degradan fármacos y pueden evolucionarse, mediante tecnologías de display en imagen especular, hasta convertirse en bloqueadores potentes y no inmunogénicos de factores de crecimiento y señales inflamatorias.
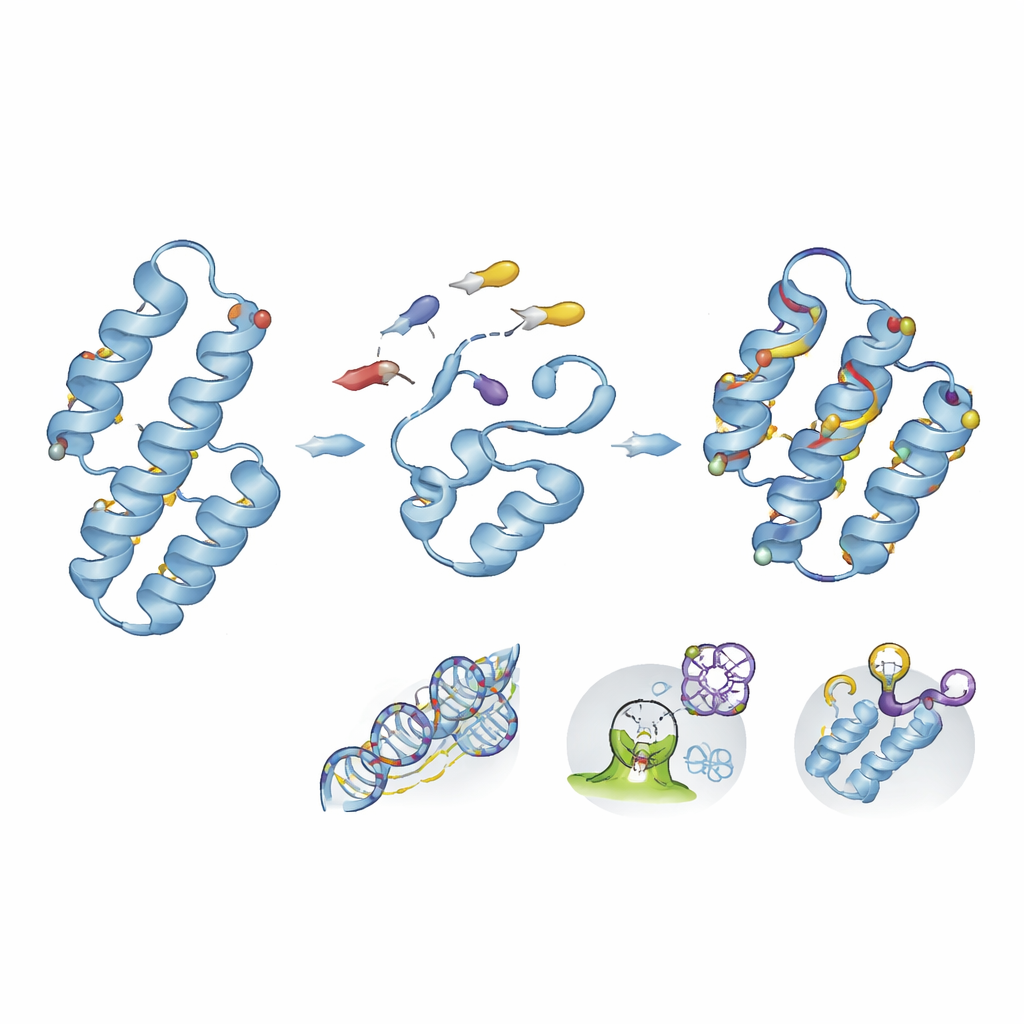
Construir proteínas desde cero para capturar fármacos y toxinas
Más allá de modificar lo que proporciona la naturaleza, el diseño de novo de proteínas permite a los científicos crear nuevos pliegues que nunca existieron en la biología. Utilizando planos computacionales y cribado de alto rendimiento, los equipos han construido pequeños haces helical que alojan fármacos tóxicos como el anticoagulante apixabán dentro de bolsillos especializados, extrayéndolos de la circulación en modelos animales. Los mismos principios de diseño pueden combinarse con ciclización de la columna vertebral o química de imagen especular para generar ligandos altamente estables y de larga duración. Otras miniproteínas a medida se han diseñado para reconocer dianas relacionadas con el cáncer o la inflamación con afinidades en el rango nanomolar mientras resisten la degradación en sangre y tejidos.
De los trucos químicos a los medicamentos del futuro
Para concluir, el artículo sostiene que el matrimonio entre la química orgánica, la biología estructural y la computación está convirtiendo a las proteínas en materiales completamente diseñables. Al alterar cadenas laterales, secuencias y columnas vertebrales de forma controlada, los investigadores pueden ahora crear proteínas más estables, más selectivas y con mejor capacidad para entrar en células que muchas de sus contrapartes naturales. Los retos pendientes incluyen escalabilizar síntesis complejas, ampliar los tipos de uniones químicas que se pueden usar para unir fragmentos y plegar de forma fiable proteínas grandes y fuertemente modificadas. No obstante, la trayectoria es clara: las proteínas diseñadas químicamente están preparadas para convertirse en una nueva clase de medicamentos y herramientas moleculares, capaces de abordar dianas previamente “indrugables” y posibilitar terapias con mayor precisión y menos efectos secundarios.
Cita: Nithun, R.V., Singh, M., Baransi, A. et al. Advancing protein engineering via organic chemistry. Commun Chem 9, 161 (2026). https://doi.org/10.1038/s42004-026-02033-3
Palabras clave: ingeniería química de proteínas, proteínas sintéticas, terapéuticas proteicas, diseño de proteínas de novo, proteínas en imagen especular