Clear Sky Science · fr
Faire progresser l’ingénierie des protéines grâce à la chimie organique
Réécrire les éléments constitutifs de la nature
Les protéines sont les petites machines qui font fonctionner nos cellules, de la lutte contre les infections au transport de messages et de médicaments. Pourtant, la nature ne les assemble qu’à partir d’une boîte à outils limitée de 20 acides aminés standards et de quelques modifications naturelles. Cet article explique comment la chimie organique moderne permet aux scientifiques de dépasser les règles de la nature : ils peuvent désormais construire, remodeler et améliorer les protéines atome par atome pour créer des médicaments plus résistants, des diagnostics plus intelligents et des outils précis pour étudier les maladies.
Comment les chimistes améliorent les protéines naturelles
La revue commence par décrire comment les protéines naturelles sont déjà finement régulées par de petites étiquettes chimiques, appelées modifications post-traductionnelles, qui peuvent activer ou désactiver leur activité. S’inspirant de cela, les chimistes modifient désormais délibérément les chaînes latérales, les séquences et même l’épine dorsale des protéines pour ajuster leur forme et leur stabilité. Des méthodes puissantes, telles que la synthèse peptidique en phase solide et les ligations chimiquement sélectives de type “click”, permettent aux chercheurs d’assembler des longues chaînes protéiques morceau par morceau, puis d’ajouter des changements précis à des positions choisies. Ces stratégies transforment les protéines en plates-formes personnalisables dont le comportement peut être programmé plutôt que simplement observé.
Verrouiller les protéines dans des conformations plus robustes et plus intelligentes
Un thème majeur est l’utilisation d’« agrafes » chimiques et de réticulations pour verrouiller les protéines dans des conformations qui fonctionnent mieux dans des conditions difficiles, comme à l’intérieur des tumeurs ou dans des réacteurs industriels. Par exemple, des chercheurs ont renforcé des facteurs de transcription fragiles — des protéines qui se lient à l’ADN et contrôlent l’activation des gènes — en installant des agrafes hydrocarbonées et des ponts aromatiques entre des hélices clés. Ces mimétiques stabilisés peuvent pénétrer dans les cellules, s’accrocher à des sites d’ADN liés au cancer et bloquer l’action de cibles difficiles à traiter, comme l’oncogène Myc. Des stratégies de réticulation similaires ont rendu les enzymes plus résistantes à la chaleur et plus actives, et ont renforcé le messager immunitaire interleukine-2 pour qu’il dure plus longtemps dans l’organisme sans perdre ses effets bénéfiques.
Concevoir des protéines avec de nouvelles séquences et des images-miroir
Les auteurs soulignent également comment des séquences protéiques entièrement nouvelles peuvent être conçues pour exposer des poches de liaison cachées ou inverser la sélectivité habituelle des réactions. La synthèse automatisée en flux permet la production rapide de protéines macrocycliques aux conformations verrouillées qui favorisent la liaison à des molécules de type médicament spécifiques. Les chimistes peuvent introduire des acides aminés non naturels pour sonder quelles interactions sont les plus importantes pour la catalyse ou la reconnaissance. Aller plus loin, ils construisent des protéines « image-miroir » composées d’acides D — l’opposé chimique de ceux de la nature. Ces protéines-miroir résistent aux enzymes naturelles qui dégradent habituellement les médicaments et peuvent être évoluées, grâce à des technologies d’affichage image-miroir, en bloqueurs puissants et non immunogènes de facteurs de croissance et de signaux inflammatoires.
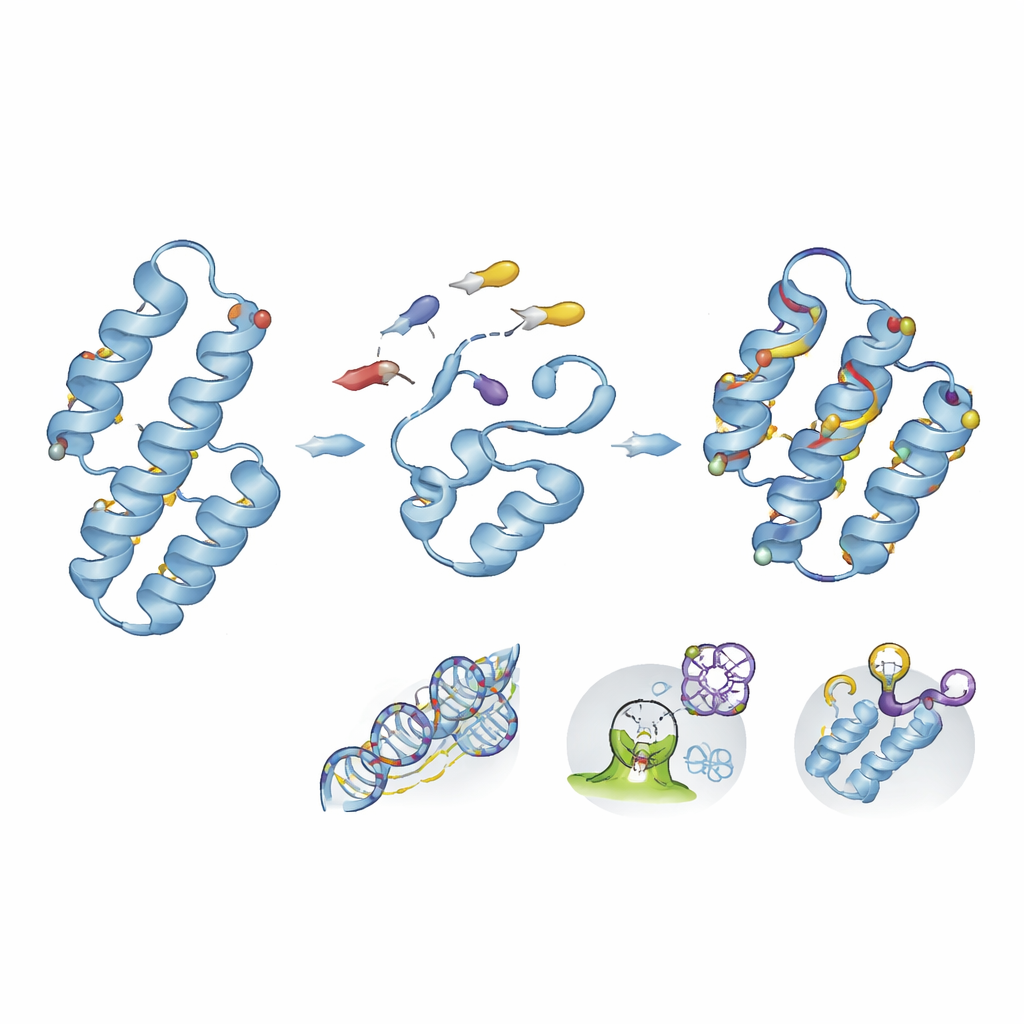
Construire des protéines à partir de zéro pour capter médicaments et toxines
Au-delà de la modification de ce que fournit la nature, la conception de novo de protéines permet de créer de nouveaux repliements qui n’existaient pas en biologie. À l’aide de plans computationnels et de criblages à haut débit, des équipes ont construit de petits paquets hélicoïdaux qui logent des médicaments toxiques tels que l’anticoagulant apixaban dans des poches spécialisées, les retirant ainsi de la circulation chez des modèles animaux. Les mêmes principes de conception peuvent être combinés avec la cyclisation de l’épine dorsale ou la chimie image-miroir pour obtenir des liaisons très stables et durables. D’autres miniprotéines sur mesure ont été adaptées pour reconnaître des cibles liées au cancer ou à l’inflammation avec une affinité nanomolaire tout en résistant à la dégradation dans le sang et les tissus.
Des astuces chimiques aux médicaments de demain
En conclusion, l’article soutient que le mariage de la chimie organique, de la biologie structurale et de la computation transforme les protéines en matériaux pleinement ingénierables. En modifiant de manière contrôlée les chaînes latérales, les séquences et les épines dorsales, les chercheurs peuvent désormais concevoir des protéines plus stables, plus sélectives et mieux capables de pénétrer dans les cellules que beaucoup de leurs homologues naturels. Les défis restants incluent la montée en échelle des synthèses complexes, l’élargissement des types de jonctions chimiques utilisables pour assembler des fragments, et le pliage fiable de grandes protéines fortement modifiées. Néanmoins, la trajectoire est claire : les protéines conçues chimiquement sont prêtes à devenir une nouvelle classe de médicaments et d’outils moléculaires, capables d’attaquer des cibles jusqu’ici « non médicamentables » et de permettre des thérapies plus précises avec moins d’effets secondaires.
Citation: Nithun, R.V., Singh, M., Baransi, A. et al. Advancing protein engineering via organic chemistry. Commun Chem 9, 161 (2026). https://doi.org/10.1038/s42004-026-02033-3
Mots-clés: ingénierie chimique des protéines, protéines synthétiques, thérapeutiques protéiques, conception de novo de protéines, protéines image-miroir