Clear Sky Science · zh
在单细胞分辨率下描绘细胞类型特异性的正向遗传相互作用用于肺腺癌
为什么细胞之间的微小差异很重要
临床医生知道,即便是“相同”类型的肺癌,两个患者对治疗的反应也可能截然不同。部分原因在于肿瘤并非单一的实体,而是由多种细胞类型构成的拼贴——处于不同状态的癌细胞、可能抵抗或助长肿瘤的免疫细胞等。该研究提出了一个简单但有力的问题:我们能否通过读取单个细胞内基因如何协同工作的模式,来判断哪些肿瘤更具危险性、哪些患者更可能从免疫治疗中受益?
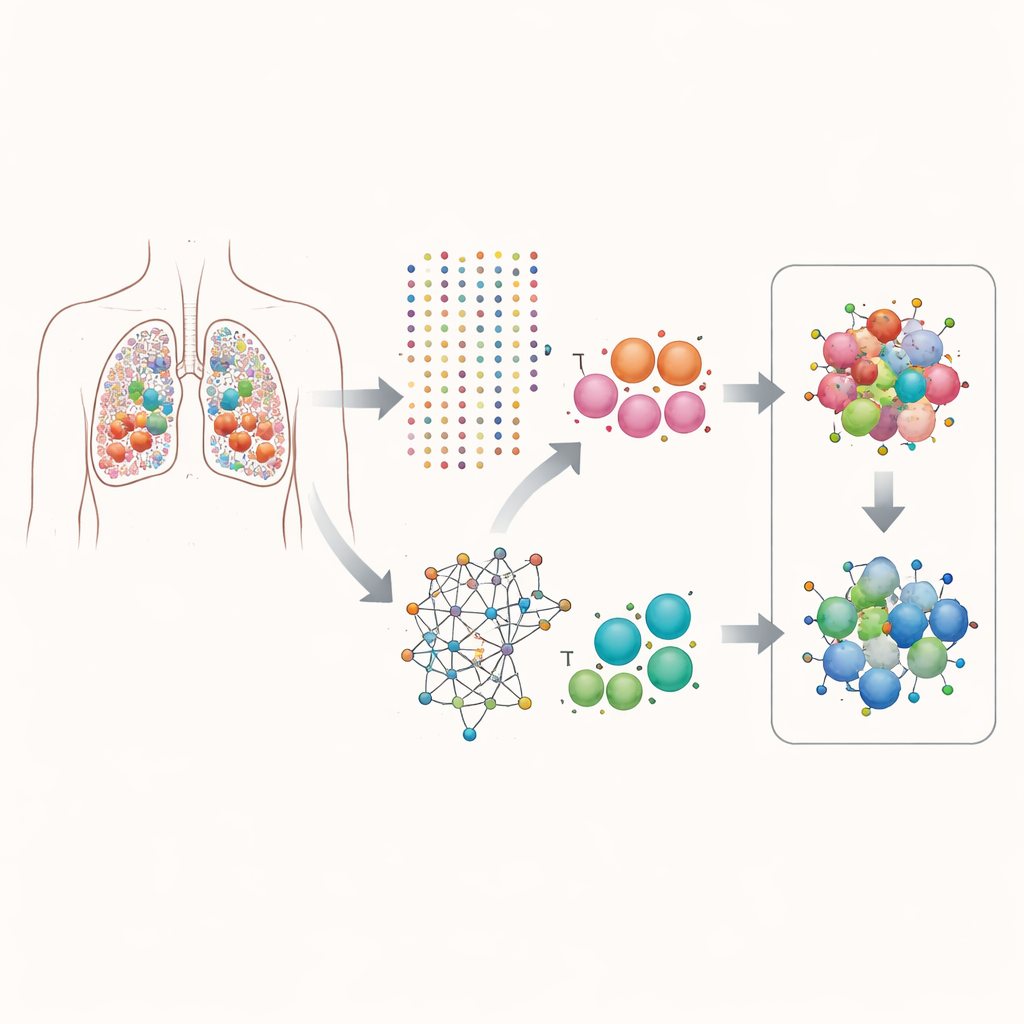
逐细胞窥视肿瘤内部
研究者将注意力集中在肺腺癌——一种常见的肺癌类型。通过单细胞RNA测序,他们测量了来自患者肿瘤的超过16万个单细胞中哪些基因被激活。他们没有只看肿瘤整体的平均基因活性,而是按细胞类型分离数据,特别关注上皮细胞(即发生癌变的细胞)和T细胞(可攻击肿瘤的免疫细胞)。这种逐细胞视角允许他们探究哪些基因倾向于在同一细胞中共同被激活,以及这些基因对如何影响细胞分裂速率的配对关系。
发现有益的基因伙伴关系
团队构建了一个称为scPGI-finder的计算流程,用于在单细胞分辨率下寻找“正向遗传相互作用”。通俗地说,他们寻找那些常在同一细胞中共同激活且其联合活性与较高细胞适应性(以细胞分裂与生长的特征为衡量)相关的基因对。经过多重筛选步骤——检查每对基因共同活跃的频率、相关细胞是否更具增殖性、基因是否强烈共表达以及是否共享相似的生物学功能——他们绘制了两张大型的基因–基因伙伴关系图谱:上皮细胞约5万对,T细胞约1.6万对。这些相互作用网络在已知的蛋白质和通路图谱中高度连通,表明它们更可能反映真实的协作程序,而非随机巧合。
从癌细胞的连接模式读出恶性程度
在上皮细胞的相互作用中,作者强调了一组在恶性癌细胞中比邻近的非恶性上皮细胞更强烈共激活的基因对。他们将这些基因对合并为一个评分,反映在给定细胞或组织样本中有多少这样的“恶性上皮”基因对被共同激活。得分较高的癌细胞表现得更像干细胞、分化程度更低,并且与不受控制生长等典型癌症特征更相关。当将该评分应用于多个患者队列的整体肿瘤样本时,肿瘤的得分始终高于邻近正常肺组织,并能以极高的准确度区分肿瘤和正常组织。肿瘤得分高的患者通常预后较差,且某些高评分细胞系对多种针对驱动生长信号的药物更敏感,尤其是针对EGFR通路的药物。
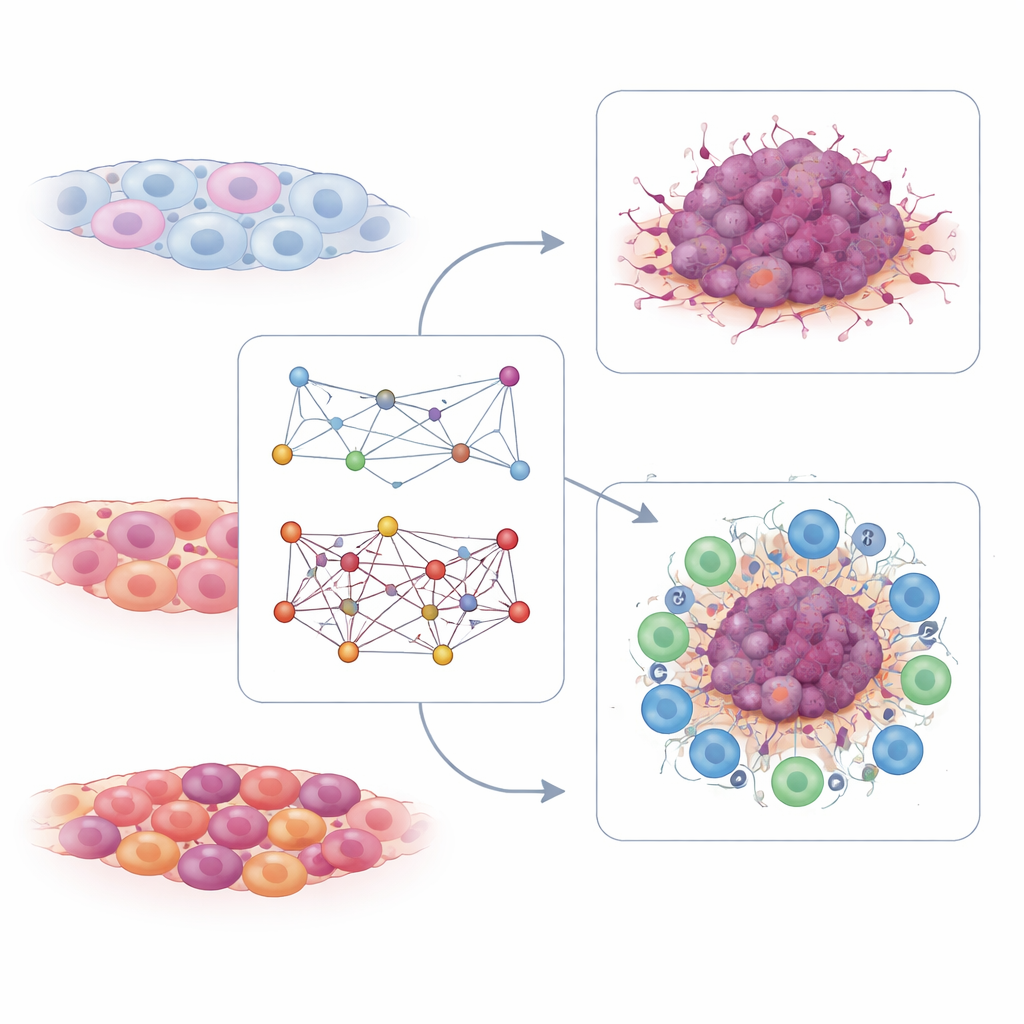
从T细胞中读出免疫强度
T细胞相互作用图谱讲述了一个互补的故事。在这里,研究者寻找那些在T细胞中共同活性与免疫检查点疗法应答好坏相关的基因对——免疫检查点疗法是一种释放T细胞攻击癌症的免疫治疗。他们发现了数百对与应答或耐药相关的基因对。从中提炼出一个由仅六对与T细胞受体信号相关的交互对组成的小型特征。在多个独立患者数据集中,T细胞相互作用评分较高的人更可能对基于PD-1的免疫治疗有反应,并且与更长的生存期相关。高T细胞评分的肿瘤往往具有“热”免疫环境,富含活跃的免疫细胞,而低评分则标志着更可能不从这些药物获益的“冷”肿瘤。
这对未来癌症护理意味着什么
这项工作表明,不仅关注哪些基因被激活,还关注特定细胞类型内基因对的共同激活方式,能够揭示肿瘤内部的隐藏结构。在肺腺癌中,癌细胞中协作基因活动的模式有助于标记更具侵袭性的疾病,而T细胞中的类似模式有助于预测谁会从免疫治疗中受益。尽管这些相互作用图谱基于相关性而非直接的功能性实验,但它们提供了一种从单细胞数据读取肿瘤内部连线的新方法,并且随着该方法被改进并推广到其他癌种,可能为更精确的诊断、预后和治疗选择提供指导。
引用: Chen, B., Liu, M., Dong, Q. et al. Charting cell-type-specific positive genetic interaction at single-cell resolution for lung adenocarcinoma. npj Precis. Onc. 10, 137 (2026). https://doi.org/10.1038/s41698-026-01328-x
关键词: 肺腺癌, 单细胞基因组学, 遗传相互作用, 肿瘤微环境, 免疫治疗反应