Clear Sky Science · es
Cartografiar interacciones genéticas positivas específicas por tipo celular a resolución de célula única para adenocarcinoma de pulmón
Por qué importan las pequeñas diferencias entre células
Los médicos saben que dos personas con el “mismo” cáncer de pulmón pueden responder de forma muy distinta al tratamiento. Una razón es que un tumor no es un bulto uniforme, sino un mosaico de muchos tipos celulares: células cancerosas en distintos estados, células inmunitarias que pueden combatir o favorecer el tumor, y más. Este estudio plantea una pregunta simple pero potente: ¿podemos leer los patrones de cómo los genes actúan juntos dentro de células individuales para saber qué tumores son más peligrosos y qué pacientes tienen más probabilidades de beneficiarse de la inmunoterapia?
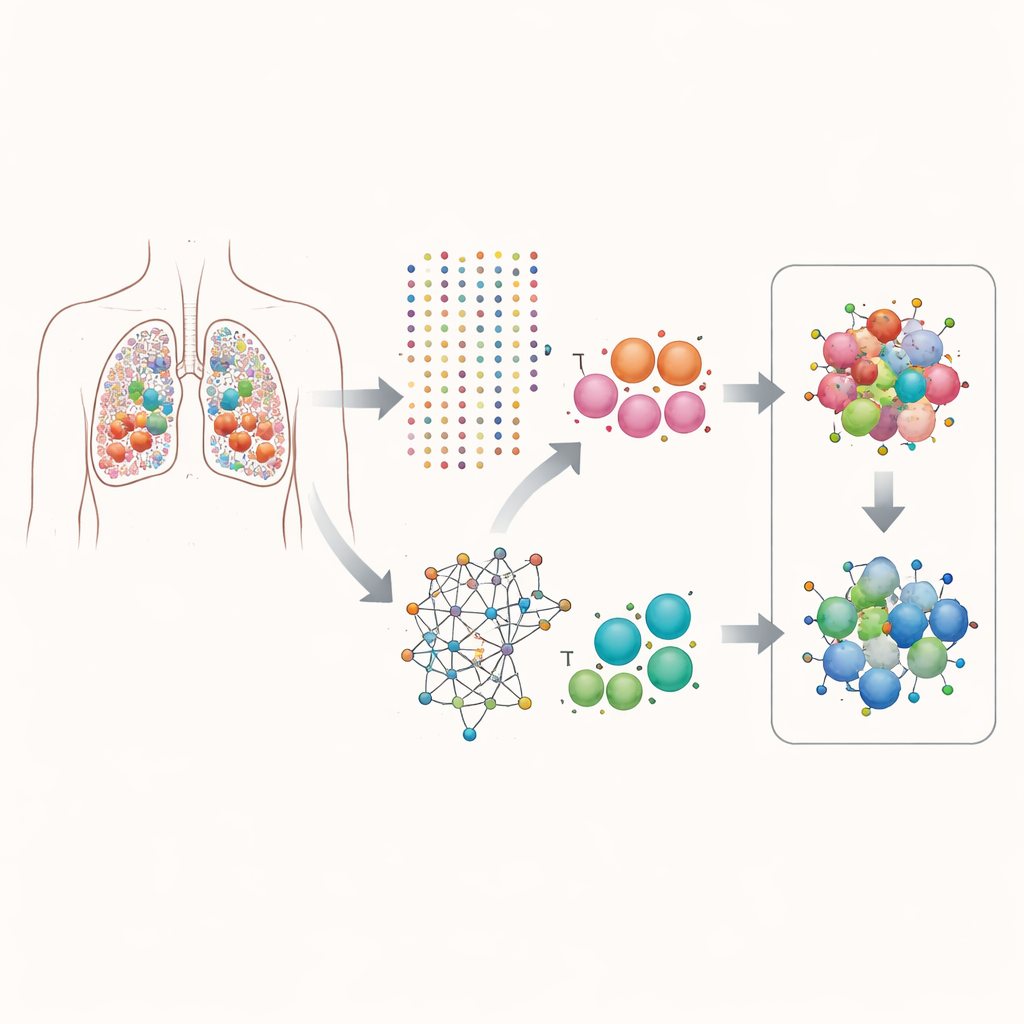
Mirando dentro de los tumores una célula a la vez
Los investigadores se centraron en el adenocarcinoma de pulmón, una forma común de cáncer de pulmón. Usando secuenciación de ARN a célula única, midieron qué genes estaban activados en más de 160.000 células individuales procedentes de tumores de pacientes. En lugar de examinar la actividad génica promedio en todo el tumor, separaron los datos por tipo celular, prestando especial atención a las células epiteliales (las que se vuelven cancerosas) y a las células T (células inmunitarias que pueden atacar los tumores). Esta visión célula por célula les permitió preguntar qué genes tienden a activarse juntos dentro de la misma célula y cómo esas parejas se relacionan con la velocidad aparente de división de las células.
Encontrar asociaciones génicas útiles
El equipo construyó una tubería computacional que denominaron scPGI-finder para buscar “interacciones genéticas positivas” a resolución de célula única. En términos sencillos, buscaron pares de genes que a menudo están activos simultáneamente en la misma célula y cuya actividad conjunta se asocia con mayor aptitud celular, medida por firmas de división y crecimiento celular. Tras varios pasos de filtrado —comprobando con qué frecuencia cada par está coactivo, si esas células parecen más proliferativas, si los genes están fuertemente coexpresados y si comparten roles biológicos similares—, ensamblaron dos amplios mapas de asociaciones gen–gen: unos 50.000 pares en células epiteliales y 16.000 en células T. Estas redes de interacción estaban estrechamente conectadas en mapas de proteínas y vías conocidas, lo que sugiere que capturan programas cooperativos reales en lugar de coincidencias aleatorias.
Leer la malignidad a partir del cableado de las células cancerosas
Entre las interacciones epiteliales, los autores destacaron un subconjunto que mostraba coactividad mucho más intensa en células cancerosas malignas que en células epiteliales no malignas cercanas. Los combinaron en una puntuación que refleja cuántos de esos pares génicos “epiteliales malignos” están activos conjuntamente en una célula o muestra de tejido dada. Las células cancerosas con puntuaciones más altas parecían más similares a células madre, menos diferenciadas y más asociadas con rasgos clásicos del cáncer, como el crecimiento descontrolado. Al aplicar esta puntuación a muestras tumorales masivas de varias cohortes de pacientes, la puntuación fue consistentemente más alta en tumores que en pulmón normal adyacente y separó tumor de tejido normal con muy alta precisión. Los pacientes cuyos tumores tenían puntuaciones altas tendieron a tener peor supervivencia, y ciertas líneas celulares con puntuaciones altas fueron más sensibles a varios fármacos que apuntan a señales que impulsan el crecimiento, en particular fármacos dirigidos a la vía EGFR.
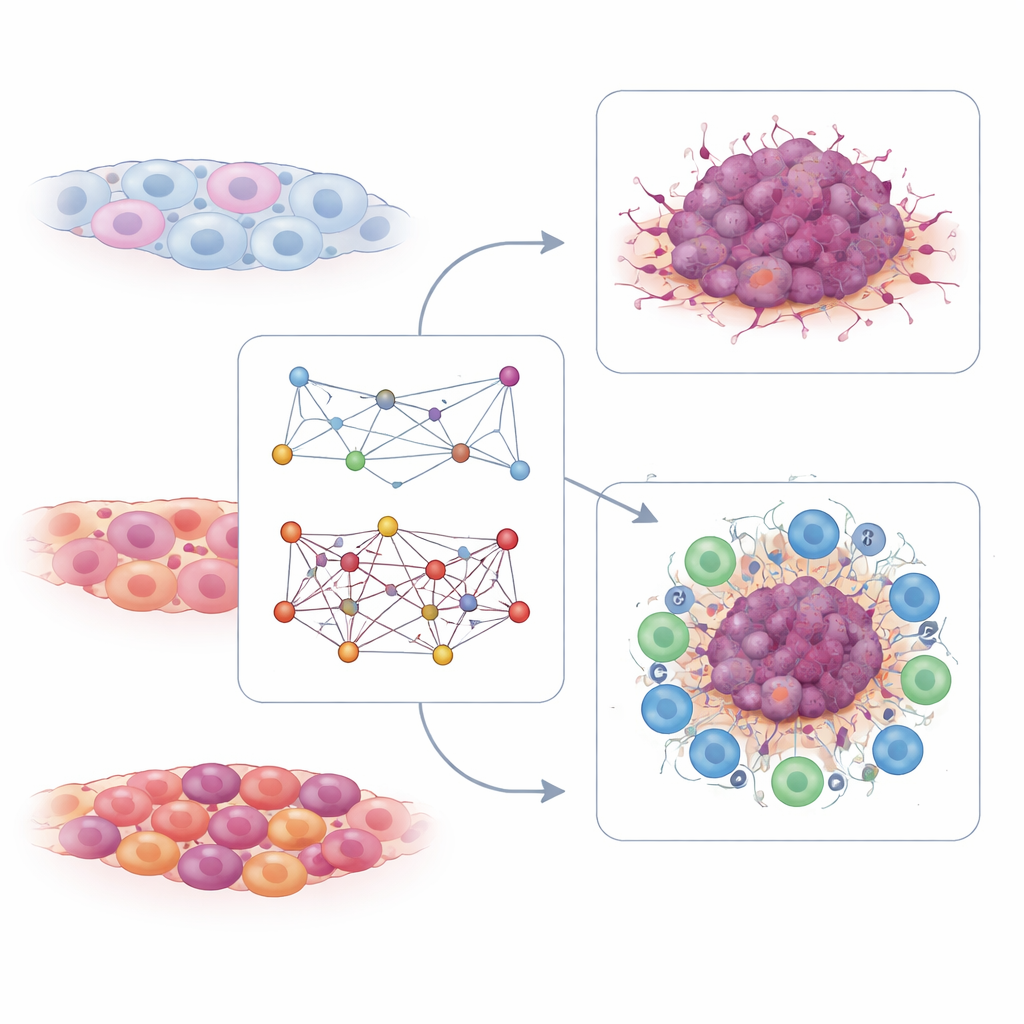
Leer la fuerza inmunitaria a partir de las células T
El mapa de interacciones de las células T contó una historia complementaria. Aquí, los investigadores buscaron pares de genes cuya actividad conjunta en células T se relacionara con buenas o malas respuestas a la terapia con inhibidores de puntos de control inmunitario, una forma de inmunoterapia que libera a las células T contra el cáncer. Encontraron cientos de pares conectados tanto con la respuesta como con la resistencia. A partir de estos, destilaron una pequeña firma formada por solo seis pares de interacción ligados a la señalización del receptor de células T. En múltiples conjuntos de datos independientes de pacientes, valores más altos de esta puntuación de interacción de células T se observaron en personas que respondieron a la inmunoterapia basada en PD-1 y se asociaron con supervivencia más prolongada. Los tumores con puntuaciones altas en células T tendían a tener un entorno inmunitario “caliente”, rico en células inmunitarias activas, mientras que las puntuaciones bajas marcaban tumores “fríos” con menos probabilidades de beneficiarse de estos medicamentos.
Qué significa esto para la atención oncológica futura
Este trabajo muestra que mirar no solo qué genes están activados, sino cómo pares de genes se coactivan dentro de tipos celulares específicos, puede revelar una estructura oculta en los tumores. En el adenocarcinoma de pulmón, los patrones de actividad génica cooperativa en las células cancerosas ayudan a señalar enfermedad más agresiva, mientras que patrones similares en las células T ayudan a predecir quién se beneficiará de la inmunoterapia. Aunque estos mapas de interacción se basan en correlaciones más que en experimentos directos, ofrecen una nueva forma de leer el cableado interno de un tumor a partir de datos de célula única y podrían guiar diagnósticos, pronósticos y opciones de tratamiento más precisos a medida que el enfoque se refine y se extienda a otros cánceres.
Cita: Chen, B., Liu, M., Dong, Q. et al. Charting cell-type-specific positive genetic interaction at single-cell resolution for lung adenocarcinoma. npj Precis. Onc. 10, 137 (2026). https://doi.org/10.1038/s41698-026-01328-x
Palabras clave: adenocarcinoma de pulmón, genómica de célula única, interacciones genéticas, microambiente tumoral, respuesta a inmunoterapia