Clear Sky Science · pl
Mapowanie komórkowo-swoistych dodatnich interakcji genetycznych w rozdzielczości pojedynczej komórki dla gruczolakoraka płuca
Dlaczego drobne różnice między komórkami mają znaczenie
Lekarze wiedzą, że dwie osoby z „tym samym” rakiem płuca mogą reagować na leczenie w bardzo różny sposób. Jednym z powodów jest to, że guz nie jest jednorodną masą, lecz mozaiką różnych typów komórek — komórek nowotworowych w różnych stanach, komórek odpornościowych, które mogą zwalczać lub wspierać guz, i innych. W tym badaniu postawiono proste, ale silne pytanie: czy możemy odczytać wzorce współdziałania genów wewnątrz pojedynczych komórek, by powiedzieć, które guzy są bardziej niebezpieczne i które osoby mają większą szansę skorzystać z immunoterapii?
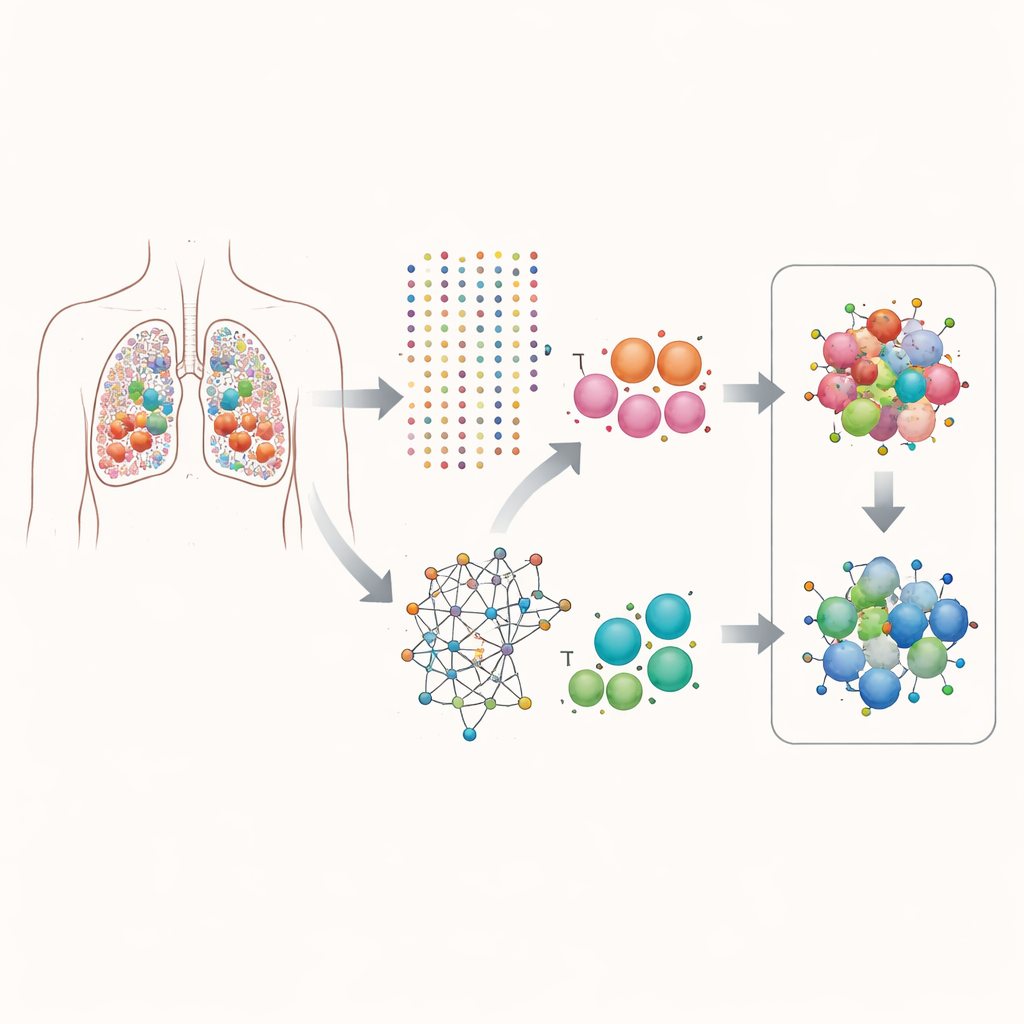
Wgląd w guzy — komórka po komórce
Naukowcy skupili się na gruczolakoraku płuca, częstej postaci raka płuca. Przy użyciu sekwencjonowania RNA pojedynczych komórek zmierzyli, które geny są aktywne w ponad 160 000 pojedynczych komórek pobranych z guzów pacjentów. Zamiast analizować średnią aktywność genów w całym guzie, rozdzielili dane według typu komórek, ze szczególnym uwzględnieniem komórek nabłonkowych (tych, które ulegają zezłośliwieniu) oraz limfocytów T (komórek odpornościowych zdolnych atakować guz). Ten komórka-po-komórce ogląd pozwolił im zapytać, które geny mają tendencję do równoczesnej aktywacji w tej samej komórce i jak takie parowania wiążą się z tempem podziałów komórkowych.
Odnajdywanie korzystnych par genów
Zespół zbudował obliczeniowy pipeline nazwany scPGI-finder, aby wyszukiwać „dodatnie interakcje genetyczne” w rozdzielczości pojedynczej komórki. Mówiąc prościej, szukali par genów często jednocześnie aktywnych w tej samej komórce, których wspólna aktywność łączyła się z wyższą kondycją komórki, mierzoną sygnaturami podziału i wzrostu. Po kilku etapach filtrowania — sprawdzeniu, jak często dana para jest współaktywna, czy te komórki wyglądają na bardziej proliferujące, czy geny są silnie współekspresyjne i czy pełnią podobne role biologiczne — zbudowali dwa obszerne mapy partnerskich par gen–gen: około 50 000 par w komórkach nabłonkowych i 16 000 w limfocytach T. Sieci tych interakcji były mocno powiązane z znanymi mapami białek i szlaków, co sugeruje, że odzwierciedlają rzeczywiste programy kooperacyjne, a nie przypadkowe zbiegi okoliczności.
Odczytywanie złośliwości z połączeń komórek nowotworowych
Wśród interakcji nabłonkowych autorzy wyróżnili podzbiór par, które były znacznie silniej współaktywne w komórkach złośliwych niż w pobliskich nie-złośliwych komórkach nabłonkowych. Połączyli je w miarę odzwierciedlającą, ile z tych „złośliwych nabłonkowych” par genów jest jednocześnie aktywnych w danej komórce lub próbce tkanki. Komórki nowotworowe z wyższymi wartościami tego wskaźnika wykazywały cechy bardziej zbliżone do komórek macierzystych, były mniej zróżnicowane i silniej powiązane z klasycznymi znakami nowotworowymi, takimi jak niekontrolowany wzrost. Zastosowany do „bulkowych” próbek guzów z licznych kohort pacjentów, wskaźnik ten był konsekwentnie wyższy w guzach niż w przyległej zdrowej tkance płucnej i z dużą dokładnością rozróżniał tkankę nowotworową od normalnej. Pacjenci, których guzy miały wysokie wartości tego wskaźnika, mieli zwykle gorsze przeżycia, a niektóre linie komórkowe o wysokich wynikach były bardziej wrażliwe na kilka leków celujących sygnały napędzające wzrost, szczególnie leki ukierunkowane na szlak EGFR.
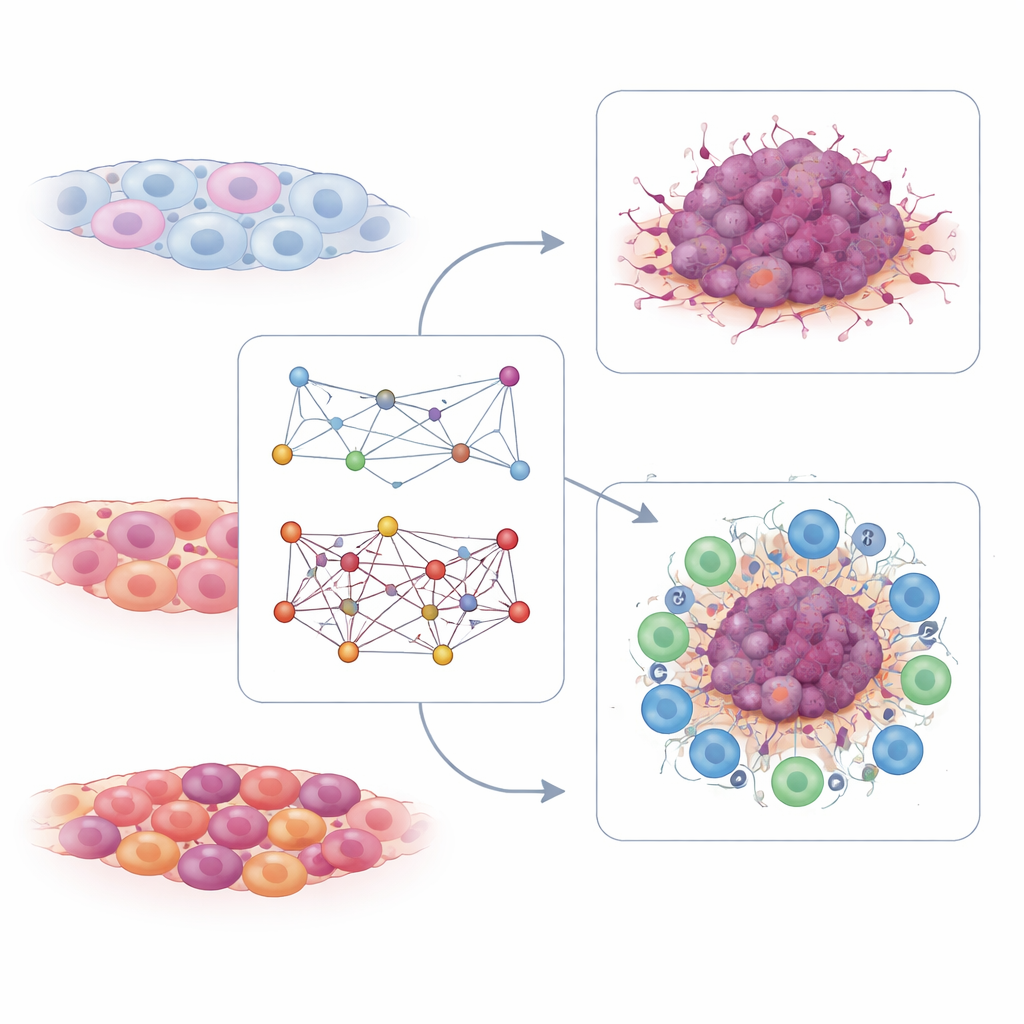
Odczytywanie siły odpornościowej z limfocytów T
Mapa interakcji w limfocytach T ujawniła komplementarną historię. Tutaj badacze szukali par genów, których wspólna aktywność w komórkach T wiązała się z dobrą lub słabą odpowiedzią na terapię blokadą punktów kontrolnych immunologicznych — typ immunoterapii uwalniający limfocyty T przeciwko rakowi. Znaleźli setki par powiązanych albo z wrażliwością, albo z opornością. Z tych par wyodrębnili niewielki sygnaturowy zestaw złożony z zaledwie sześciu par interakcji związanych z sygnalizacją receptora komórkowego T. W wielu niezależnych zbiorach danych pacjentów wyższe wartości tego wskaźnika dla komórek T występowały u osób odpowiadających na immunoterapię opartą na blokadzie PD-1 i wiązały się z dłuższym przeżyciem. Guzy o wysokich wartościach wskaźnika T komórek miały tendencję do „gorącego” środowiska immunologicznego, bogatego w aktywne komórki odpornościowe, podczas gdy niskie wartości charakteryzowały „zimne” guzy, mniej prawdopodobne do skorzystania z tych leków.
Co to oznacza dla przyszłej opieki onkologicznej
Praca ta pokazuje, że analizowanie nie tylko tego, które geny są załączone, lecz także tego, jak pary genów są współaktywowane w specyficznych typach komórek, może ujawnić ukrytą strukturę guzów. W gruczolakoraku płuca wzorce kooperatywnej aktywności genów w komórkach nowotworowych pomagają wskazać bardziej agresywne choroby, natomiast podobne wzorce w limfocytach T pomagają przewidzieć, kto skorzysta z immunoterapii. Choć mapy tych interakcji opierają się na korelacjach, a nie na bezpośrednich eksperymentach przyczynowych, oferują nowy sposób czytania wewnętrznego okablowania guza z danych pojedynczych komórek i mogą kierować precyzyjniejszą diagnostyką, prognozą i doborem terapii w miarę udoskonalania podejścia i jego rozszerzania na inne nowotwory.
Cytowanie: Chen, B., Liu, M., Dong, Q. et al. Charting cell-type-specific positive genetic interaction at single-cell resolution for lung adenocarcinoma. npj Precis. Onc. 10, 137 (2026). https://doi.org/10.1038/s41698-026-01328-x
Słowa kluczowe: gruczolakorak płuca, genomika pojedynczych komórek, interakcje genetyczne, mikrośrodowisko guza, odpowiedź na immunoterapię