Clear Sky Science · de
Kartierung zelltypspezifischer positiver genetischer Interaktionen in Einzelzellauflösung für Lungenadenokarzinom
Warum winzige Unterschiede zwischen Zellen wichtig sind
Ärztinnen und Ärzte wissen, dass zwei Menschen mit „dem gleichen“ Lungenkrebs sehr unterschiedlich auf eine Behandlung reagieren können. Ein Grund ist, dass ein Tumor kein einheitlicher Klumpen ist, sondern ein Flickenteppich vieler Zelltypen – Krebszellen in unterschiedlichen Zuständen, Immunzellen, die dem Tumor schaden oder ihm helfen können, und mehr. Diese Studie stellt eine einfache, aber wirkungsvolle Frage: Können wir aus Mustern der Zusammenarbeit von Genen innerhalb einzelner Zellen ablesen, welche Tumoren gefährlicher sind und welche Patientinnen und Patienten wahrscheinlicher von einer Immuntherapie profitieren?
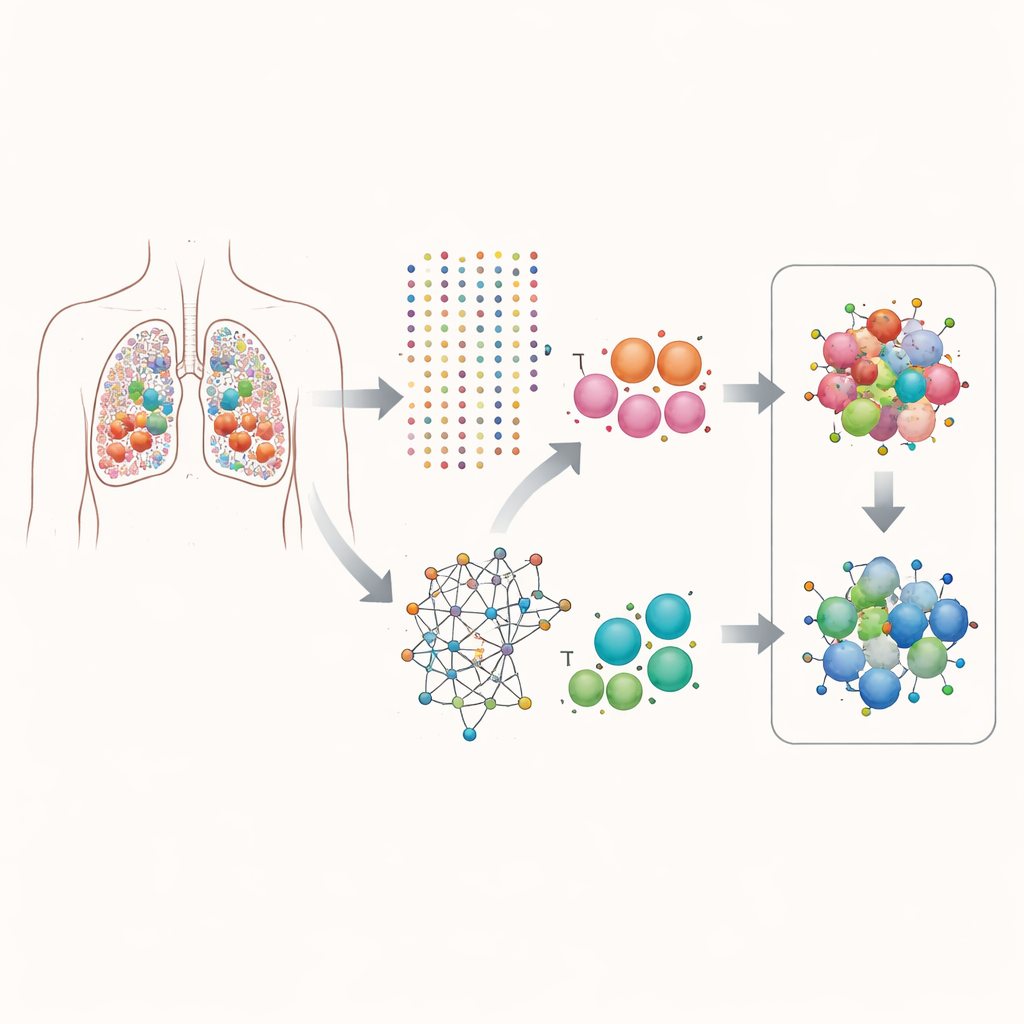
Tumoren Zelle für Zelle betrachten
Die Forschenden konzentrierten sich auf Lungenadenokarzinom, eine häufige Form von Lungenkrebs. Mit Einzelzell-RNA-Sequenzierung maßen sie, welche Gene in über 160.000 einzelnen Zellen aus Patiententumoren aktiviert waren. Statt die durchschnittliche Genaktivität über den gesamten Tumor zu betrachten, teilten sie die Daten nach Zelltyp auf und richteten besonderes Augenmerk auf Epithelzellen (die Zellen, die krebsartig werden) und T‑Zellen (Immunzellen, die Tumore angreifen können). Diese Zelle‑für‑Zelle‑Sicht erlaubte ihnen zu fragen, welche Gene innerhalb derselben Zelle häufig gemeinsam eingeschaltet sind und wie diese Paare mit der Teilungsaktivität der Zellen zusammenhängen.
Hilfreiche Genpartnerschaften finden
Das Team entwickelte eine Rechenpipeline, die sie scPGI‑finder nennen, um nach „positiven genetischen Interaktionen“ in Einzelzellauflösung zu suchen. Einfach ausgedrückt suchten sie nach Genpaaren, die oft gemeinsam in derselben Zelle aktiv sind und deren gemeinsame Aktivität mit höherer Zellfitness verknüpft ist, gemessen an Signaturen von Zellteilung und Wachstum. Nach mehreren Filterstufen – Überprüfung, wie häufig Paare koaktiv sind, ob diese Zellen proliferativer erscheinen, ob die Gene stark koexprimiert sind und ob sie ähnliche biologische Rollen teilen – stellten sie zwei große Karten von Gen‑Gen‑Partnerschaften zusammen: etwa 50.000 Paare in Epithelzellen und 16.000 in T‑Zellen. Diese Interaktionsnetzwerke waren eng verknüpft mit bekannten Protein‑ und Signalwegkarten, was darauf hindeutet, dass sie echte kooperative Programme und keine zufälligen Zusammenhänge erfassen.
Malignität aus der Verschaltung von Krebszellen ablesen
Unter den epithelialen Interaktionen hoben die Autorinnen und Autoren eine Untergruppe hervor, die in malignen Krebszellen deutlich stärker koaktiv war als in benachbarten nicht malignen Epithelzellen. Sie kombinierten diese zu einem Score, der widerspiegelt, wie viele dieser „malignen epithelialen“ Genpaare in einer gegebenen Zelle oder Probe gemeinsam aktiv sind. Krebszellen mit höheren Scores wirkten stammzellähnlicher, weniger differenziert und stärker mit klassischen Krebsmerkmalen wie unkontrolliertem Wachstum assoziiert. Auf Bulk‑Tumorproben aus vielen Patienten‑Kohorten angewandt, war dieser Score konsistent in Tumoren höher als im angrenzenden normalen Lungengewebe und trennte Tumor von Normalgewebe mit sehr hoher Genauigkeit. Patientinnen und Patienten mit hohen Scores hatten tendenziell eine schlechtere Überlebensprognose, und bestimmte hoch bewertete Zelllinien waren empfindlicher gegenüber mehreren Wirkstoffen, die wachstumsfördernde Signale hemmen, insbesondere gegenüber Medikamenten, die auf den EGFR‑Signalweg abzielen.
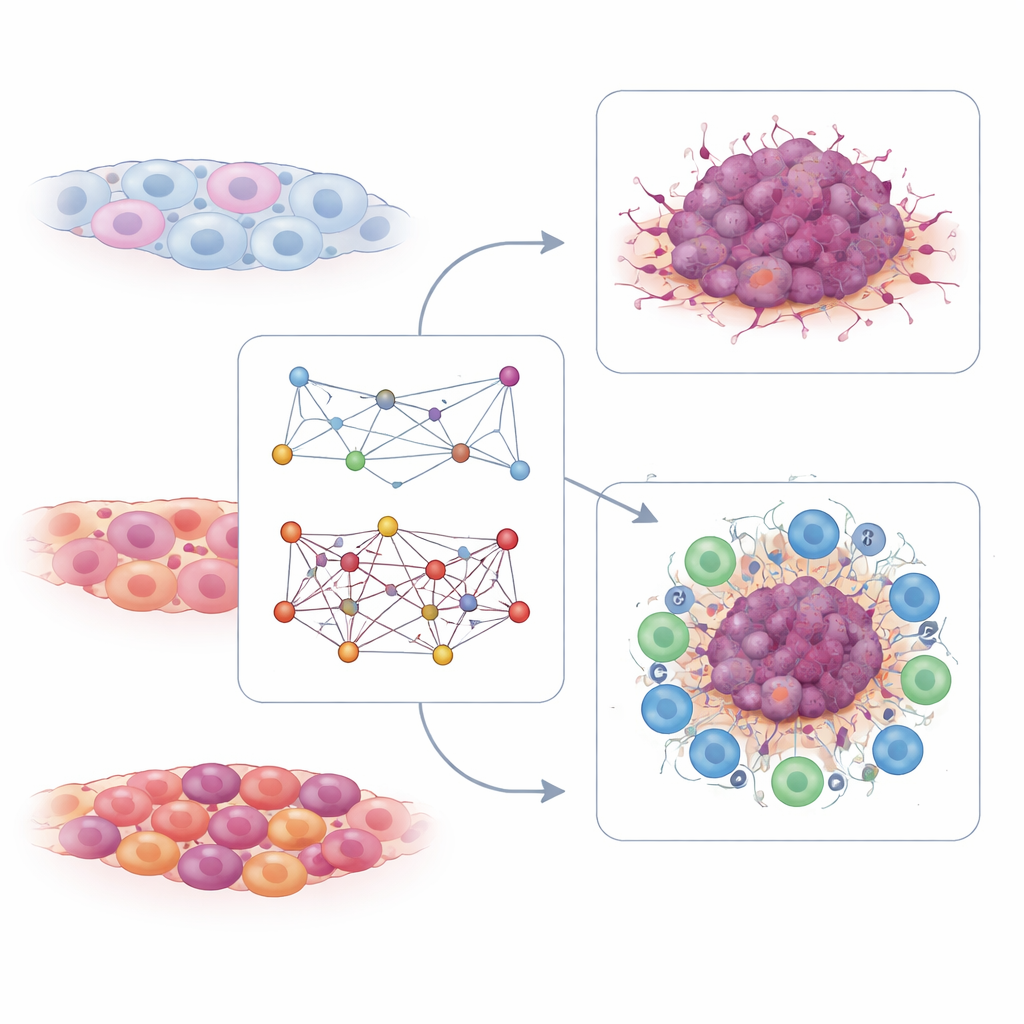
Immunstärke aus T‑Zellen ablesen
Die T‑Zell‑Interaktionskarte erzählte eine ergänzende Geschichte. Hier suchten die Forschenden nach Genpaaren, deren gemeinsame Aktivität in T‑Zellen mit gutem oder schlechtem Ansprechen auf eine Checkpoint‑Inhibitor‑Therapie verknüpft war, eine Form der Immuntherapie, die T‑Zellen gegen den Krebs freisetzt. Sie fanden Hunderte von Paaren, die mit entweder Ansprechbarkeit oder Resistenz verbunden waren. Daraus destillierten sie eine kleine Signatur aus nur sechs Interaktionspaaren, die an der T‑Zell‑Rezeptor‑Signalgebung beteiligt sind. In mehreren unabhängigen Patientendatensätzen zeigten höhere Werte dieses T‑Zell‑Interaktionsscores Personen, die auf PD‑1‑basierte Immuntherapie ansprachen, und er waren mit längerer Überlebenszeit verbunden. Tumoren mit hohen T‑Zell‑Scores wiesen tendenziell eine „heiße“ Immunumgebung mit vielen aktiven Immunzellen auf, während niedrige Scores „kalte“ Tumoren markierten, die weniger wahrscheinlich von diesen Medikamenten profitieren.
Was das für die künftige Krebsbehandlung bedeutet
Diese Arbeit zeigt, dass man nicht nur betrachten sollte, welche Gene angeschaltet sind, sondern auch, wie Genpaare innerhalb bestimmter Zelltypen gemeinsam aktiviert werden. Das kann verborgene Struktur in Tumoren offenlegen. Beim Lungenadenokarzinom helfen Muster kooperativer Genaktivität in Krebszellen, aggressivere Verläufe zu kennzeichnen, während ähnliche Muster in T‑Zellen vorhersagen können, wer von einer Immuntherapie profitiert. Auch wenn diese Interaktionskarten auf Korrelationen und nicht auf direkten Experimenten beruhen, bieten sie eine neue Möglichkeit, die interne Verschaltung eines Tumors aus Einzelzell‑Daten zu lesen, und könnten bei Verfeinerung und Ausweitung auf andere Krebsarten zu präziseren Diagnosen, Prognosen und Therapieentscheidungen beitragen.
Zitation: Chen, B., Liu, M., Dong, Q. et al. Charting cell-type-specific positive genetic interaction at single-cell resolution for lung adenocarcinoma. npj Precis. Onc. 10, 137 (2026). https://doi.org/10.1038/s41698-026-01328-x
Schlüsselwörter: Lungenadenokarzinom, Einzelzellgenomik, genetische Interaktionen, Tumormikroumgebung, Immuntherapieansprechen