Clear Sky Science · zh
开发一种创新的纳米聚合物‑lncRNA‑SRHC 复合体作为靶向肝细胞癌治疗的治疗手段
这项研究对肝癌为何重要
原发性肝癌,尤其是肝细胞癌,是全球致死率最高的癌症之一,常常在可用治疗选项受限时才被发现。本研究探索了一种通过将保护性“纳米”载体与健康肝脏用以控制细胞增殖的天然 RNA 分子相结合来阻止肝肿瘤生长的新方法。该工作在小鼠中完成,但基于人类数据,显示出比传统化疗更温和、更精确的治疗前景。
肝细胞中缺失的安全开关
健康肝细胞产生一种名为 SRHC 的长链 RNA,虽不编码蛋白,但有助于维持增殖信号的平衡。在肝癌中,SRHC 水平大幅下降,移除了对细胞分裂的重要制动。早期研究表明,恢复 SRHC 可在体外减缓或抑制肝癌细胞,但该分子易碎且在体内易被破坏。作者首先利用大型人类肿瘤数据库确认 SRHC 在正常肝组织中丰度高,而在肝细胞癌中持续降低,这进一步支持其作为抑瘤因子的作用并可能成为治疗靶点的想法。
构建微小递送载体
为将 SRHC 送回受损肝脏,研究团队转向纳米技术。他们用一种已知的可生物降解材料 PLGA 制成微小球体,该材料已用于医学产品。在颗粒形成过程中将 SRHC 链混入,使 RNA 紧密嵌入聚合物壳中。测量显示所得纳米颗粒直径约为 200 纳米——足够小以通过肿瘤渗漏的血管,又足够大以避免被肾脏迅速清除——并带有强烈的表面电荷,防止聚集并有助于与细胞膜相互作用。在使用人肝癌细胞的细胞培养实验中,自由 SRHC 与装载 SRHC 的纳米颗粒均降低了癌细胞存活率,其中纳米制剂表现出稍强的活性。
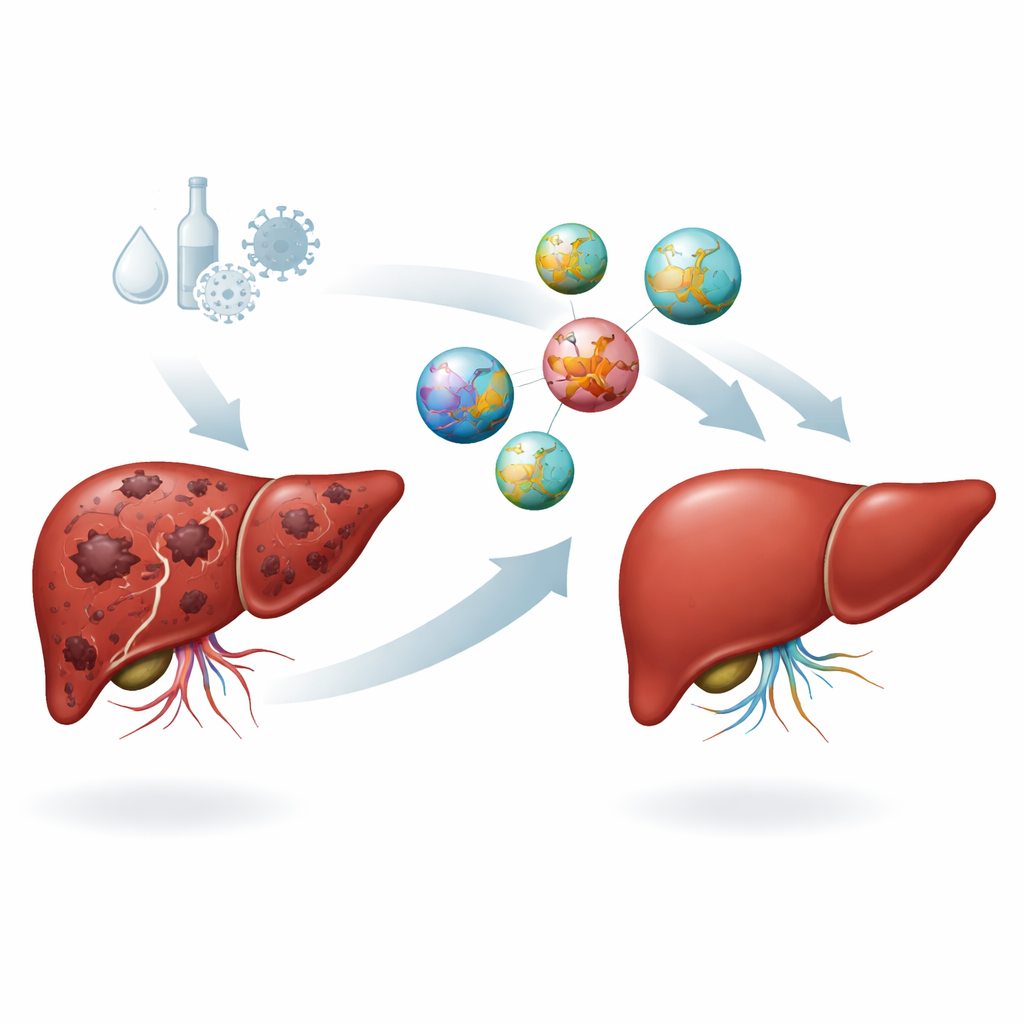
在活体中测试疗法
真正的考验是在通过长期接触化学致癌物建立的小鼠肝癌模型中进行的。一组小鼠作为健康对照,其他小鼠发育出肝肿瘤后接受无治疗、空载纳米颗粒、自由 SRHC 或直接注入肝脏的 SRHC‑载纳米颗粒。研究人员在十六周内追踪与肿瘤生长相关的血液标志物,包括甲胎蛋白以及若干驱动新血管形成和炎症的信号。仅接受致癌化学物质或空载纳米颗粒的小鼠在所有这些标志物上均显示很高的水平,证实了疾病的侵袭性。相比之下,SRHC 与 SRHC‑纳米颗粒治疗都显著降低了肿瘤相关信号,而纳米‑SRHC 联合方式导致的下降幅度最大。
洞察基因和组织结构
为了解肝脏内发生的变化,团队检查了关键基因和组织切片。在未治疗的肿瘤小鼠中,促进生长和扩散的基因(SENP1 与 β‑连环蛋白)高度活跃,而维持正常肝脏身份的基因(HNF‑4α)被强烈抑制。自由 SRHC 部分逆转了这种模式,但 SRHC‑纳米颗粒治疗效果更强,抑制了促癌信号并恢复了保护性基因。显微观察也得出相同结论:未治疗或空载纳米颗粒组的肝脏结构紊乱,充斥异常细胞和新生血管,而 SRHC 处理的肝脏恶性改变较少。纳米‑SRHC 组最接近正常,叶状结构更清晰,并出现对残余肿瘤细胞的免疫清除迹象。重要的是,任何治疗组均未显示明显的毒性或痛苦迹象。
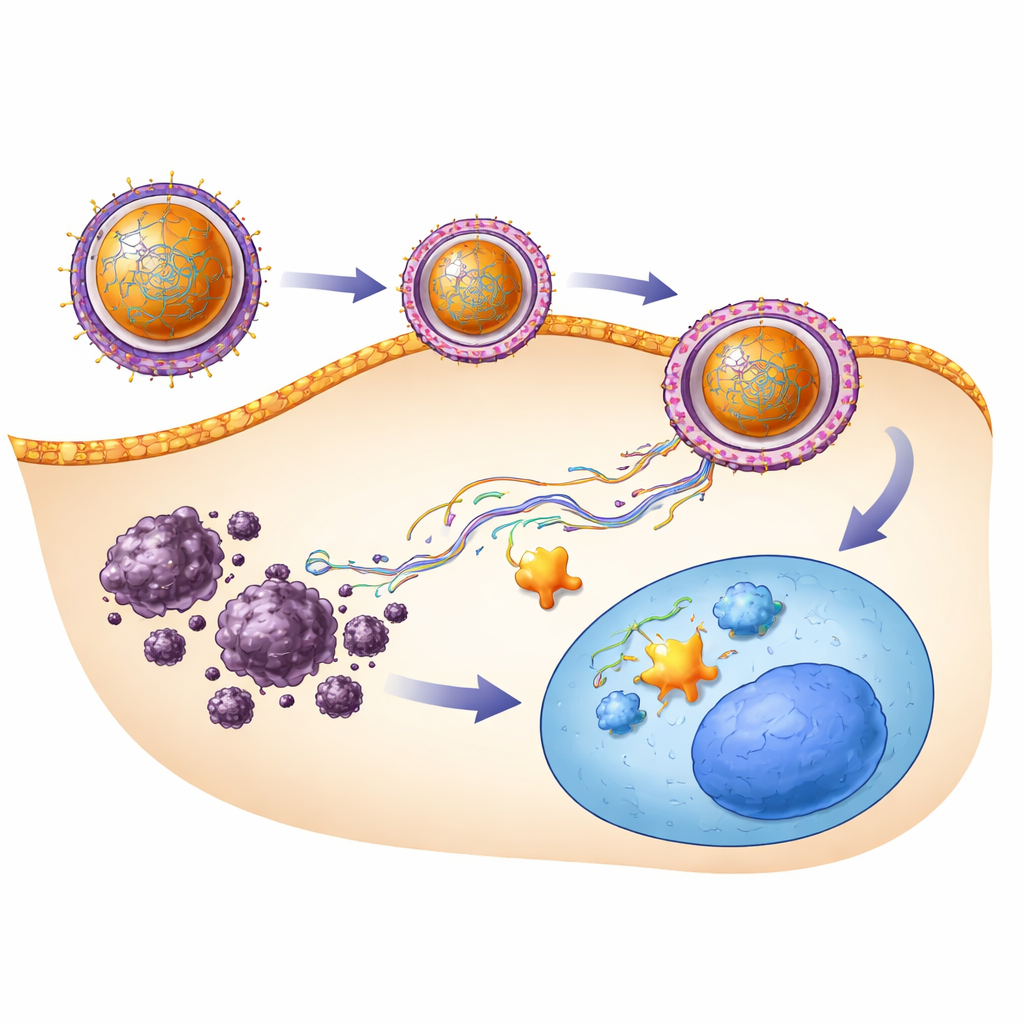
这对未来治疗的意义
简而言之,这项研究表明,在肝细胞中替换丢失的“刹车”分子并用智能纳米载体保护它,能够在小鼠中减缓或逆转肝癌而无明显危害。SRHC‑纳米颗粒复合体不仅降低了肿瘤标志物和危险的生长信号,还帮助重建正常的肝组织结构。尽管在这一策略进入临床之前仍需大量工作——包括优化递送途径、确保长期安全性以及与现有药物的联合——这些结果突出了一个有前景的策略:使用工程化颗粒将脆弱的基因调控因子运回其该在之处,从内部抑制癌症。
引用: Elkramani, N., Elzallat, M., Mohammed, D.M. et al. Development of an innovative nanopolymer-lncRNA-SRHC complex as therapeutic modalities for targeted hepatocellular carcinoma therapy. Sci Rep 16, 14695 (2026). https://doi.org/10.1038/s41598-026-51340-1
关键词: 肝细胞癌, 纳米颗粒治疗, 长链非编码 RNA, 肝癌治疗, 靶向药物递送