Clear Sky Science · ru
Разработка инновационного комплекса нанополимер‑lncRNA‑SRHC в качестве терапевтического средства для таргетной терапии гепатоцеллюлярной карциномы
Почему это исследование важно для рака печени
Первичный рак печени, особенно гепатоцеллюлярная карцинома, входит в число самых смертельных злокачественных опухолей в мире и часто остается невыявленным до тех пор, пока варианты лечения не становятся ограниченными. В этом исследовании изучается новый подход к приостановке роста печеночных опухолей: сочетание защитного «нано»‑носителя с естественной РНК-молекулой, которую здоровая печень использует для контроля клеточного деления. Работа выполнена на мышиной модели, но опирается на данные человека, и указывает на более мягкую и точную терапию по сравнению с традиционной химиотерапией.
Отсутствующий предохранитель в клетках печени
Здоровые клетки печени вырабатывают длинную РНК под названием SRHC, которая не кодирует белок, но помогает поддерживать баланс сигналов роста. При раке печени уровень SRHC резко снижается, что устраняет важный тормоз клеточного деления. Ранее предполагалось, что восстановление SRHC может замедлять или останавливать рост раковых клеток в культуре, однако эта молекула хрупка и легко разрушается в организме. Авторы сначала использовали крупные базы данных опухолей человека, чтобы подтвердить, что SRHC обилен в нормальной печеночной ткани, но стабильно снижен при гепатоцеллюлярной карциноме, что подкрепляет идею о его роли супрессора опухолей и его потенциале в качестве терапевтической мишени.
Создание крошечного транспортного средства
Чтобы вернуть SRHC в повреждённую печень, команда обратилась к нанотехнологиям. Они создали микросферы из известного биоразлагаемого материала PLGA, уже применяемого в медицинских изделиях. Строки SRHC смешивали в процессе формирования частиц так, чтобы РНК плотно вошла в полимерную оболочку. Измерения показали, что полученные наночастицы имеют размер около 200 нанометров — достаточно малы, чтобы проходить через «протекающие» сосуды опухоли, но достаточно крупны, чтобы избежать быстрого выведения почками — и обладают выраженным зарядом поверхности, который препятствует их агрегации и способствует взаимодействию с клеточными мембранами. В тестах in vitro на культурах человеческих раковых клеток печени и свободный SRHC, и SRHC в наночастицах снижали выживаемость раковых клеток, при этом наноформулация проявляла несколько более сильный эффект.
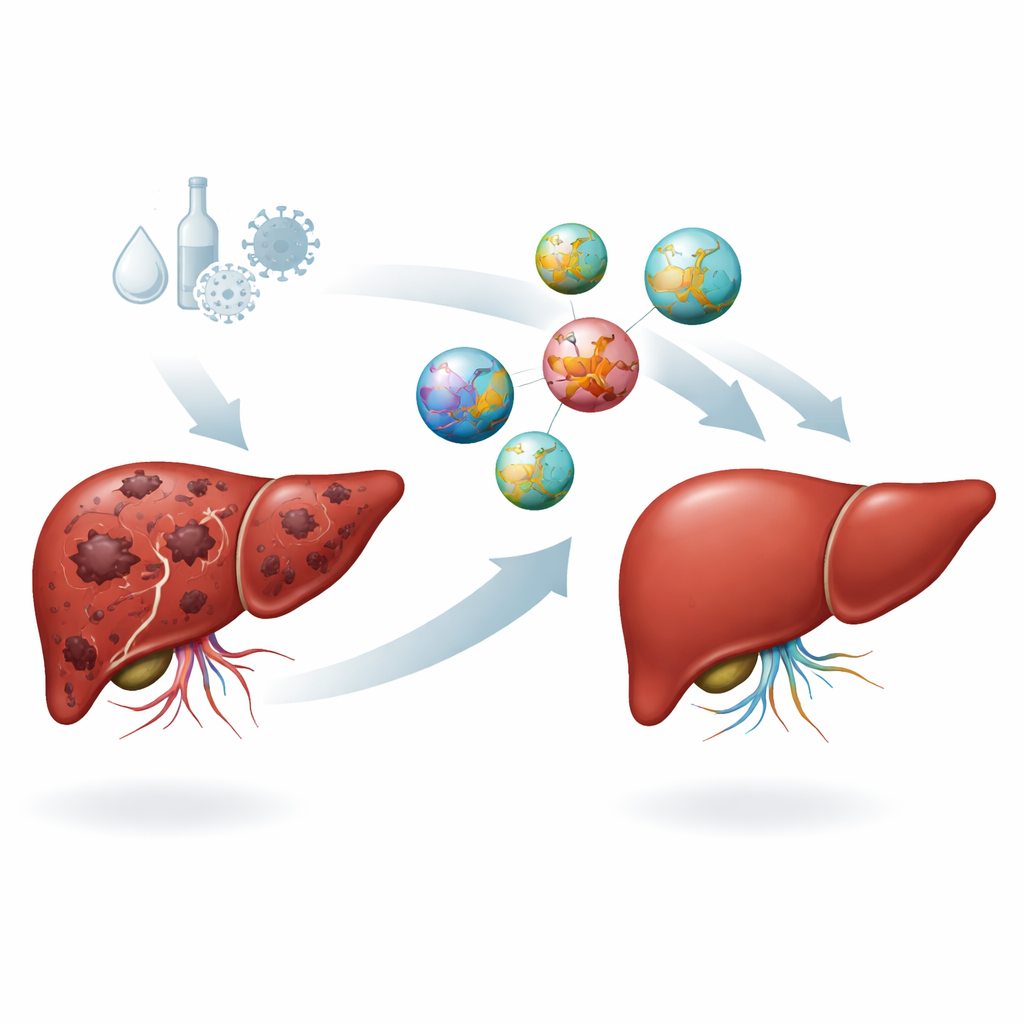
Испытание терапии в живом организме
Реальное испытание проводили на мышиной модели рака печени, вызванной длительным воздействием химического канцерогена. Одна группа мышей оставалась здоровым контролем, в то время как у других развивались печеночные опухоли; затем животные получали либо отсутствие лечения, либо пустые наночастицы, либо свободный SRHC, либо наночастицы с SRHC, вводимые непосредственно в печень. В течение шестнадцати недель исследователи отслеживали в крови маркеры, ассоциированные с ростом опухоли, включая альфа‑фетопротеин, а также несколько сигналов, стимулирующих неоваскуляризацию и воспаление. Мыши, получавшие только канцероген или пустые наночастицы, демонстрировали очень высокие уровни всех этих маркеров, подтверждая агрессивное течение болезни. Напротив, как свободный SRHC, так и лечение SRHC‑в‑наночастицах резко понижали опухолевые сигналы, при этом комбинированный нано‑SRHC подход давал наибольшее снижение.
Взгляд на гены и структуру ткани
Чтобы понять происходящее внутри печени, команда изучала ключевые гены и срезы ткани. У не лечённых мышей с опухолями были высокоактивны гены, способствующие росту и метастазированию (SENP1 и β‑катенин), тогда как ген, поддерживающий нормальную печёночную идентичность (HNF‑4α), был сильно подавлен. Свободный SRHC частично обратил этот паттерн, но терапия SRHC‑в‑наночастицах сделала это более эффективно, снижая онкогенные сигналы и восстанавливая защитный. Микроскопическое исследование подтвердило эти результаты: печень у не леченных или получавших пустые наночастицы животных была дезорганизована, заполнена аномальными клетками и новыми сосудами, тогда как у животных, получавших SRHC, отмечалось меньше злокачественных изменений. Группа, получавшая нано‑SRHC, была ближе всего к норме: более чёткая дольчатая структура и признаки активной иммунной очистки остаточных опухолевых клеток. Важно, что ни одна из групп лечения не показала явных признаков токсичности или дистресса.
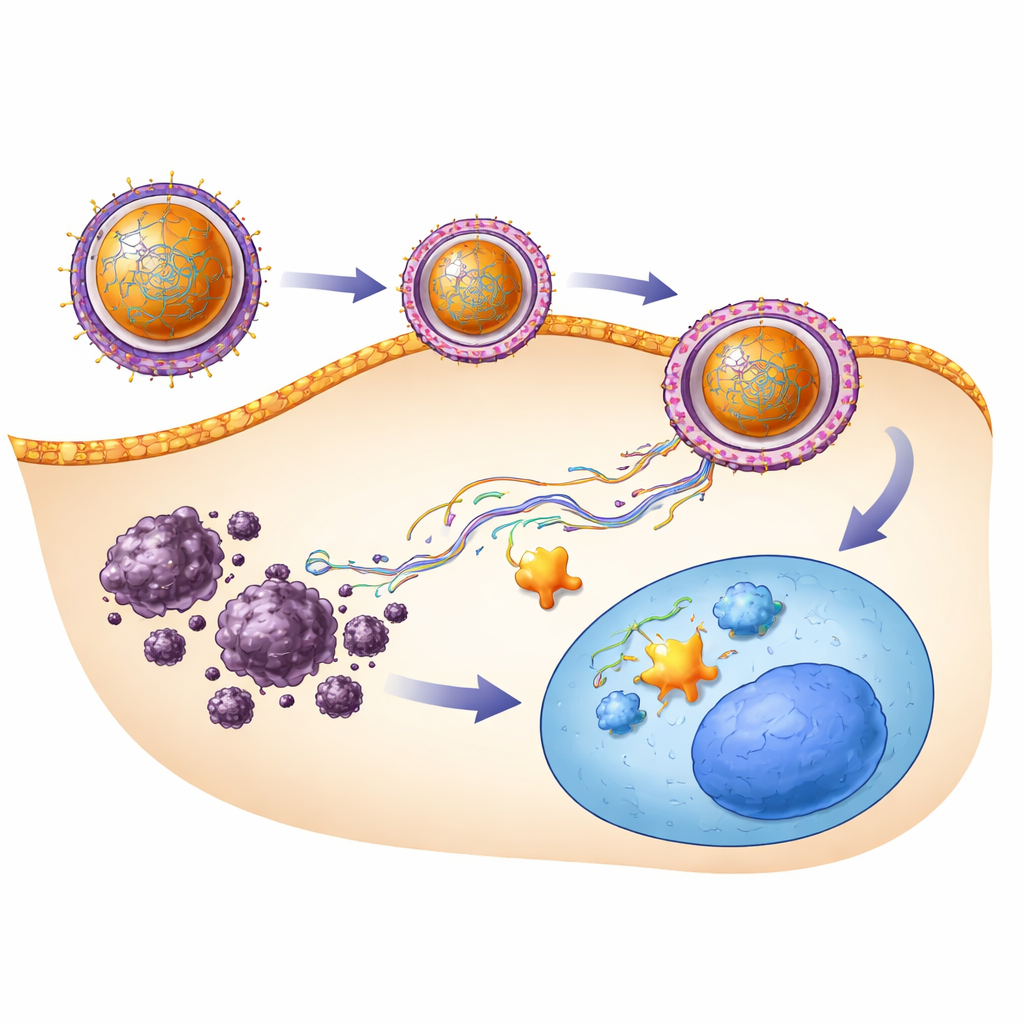
Что это может значить для будущих методов лечения
Проще говоря, это исследование показывает, что замена отсутствующей «тормозящей» молекулы в клетках печени и её защита с помощью умного нано‑носителя может замедлить или обратить развитие рака печени у мышей без очевидного вреда. Комплекс SRHC‑в‑наночастицах не только уменьшил опухолевые маркеры и опасные сигналы роста, но и способствовал восстановлению нормальной архитектуры печени. Хотя предстоит много работы, прежде чем такой подход достигнет пациентов — включая оптимизацию путей доставки, подтверждение долгосрочной безопасности и комбинацию с существующими препаратами — эти результаты выделяют перспективную стратегию: использование специально разработанных частиц для доставки хрупких генетических регуляторов туда, где они нужны, чтобы подавить рак изнутри.
Цитирование: Elkramani, N., Elzallat, M., Mohammed, D.M. et al. Development of an innovative nanopolymer-lncRNA-SRHC complex as therapeutic modalities for targeted hepatocellular carcinoma therapy. Sci Rep 16, 14695 (2026). https://doi.org/10.1038/s41598-026-51340-1
Ключевые слова: гепатоцеллюлярная карцинома, терапия наночастицами, длинная некодирующая РНК, лечение рака печени, таргетная доставка лекарств