Clear Sky Science · it
Sviluppo di un innovativo complesso nanopolimero-lncRNA-SRHC come modalità terapeutiche per la terapia mirata del carcinoma epatocellulare
Perché questa ricerca è importante per il cancro al fegato
Il tumore primario del fegato, in particolare il carcinoma epatocellulare, è uno dei tumori più letali al mondo e spesso rimane inosservato fino a quando le opzioni di trattamento sono limitate. Questo studio esplora un nuovo modo per arrestare la crescita dei tumori epatici combinando un vettore «nano» protettivo con una molecola di RNA naturale che il fegato sano utilizza per regolare la proliferazione cellulare. Il lavoro, condotto su modelli murini ma basato su dati umani, indica una terapia più delicata e precisa rispetto alla chemioterapia tradizionale.
Un interruttore di sicurezza mancante nelle cellule epatiche
Le cellule del fegato sano producono una lunga molecola di RNA chiamata SRHC, che non codifica per una proteina ma contribuisce a mantenere l’equilibrio dei segnali di crescita. Nel cancro del fegato i livelli di SRHC diminuiscono drasticamente, rimuovendo un importante freno alla divisione cellulare. Studi precedenti hanno suggerito che il ripristino di SRHC può rallentare o bloccare le cellule di carcinoma epatocellulare in coltura, ma la molecola è fragile e facilmente degradata nell’organismo. Gli autori hanno prima utilizzato grandi banche dati di tumori umani per confermare che SRHC è abbondante nel tessuto epatico normale ma costantemente ridotto nel carcinoma epatocellulare, rafforzando l’idea che agisca come soppressore tumorale e possa costituire un bersaglio terapeutico.
Costruire un minuscolo veicolo di rilascio
Per riportare SRHC nei fegati danneggiati, il team si è rivolto alla nanotecnologia. Hanno costruito sfere microscopiche da un noto materiale biodegradabile chiamato PLGA, già impiegato in prodotti medici. Fili di SRHC sono stati incorporati durante la formazione delle particelle in modo che l’RNA risultasse saldamente inglobato nel guscio polimerico. Le misurazioni hanno mostrato che le nanoparticelle ottenute avevano un diametro di circa 200 nanometri—abbastanza piccole da attraversare i vasi sanguigni tumorali permeabili ma abbastanza grandi da evitare l’eliminazione rapida attraverso i reni—andavano dotate di una forte carica superficiale che ne impedisce l’aggregazione e facilita l’interazione con le membrane cellulari. In test su colture cellulari di carcinoma epatico umano, sia l’SRHC libero sia le nanoparticelle cariche di SRHC hanno ridotto la sopravvivenza delle cellule tumorali, con la nano-formulazione che mostrava una attività leggermente più marcata.
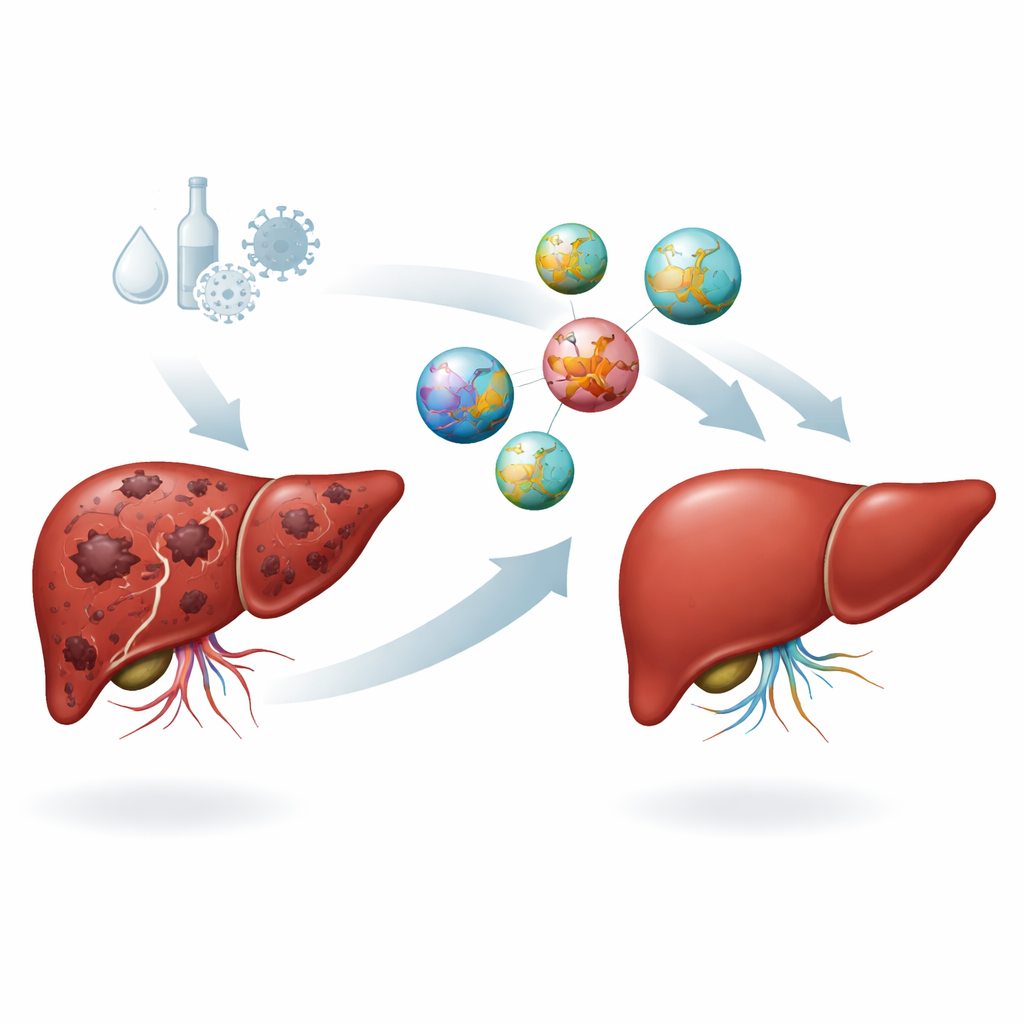
Testare la terapia in un organismo vivente
La prova decisiva è arrivata in un modello murino di cancro al fegato indotto da esposizione prolungata a un carcinogeno chimico. Un gruppo di topi è rimasto come controllo sano, mentre altri hanno sviluppato tumori epatici e poi non hanno ricevuto trattamento, nanoparticelle vuote, SRHC libero o nanoparticelle cariche di SRHC iniettate direttamente nel fegato. Per sedici settimane i ricercatori hanno monitorato i marker ematici associati alla crescita tumorale, inclusa l’alfa-fetoproteina e diversi segnali che promuovono la formazione di nuovi vasi e l’infiammazione. I topi trattati solo con il chimico o con nanoparticelle vuote hanno mostrato livelli molto elevati di tutti questi marker, confermando una malattia aggressiva. Al contrario, sia SRHC libero sia il trattamento con nanoparticelle-SRHC hanno ridotto nettamente i segnali tumorali, con l’approccio nano-SRHC che ha prodotto la diminuzione più marcata.
Esaminare geni e struttura tissutale
Per capire cosa stesse accadendo all’interno del fegato, il team ha analizzato geni chiave e sezioni tissutali. Nei topi portatori di tumore non trattati, i geni che promuovono crescita e diffusione (SENP1 e β-catenina) risultavano molto attivi, mentre un gene che mantiene l’identità epatica normale (HNF-4α) era fortemente soppresso. L’SRHC libero ha parzialmente invertito questo quadro, ma il trattamento con SRHC–nanoparticelle l’ha fatto in modo più incisivo, riducendo i segnali pro-tumorali e ripristinando quello protettivo. L’ispezione microscopica ha raccontato la stessa storia: i fegati dei gruppi non trattati o con nanoparticelle vuote erano disorganizzati, densi di cellule anomale e nuovi vasi, mentre i fegati trattati con SRHC mostravano meno alterazioni maligne. Il gruppo nano-SRHC si è avvicinato maggiormente alla normalità, con una struttura lobulare più chiara e segni di un’attiva rimozione immunitaria delle cellule tumorali residue. È importante sottolineare che in nessun gruppo di trattamento sono emersi segni evidenti di tossicità o disagio.
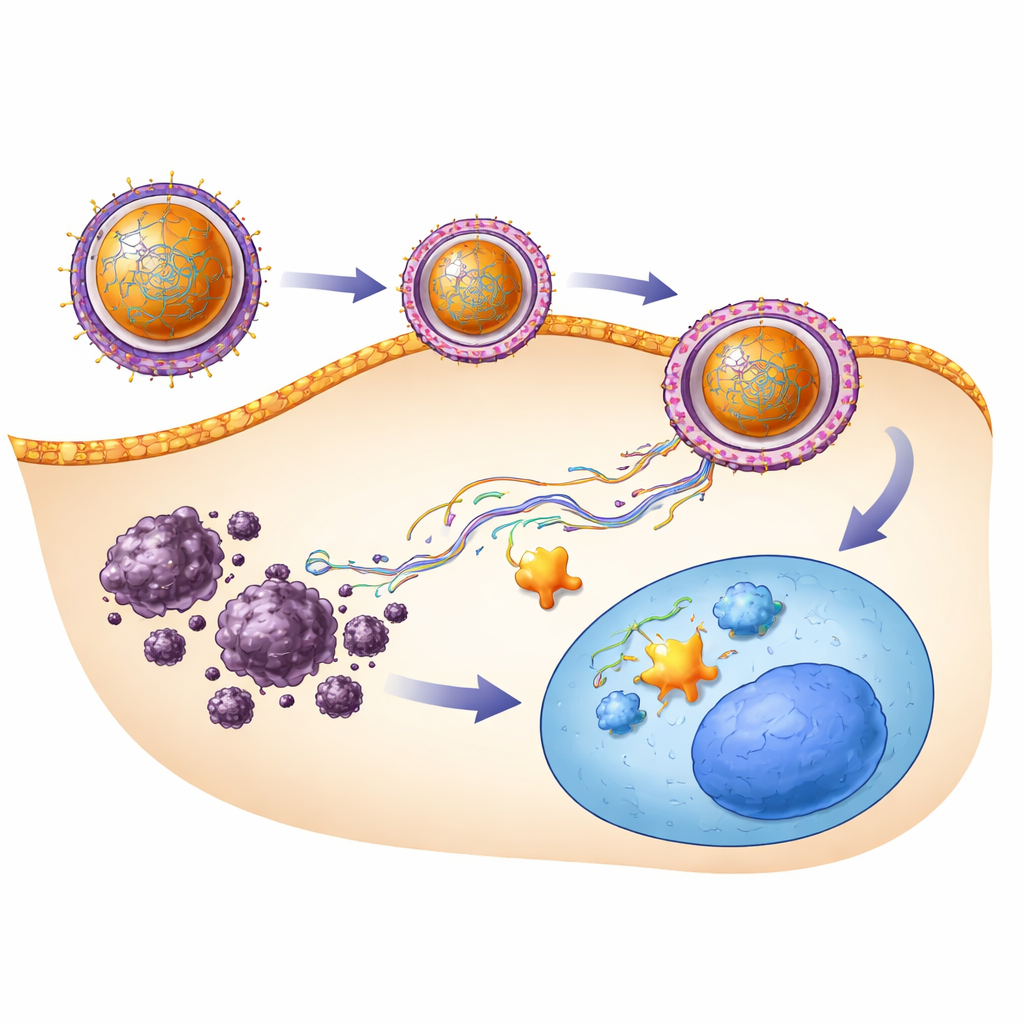
Cosa potrebbe significare per i trattamenti futuri
In parole semplici, questo studio mostra che sostituire una molecola «freno» mancante nelle cellule del fegato e proteggerla con un intelligente nanovettore può rallentare o invertire il cancro epatico nei topi senza danni evidenti. Il complesso SRHC–nanoparticelle non solo ha ridotto i marker tumorali e i segnali di crescita pericolosi, ma ha anche contribuito a ricostruire l’architettura epatica normale. Pur restando molto lavoro prima che un approccio simile possa arrivare ai pazienti—comprese la messa a punto delle vie di somministrazione, la verifica della sicurezza a lungo termine e la sua integrazione con farmaci esistenti—questi risultati evidenziano una strategia promettente: utilizzare particelle ingegnerizzate per trasportare regolatori genetici fragili al loro sito d’azione, spegnendo il cancro dall’interno.
Citazione: Elkramani, N., Elzallat, M., Mohammed, D.M. et al. Development of an innovative nanopolymer-lncRNA-SRHC complex as therapeutic modalities for targeted hepatocellular carcinoma therapy. Sci Rep 16, 14695 (2026). https://doi.org/10.1038/s41598-026-51340-1
Parole chiave: carcinoma epatocellulare, terapia con nanoparticelle, RNA lungo non codificante, trattamento del cancro del fegato, consegna mirata del farmaco